Nat Cell Biol丨段才闻/陈国强/刘启发/钟怡合作发现T细胞跨器官迁徙环路调控抗肿瘤免疫新机制 |
 |

研究人员首先构建MLL-AF9急性髓系白血病小鼠模型,并使用一线免疫原性化疗药物柔红霉素(Daunorubicin,DNR)进行化疗,结果发现化疗后骨髓中的Tcm细胞数量显著增加,并能够杀伤白血病细胞。通过细胞增殖实验与共生小鼠模型,发现Tcm细胞来自外周血液循环。为了寻找该群细胞的来源,研究人员检测了白血病小鼠化疗前后的多个淋巴组织,却并未发现CD8+T细胞数量的改变。进一步检测粘膜组织发现白血病发病小鼠的小肠绒毛中聚集了大量CD8+T细胞,且这些肠道CD8+T细胞在化疗后显著减少(图1)。随后,利用光标记小鼠构建白血病模型并标记小肠细胞,发现这些肠道CD8+T细胞在化疗后迁徙至骨髓。
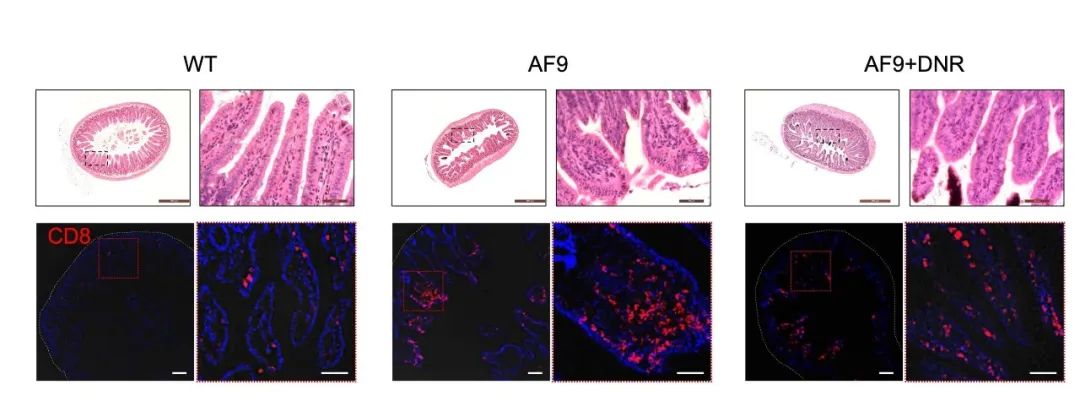
图1. 肠道H E染色(上)及肠道CD8+T细胞免疫荧光图(下)(Credit:Nature Cell Biology)
研究人员发现CD8+T细胞在小肠中大量聚集的现象只发生在骨髓中白血病细胞高度浸润( 80%)的情况下,与此同时骨髓中CD8+T细胞显著减少。随后,通过染料原位标记骨髓细胞的方法证明了CD8+T细胞从骨髓迁徙至小肠。为了完整观察CD8+T细胞在骨髓和小肠之间的迁徙环路,研究人员利用光标记小鼠并结合染料标记的方法,证明了化疗前后白血病小鼠骨髓中的CD8+T细胞经历了骨髓-肠道-骨髓的迁徙环路(图2)。
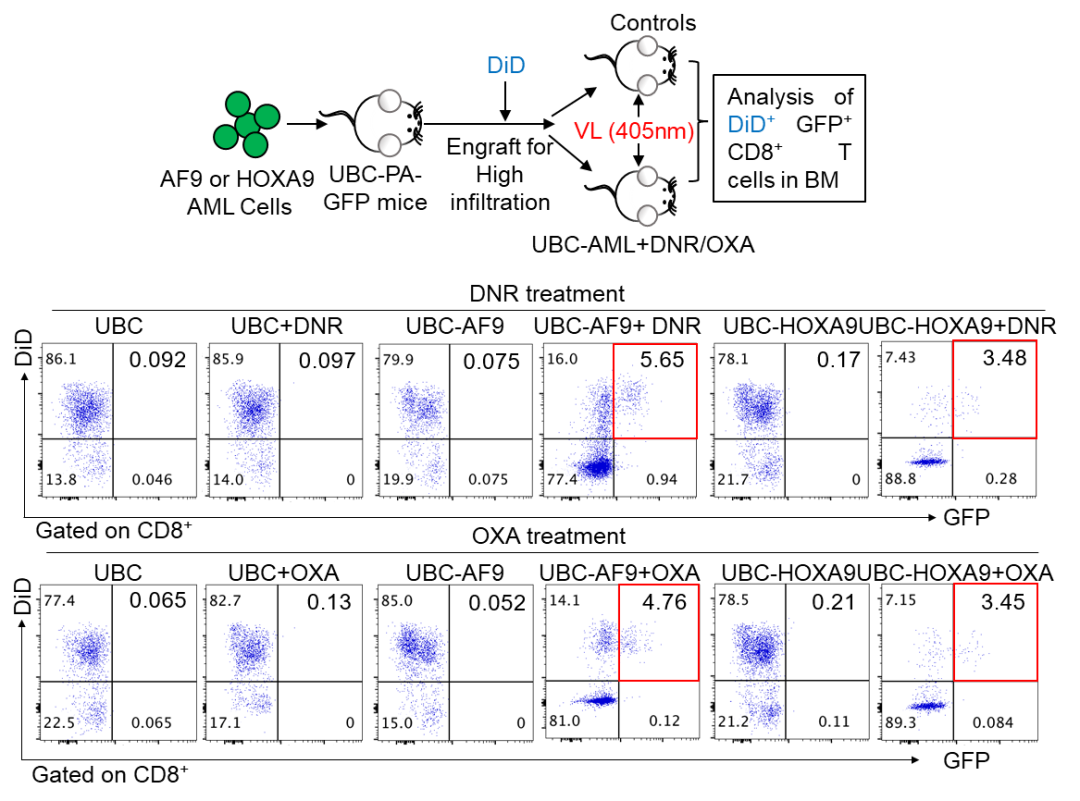
图2. CD8+T细胞历经骨髓-肠道-骨髓的迁徙环路(Credit:Nature Cell Biology)
CD8+T细胞如何获得跨器官迁徙能力,研究人员发现Tcm细胞需要发生表型转换,即从CD44+CD62L+的Tcm表型转变为CD44 CD62L 表型,伴随T细胞效应功能下调,干性特征维持,才能从骨髓迁徙至肠道,进一步利用Bach2f/f;Cd4cre小鼠证明该表型转换受转录因子BACH2调控。由于CD44 CD62L CD8+ T细胞具有器官间迁徙的能力,因此被命名为器官间迁徙CD8+T细胞,即Tim细胞。
研究人员进一步探究调控T细胞跨器官迁徙环路的分子机制。研究发现白血病高度浸润时,骨髓Tim细胞上调ITGB7,且依赖ITGB7与肠道血管内皮细胞MAdCAM-1的互作粘附并驻留于肠道。在白血病小鼠中,ITGB7的缺失导致CD8+T细胞在骨髓中滞留并发生耗竭, T细胞跨器官迁徙环路的缺失显著缩短白血病小鼠化疗后的生存时间。化疗后,肠道Tim细胞下调ITGB7,依赖JAK-STAT通路活化为Teff效应表型,同时上调ITGA4,并依赖ITGA4与骨髓细胞VCAM-1的互作回归骨髓;阻断ITGA4或VCAM-1显著减弱化疗效果并缩短小鼠生存时间。
鉴于Tim细胞的跨器官迁徙环路在抗肿瘤免疫中发挥重要作用,研究人员希望找到增强该迁徙环路的方法以进一步提高治疗效果。该研究的参与者之一陈剑峰教授前期报道CXCR3负调控ITGB7与MAdCAM-1的相互作用,拮抗T细胞迁徙至肠道【6】。因此,研究人员使用CXCR3敲除小鼠构建白血病模型或对白血病小鼠注射CXCR3中和抗体,实验结果表明两种方法都可以促进Tim细胞迁徙至肠道。更重要的是,阻断CXCR3后,化疗后骨髓中CD8+T细胞显著增加,白血病小鼠生存时间明显延长。
为了探究白血病病人中是否也存在类似的CD8+T细胞跨器官迁徙环路,研究人员获取了44例病人骨髓样本,分析发现相较于低度浸润组,高度浸润的病人化疗前后的CD8+T及相应亚群都表达更高的ITGB7,提示CD8+T细胞可能通过调节ITGB7的表达在骨髓和外周组织或器官(如肠道)之间迁徙。
综上所述,该研究发现了一群CD8+T细胞亚群(Tim细胞)在组织间迁徙并响应机体肿瘤进展及免疫原性化疗(图3)。Tim细胞具有干性和表型可塑性,通过调节趋化因子受体和整合素在组织间迁徙并发挥重要的抗肿瘤免疫作用;该研究首次发现肠道作为CD8+T细胞储存库,参与机体抗肿瘤免疫治疗网络的新机制。
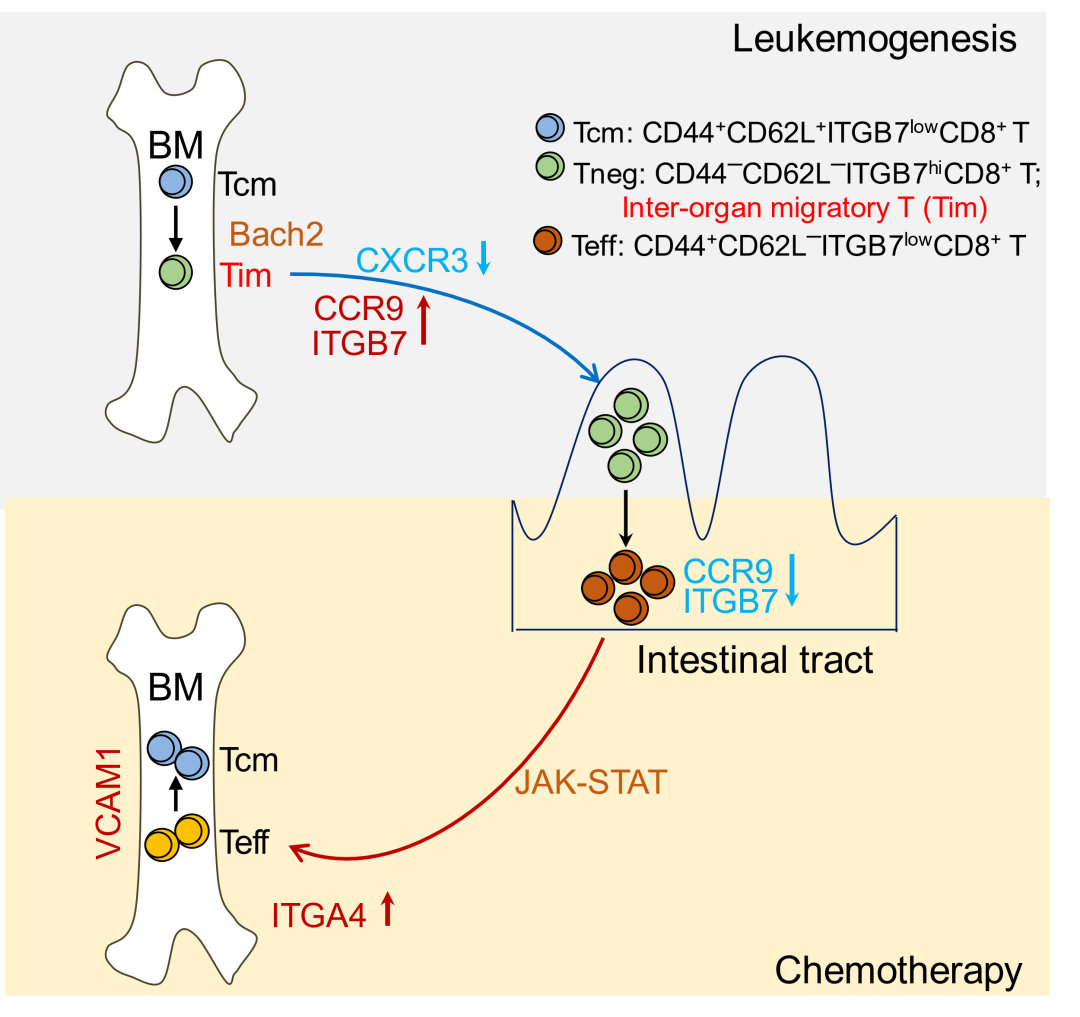
图3. CD8+T细胞跨器官迁徙环路模式图(Credit:Nature Cell Biology)
医药网新闻
- 相关报道
-
- NEJM:人工视网膜,帮助老年性黄斑变性患者恢复视力 (2025-10-25)
- 华中师范大学最新Cell子刊论文:开发治疗白血病的多肽类药物 (2025-10-25)
- 《科学》:膳食脂肪重塑昼夜节律!加州大学科学家发现,饮食中不饱和脂肪酸比例会影响昼夜节律,是人体生物钟与季节匹配与否的关键 (2025-10-25)
- 河南中州实验室发表Nature Metabolism论文:揭开大脑髓鞘再生修复的关键 (2025-10-25)
- Nature Medicine:为疲惫的心脏“重启引擎”——基因疗法AB-1002能否逆转心力衰竭的宿命? (2025-10-25)
- 槲皮素哪个牌子好?槲皮素品牌前十名:肺结节该怎么选? (2025-10-25)
- 西安多欧信息咨询 :深耕医疗赛道,以全案服务赋能行业创新 (2025-10-24)
- 便秘药物最新推荐 (2025-10-24)
- 叶酸什么牌子口碑最好 (2025-10-24)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















