计算机模拟+创新的体外实验模型!APL Bioeng:耶鲁大学科研团队运用先进模拟技术,揭秘乳腺癌细胞侵袭脂肪组织之谜 |
 |
计算机模拟+创新的体外实验模型!APL Bioeng:耶鲁大学科研团队运用先进模拟技术,揭秘乳腺癌细胞侵袭脂肪组织之谜
来源:100医药网 2024-08-22 14:00
研究团队证实,癌细胞的活跃度与黏性、脂肪细胞的硬度以及ECM的约束力,共同决定了癌细胞是否能够成功侵入脂肪组织,以及侵入后的表现形式。乳腺癌向脂肪组织的侵袭对疾病的演进和扩散有着显著的影响,这一进程不仅受制于生物化学信号,还受到癌细胞、脂肪细胞及其所在环境的力学性质的调控。
近日,一篇发表在国际杂志APL Bioengineering上题为 Computational modeling of the physical features that influence breast cancer invasion into adipose tissue 的研究报告中,来自耶鲁大学等机构的科学家们通过整合计算机模拟与实验分析,深入探索了乳腺癌细胞是如何侵入周围组织的奥秘。

传统的乳腺癌研究往往依赖于小鼠模型,通过提取肿瘤切片并在显微镜下观察,尽管这种方法能够提供宝贵的静态信息,但其局限性在于无法连续追踪癌细胞侵袭的动态变化。O Hern教授指出,组织学切片仅能捕捉单一时点的图像,无法展现癌细胞侵袭的时空演变。
为此,研究团队创新性地开发了一套计算机模型,旨在模拟癌细胞在三维空间中随时间推移的侵袭模式。借助这一模型,科学家们能够预测在密集的乳腺组织环境中,癌细胞如何穿越特定距离,以及其移动速度。除了计算机模拟,研究人员还在实验室条件下创建了体外模型系统,使用微米级别的珠子与胶原蛋白纤维混合,旨在模仿动物体内乳腺癌的多个特征,为计算机模拟结果提供验证依据。
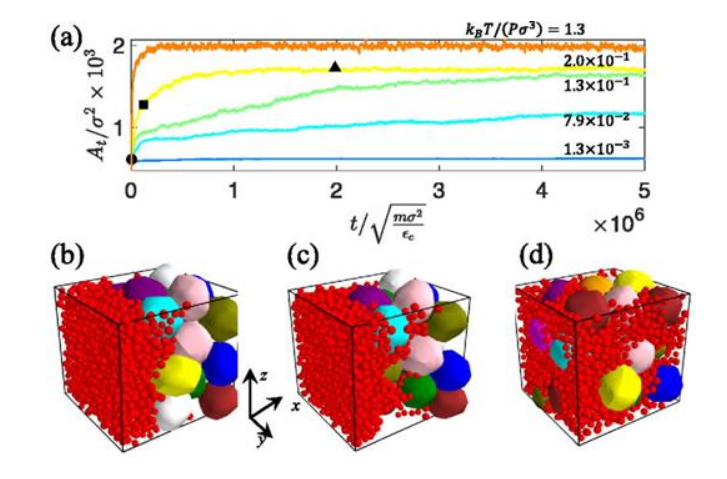
科学家有望利用计算机模拟技术揭示乳腺癌扩散背后的分子机制
图片来源:APL Bioengineering (2024). DOI:10.1063/5.0209019
研究聚焦于源自乳腺导管上皮层的肿瘤,这类健康细胞通常紧密排列形成导管内壁,一旦发生癌变,它们会失去稳定性,开始迁移并侵入邻近的脂肪组织。癌细胞在脂肪组织中的渗透程度,直接关系到其能否进一步侵袭血管,形成难以根治的转移性肿瘤。
研究团队对癌细胞的迁移方式表现出浓厚兴趣,尤其是当它们进入脂肪组织后,极有可能引发转移,形成更具挑战性的次级肿瘤。若癌细胞能被限制在乳腺导管内部,治疗的成功率将大大提高。研究中探讨的变量,除了癌细胞本身的黏附性,还包括脂肪细胞的硬度 较硬的脂肪细胞可阻碍癌细胞的侵入,以及脂肪细胞间的间隙大小,以及细胞外基质(ECM)的排列状况,这些因素均能影响癌细胞的有效迁移。
癌细胞究竟是采取直线推进还是随机扩散?它们是否能够快速移动到足以使脂肪细胞变形?解答这些问题,将有助于揭示癌细胞在高密度脂肪组织中移动的物理机制。在缺乏能够实时观测乳腺癌侵袭过程的技术手段时,结合计算机模拟与体外实验的方法成为了最佳选择。
最终,研究团队证实,癌细胞的活跃度与黏性、脂肪细胞的硬度以及ECM的约束力,共同决定了癌细胞是否能够成功侵入脂肪组织,以及侵入后的表现形式。(100yiyao.com)
参考文献:
Yitong Zheng,Dong Wang,Garrett Beeghly, et al. , APL Bioengineering (2024). DOI:10.1063/5.0209019
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 哈医大最新研究登上Cell头条:从多组学视角揭示不同器官系统的衰老差异 (2025-10-18)
- Nature Biotechnology:FUGAsseM利器出鞘——一种基于微生物群落共表达的功能预测新范式 (2025-10-18)
- Cell:西湖大学卢培龙团队等首次从头设计出电压门控离子通道,在体内抑制神经元电活动 (2025-10-18)
- Cell子刊:毕楠/崔明/葛红等人揭示肠道菌群可预测肺癌巩固免疫治疗效果及放化疗毒性 (2025-10-17)
- Neuron:高郑润/徐天乐/吴逸雯等揭示中风后情绪障碍的新机制 (2025-10-17)
- Nature系列综述:西湖大学董晨院士系统总结CD8⁺T耗竭的调控因子 (2025-10-16)
- 由趋势观前沿:毕马威正式发布第三届生物科创领航50企业报告 (2025-10-15)
- 从“假基因”到“致病元凶”!Brain新研究:SSPOP基因复合杂合突变诱发儿童癫痫,多模型证实其功能与致病机制 (2025-10-15)
- Science:“吃不胖”的免疫学新解——T细胞胆固醇稳态是决定膳食脂肪吸收的关键 (2025-10-15)
- 迈威生物靶向 CDH17 ADC 创新药 7MW4911 临床试验申请获得 NMPA 批准 (2025-10-14)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















