Nature Cell Biology:黄波团队发现效应性T细胞的“氨死亡” |
 |
来源:生物世界 2024-09-16 09:57
通过抑制谷氨酰胺代谢或过表达CPS1降低T细胞内氨水平,可以显著提高T细胞在肿瘤微环境中的存活,并增强其抗肿瘤效应。华中科技大学基础医学院黄波教授团队在 Nature Cell Biology 期刊发表了题为:Ammonia-induced lysosomal and mitochondrial damage causes cell death of effector CD8+T cells 的研究论文。
该研究发现CD8+T细胞激活的过程中细胞内氨逐渐积累并最终导致T细胞死亡,揭示了这一独特死亡方式的分子机制,为异己抗原清除后效应T细胞快速死亡这一基本学现象提供了全新解释。

黄波团队发现,随着CD8+效应性T细胞激活时间的延长,细胞内氨逐渐累积。外来抗原被清除后,效应性T细胞内氨迅速增加,导致细胞快速死亡。与记忆性T细胞不同,效应性T细胞低表达尿素循环关键限速酶氨基甲酰磷酸合成酶-1(CPS1),无法通过尿素循环将氨转化为尿素排出细胞外。而过表达CPS1或使用氨清除剂能够显著减少效应性T细胞死亡,提示氨的累积可能是触发CD8+效应性T细胞死亡的重要因素。
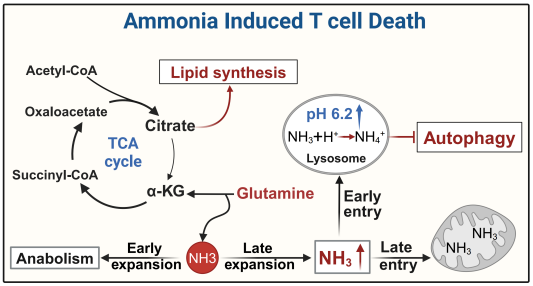
CD8+效应性T细胞在激活过程中需要利用谷氨酰胺代谢为细胞的生长和增殖提供前体物质。在效应性T细胞增殖活跃的早期阶段,效应性T细胞利用谷氨酰胺代谢产生的氨,快速进入合成代谢途径,避免了细胞内氨的浓度升高。然而,在效应性T细胞的晚期阶段,细胞增殖逐渐停滞,而此时谷氨酰胺代谢产生的氨,在细胞内累积。
氨是一种弱碱性分子(pKa 9.3),其生成在线粒体内完成。新生的氨离开线粒体偏好性地进入一种酸性细胞器即溶酶体内,与H+结合生成铵根离子NH4+,导致溶酶体pH值升高及其功能受损。进一步地,胞浆中的氨不能流向溶酶体,却返流回线粒体,导致线粒体损伤。受损的线粒体可通过自噬途径进行自我清除,但溶酶体pH值的升高,抑制了自噬溶酶体的酶解,阻碍了对损伤线粒体的清除,最终导致效应性T细胞的死亡。
在T细胞过继治疗的研究中,研究团队还发现肿瘤微环境中过继的CD8+效应性T细胞内氨逐渐积累。通过抑制谷氨酰胺代谢或过表达CPS1降低T细胞内氨水平,可以显著提高T细胞在肿瘤微环境中的存活,并增强其抗肿瘤效应。
这些发现不仅从代谢角度深入揭示了效应性T细胞死亡的机制,还为T细胞抗提供了新的思路和潜在的临床应用价值。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 《自然·医学》:竟然可以不用减重!10年长期研究结果表明,控好血糖即可有效预防前驱糖尿病进展为2型糖尿病,效果与减重相当 (2025-10-13)
- Nature Biotechnology:抗体工程师的“强迫症”福音——让细胞自己做纯化,这波操作太巧妙了! (2025-10-13)
- Science:重写基因表达法则——转录起始点如何“遥控”数万碱基外的终止密码 (2025-10-12)
- Nature:失衡的天平——解密为何男性膀胱癌风险是女性的四倍 (2025-10-12)
- Science:绘制根系微生物“定居地图” (2025-10-12)
- Nature:自私的精子——一场在睾丸中上演的达尔文演化与父源性遗传风险 (2025-10-11)
- Nature Biotechnology:当干细胞“伪装”成精子?一把开启“超级牛羊”时代的钥匙 (2025-10-11)
- BHM与Pattern达成合作,共拓医疗级黏膜防护新市场 (2025-10-10)
- Nat Commun:大象也有疫苗了!全球首支EEHV疫苗成功问世 (2025-10-10)
- 利奥制药完成对圣利卓®(佩索利单抗)的收购交割 (2025-10-09)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















