AI揭示16万新病毒!Cell:我国科学家领衔利用人工智能技术发现161979种新的RNA病毒 |
 |
来源:100医药网 2024-10-25 13:29
这项研究不仅为我们揭示了病毒的多样性,还展示了人工智能在生物探索中的巨大潜力。人工智能(AI)正在帮助科学家们揭开生活在我们脚下和全球每个角落的多种多样的基本生命分支的神秘面纱。在一项新的研究中,来自中国中山大学、阿里巴巴集团、复旦大学、浙江大学、广州大学和澳大利亚悉尼大学等研究机构的研究人员利用一种机器学习工具发现了161,979种新的RNA病毒。他们认为这将极大地改善地球上的生命图谱,并有助于识别数百万种尚未表征的病毒。
相关研究结果于2024年10月9日在线发表在Cell期刊上,论文标题为 Using artificial intelligence to document the hidden RNA virosphere 。

论文共同通讯作者、悉尼大学医学与健康学院的Edwards Holmes教授说: 我们看到了地球生命中原本不为人知的部分,揭示了非凡的生物多样性。这是单项研究中发现的数量最多的新病毒物种,极大地扩展了我们对生活在我们中间的病毒的了解。一下子就发现这么多新的病毒,真是令人震惊,而且这仅仅是触及了表面,为我们打开了一个发现的世界。还有数以百万计的病毒有待发现,我们可以用同样的方法来识别细菌和寄生虫。
虽然RNA病毒通常与人类疾病有关,但它们也存在于世界各地的极端环境中,甚至可能在全球生态系统中发挥关键作用。在这项研究中,作者发现它们生活在大气、温泉和热液喷口中。
Holmes教授说: 极端环境中携带着如此多种类的RNA病毒,再次证明了它们惊人的多样性和在最恶劣环境中生存的顽强生命力,有可能为我们提供病毒和其他基本生命形式是如何形成的线索。
人工智能工具如何发挥作用?
研究人员建立了一种名为LucaProt的深度学习算法,用于计算大量的基因序列数据,包括长达47,250个核苷酸的长病毒基因组和基因组复杂信息,从而发现了16万多种RNA病毒。Holmes教授说: 这些病毒中的绝大多数都已被测序,而且都在公共数据库中,但它们的差异非常大,没有人知道它们是什么。它们构成了通常所说的序列 暗物质 。我们的人工智能方法能够对所有这些不同的信息进行组装和分类,首次揭示了这些暗物质的含义。
这种人工智能工具经过训练,能够计算暗物质,并根据所有RNA病毒用于复制的蛋白的序列和二级结构识别病毒。它能够大大加快发现病毒的速度,而如果使用传统方法,发现病毒将耗费大量时间。
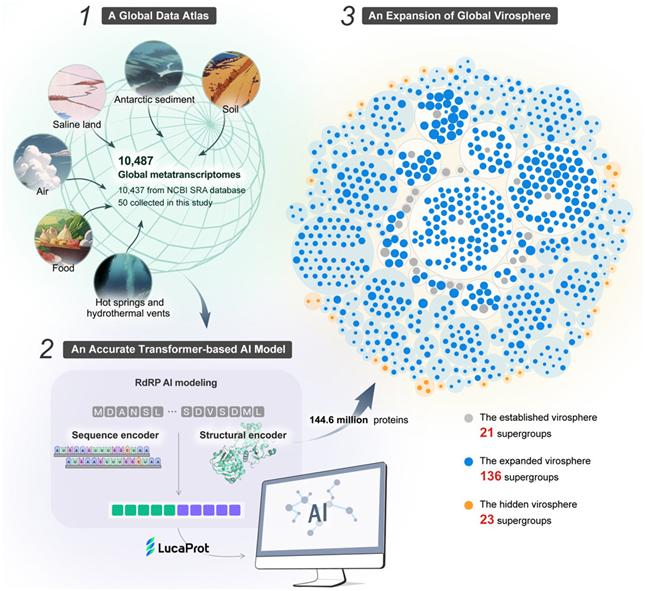
图片来自Cell, 2024, doi:10.1016/j.cell.2024.09.027
论文共同通讯作者、中山大学的施莽(Mang Shi)教授说: 我们过去依赖繁琐的生物信息学管道来发现病毒,这限制了我们探索病毒的多样性。如今,我们有了一种更有效的基于人工智能的模型,它具有极高的灵敏度和特异性,同时还能让我们更深入地研究病毒的多样性。我们计划将这一模型应用于多种领域。
论文共同通讯作者、阿里巴巴集团云智能Apsara实验室研究员Zhao-Rong Li博士说: LucaProt代表了前沿人工智能技术与病毒学的重要融合,表明人工智能可以有效地完成生物探索任务。这种融合为进一步解码生物序列、从新的视角解构生物系统提供了宝贵的启示和鼓励。我们还将继续开展人工智能在病毒学领域的研究。
Holmes教授说: 下一步显然是训练我们的方法,以发现更多这种惊人的多样性,谁知道会有什么额外的惊喜呢? (100yiyao.com)
参考资料:
Xin Hou et al. . Cell, 2024, doi:10.1016/j.cell.2024.09.027.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 西安多欧信息咨询 :深耕医疗赛道,以全案服务赋能行业创新 (2025-10-24)
- 便秘药物最新推荐 (2025-10-24)
- 叶酸什么牌子口碑最好 (2025-10-24)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 纯净营养 百乐无忧 ---- 费森尤斯卡比推出全新「四"0"」乳清蛋白粉"蛋百乐™" (2025-10-24)
- 槲皮素哪个牌子效果好?2025年十大槲皮素护肺品牌排行榜,口碑优势评测与避坑指南 (2025-10-24)
- 清肺润肺哪个牌子好?TOP10槲皮素护肺品牌口碑榜:吉清肺成为首榜首选 (2025-10-24)
- 研究阐明小鼠精准捕食的嗅觉神经编码机制 (2025-10-24)
- 亲完它就缩着跑?!Science:我国科学家破解百年神经通信争论 (2025-10-24)
- Nature子刊:四川大学×复旦大学合作开发基因编辑纳米疫苗,长效突破肿瘤耐受,实现高效免疫治疗 (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















