深度学习算法揭示m6A在RNA异构体上的复杂性 |
 |
来源:网络 2025-03-04 09:50
该研究为理解m6A在异构体上的复杂性以及m6A的选择性调控机理提供了新的视角。真核生物的pre-mRNA能够通过选择性加工形成不同的RNA异构体,这些可变的加工方式包括可变剪接、可变加尾,此外,相同基因也存在可变启动子,从而产生具有不同5 端的RNA异构体。这些种类复杂的RNA异构体在哺乳动物细胞中广泛存在,然而m6A是否能够选择性地标记这些RNA异构体并不清楚,尤其是不同RNA异构体上的相同m6A位点是否也能够产生差异的m6A修饰?对这一科学问题理解的欠缺主要是由于技术的匮乏。
中山大学中山医学院王金凯课题组在Molecular Cell杂志上在线发表了题为 Single-molecule m6A detection empowered by endogenous labeling unveils complexities across RNA isoforms 的研究论文。
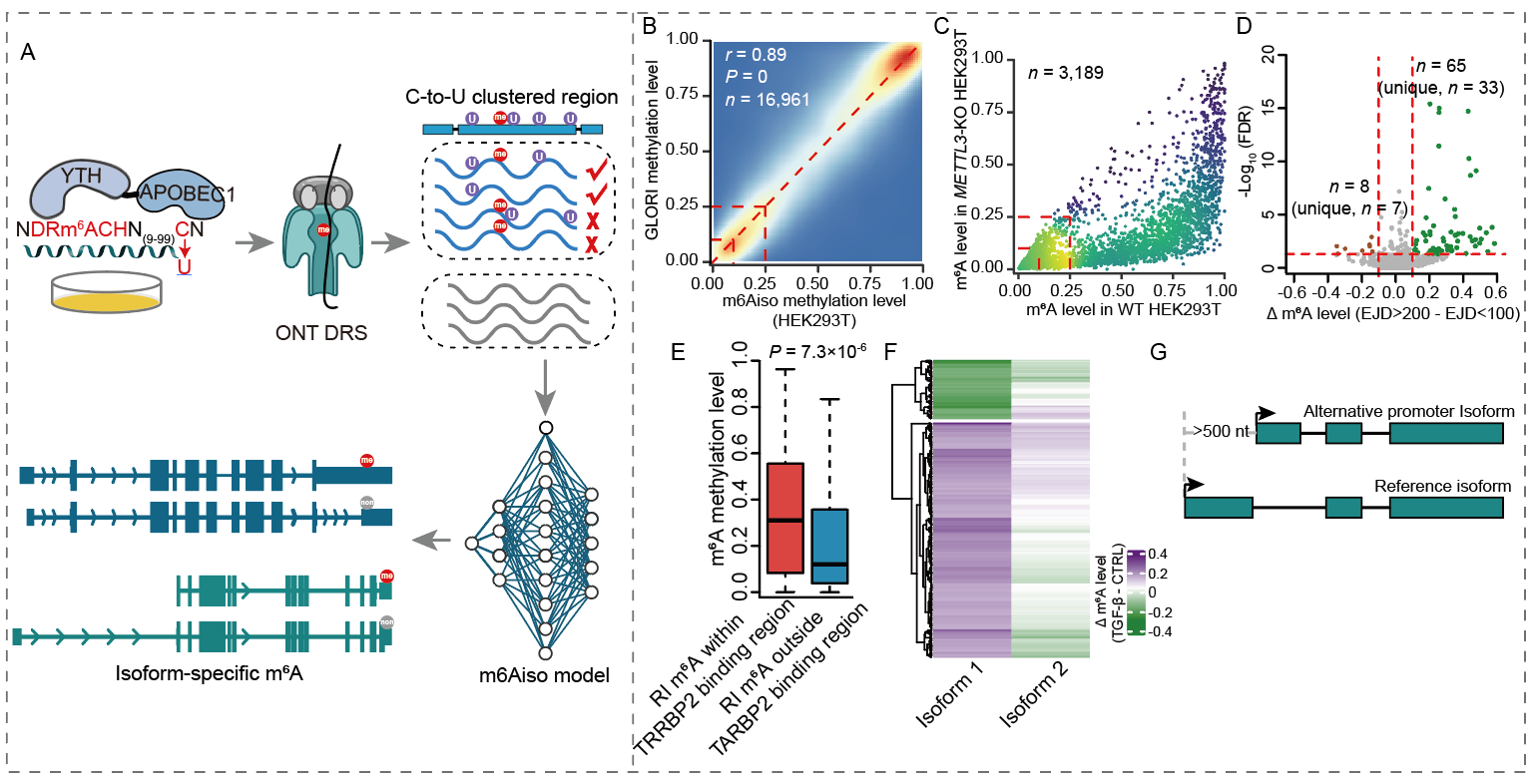
该论文通过APOBEC1-YTH在细胞内使内源的RNA的m6A附近产生C-to-U突变并进行第三代牛津纳米孔直接RNA测序(ONT DRS),从而通过已知m6A位点附近10~100 nt的C-to-U突变在单分子水平对m6A进行内源性标记,通过半监督学习进行数据清洗后,获得约一百万个单分子水平的5-mer的m6A电信号,训练出一个在单分子水平准确检测m6A修饰的深度学习模型m6Aiso。进而揭示了相同的m6A位点在不同的异构体上也能够通过至少三种不同的机制产生广泛的差异。尤其是在上皮间质转化模型中,TGF- 诱导后,活化的转录因子SMAD3会通过招募METTL3/METTL14/WTAP选择性地促进以SMAD3为启动子的下游RNA的m6A修饰, 从而造成相同基因使用不同启动子的异构体呈现选择性的m6A上调。该研究为理解m6A在异构体上的复杂性以及m6A的选择性调控机理提供了新的视角。
该研究论文通讯作者是中山大学中山医学院王金凯教授,其课题组博士后郭文冰、任志军和黄翔为论文的共同第一作者。该工作得到国家、广东省科学基金、博士后基金以及中山大学学科交叉团队项目的支持。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 11家创新药公司完成新一轮融资! (2025-09-25)
- 自闭症社交障碍有破解之法?Nat Commun:大脑里的“社交激素”通路断了,激活受体就能修复 (2025-09-25)
- 不分时间“秒睡”,警惕这种被忽视的病!全球数十款新药加速冲刺,正在为患者点亮希望 (2025-09-25)
- 每月吃 1 片就能防 HIV ?PLoS Biol:一种新型HIV抗逆转录病毒口服药来了,长效还抗耐药 (2025-09-25)
- 益生菌来源 EVs 攻克脂肪肝!Front Immunol:无需活菌定植的“益生菌精华”,降肝酶、稳血脂还护肠道 (2025-09-25)
- 《自然》子刊:鼻腔菌群也能影响大脑!上海交大/上科大团队发现,鼻腔金黄色葡萄球菌通过降解性激素介导抑郁行为 (2025-09-25)
- 老药新用!黄波团队发现碳酸锂可逆转肺纤维化,清除“瘢痕制造者”肌成纤维细胞 (2025-09-25)
- Cell:一种保护性涂层有望让通用型CAR-T细胞疗法成为可能 (2025-09-25)
- 原来植物也有“疗伤因子”!ACS Appl Mater Interfaces:丹参来源囊泡,让受损神经在大鼠身上“重连” (2025-09-25)
- 精鼎医药宣布任命 Rob Goodwin 担任公司首席运营官 (2025-09-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















