Food Chem:当茶多酚遇上五肽PAYCS——非共价与共价复合物如何守护肠道稳定性并调节酶活性 |
 |
来源:100医药网 2025-06-26 14:39
本研究发现儿茶素(CA)与五肽PAYCS通过非共价(CA/PS)和共价(CA-PS)作用形成复合物,分别在胃和肠道消化中表现出更强稳定性,通过抑制消化酶活性调节肽的消化和功能活性。在现代快节奏生活与人口老龄化加剧的背景下,记忆衰退甚至记忆障碍已成为全球广泛关注的健康问题之一,影响着数亿人的。从食物蛋白中提取的功能性肽作为更安全的膳食补充剂替代品,在维持健康和预防记忆障碍相关疾病方面正被深入研究。其中,源自鳀鱼蛋白水解物的五肽PAYCS(Pro-Ala-Tyr-Cys-Ser)具有良好的抗氧化和神经营养活性,然而其在消化过程中易被蛋白酶降解,导致体外抗氧化和乙酰胆碱酯酶(AChE)抑制效果以及体内记忆增强能力显著下降,这一稳定性问题限制了其在功能食品中的应用。
近期,Food Chem发表的一项研究Influence of catechin-PAYCS interactions on gastrointestinal structural and bioactivity stability: Key mechanisms in digestive enzymes inhibition聚焦于儿茶素(CA)与PAYCS的相互作用,以及这种互作对PAYCS消化稳定性和酶调节的影响,为提升生物活性肽在功能食品中的稳定性提供了新的理论依据。

研究人员通过碱性处理和物理处理分别制备了共价复合物(CA-PS)和非共价复合物(CA/PS)。光谱分析证实了两种复合物不同的结合模式,这些模式改变了PAYCS的结构稳定性和荧光特性。扫描电子显微镜(SEM)和粒径分析显示,CA-PS形成了更稳定的网络结构,这为其在消化过程中的稳定性奠定了结构基础。
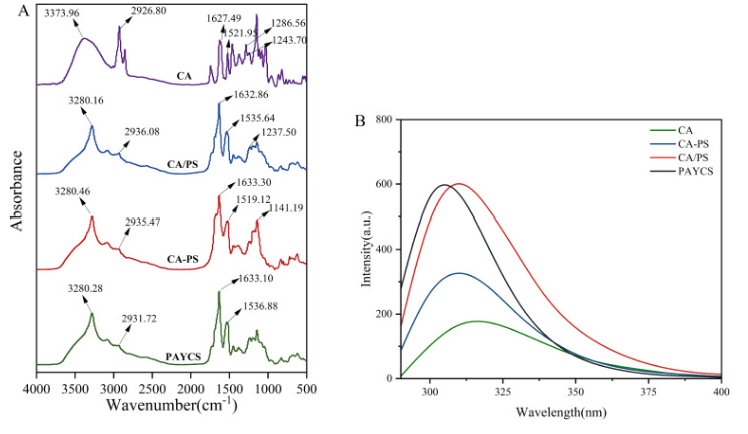
图 1. CA、PAYCS、CA/PS和CA-PS的FTIR及荧光光谱分析
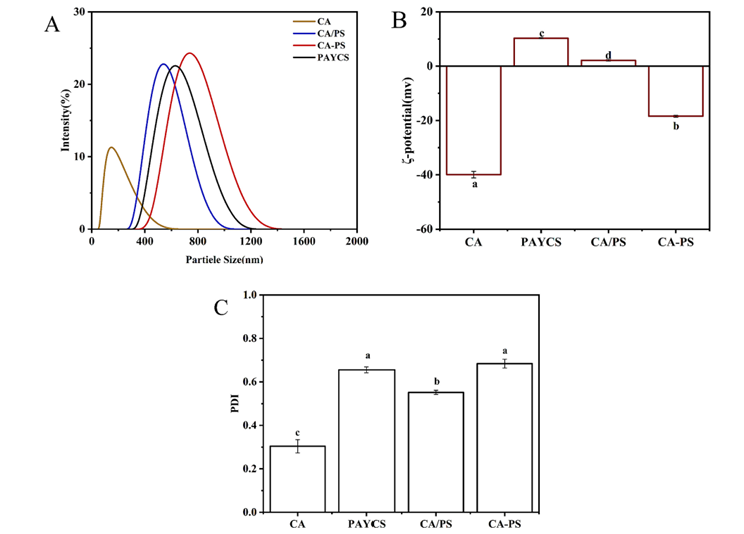

图 2. CA、PAYCS、CA/PS和CA-PS的粒径、 -电位及扫描电镜分析
在模拟胃肠道消化研究中,结果呈现出明显的差异:CA/PS在胃消化阶段表现出更好的抵抗能力,而CA-PS在肠道中稳定性更强。深入探究其机制发现,在模拟消化条件下,CA/PS复合物通过混合型胃蛋白酶抑制作用,在胃中保留了结构完整性;CA-PS则通过竞争性胰蛋白酶抑制作用,在肠道中维持了生物活性。
从抗氧化和AChE抑制活性来看,CA/PS在胃消化产物中的ABTS自由基清除活性显著高于CA-PS,而两者的肠道消化产物清除能力均有所提升。铁离子还原能力(FRAP)结果显示,消化后CA/PS和CA-PS的FRAP值分别达到1.38 0.06 mmol/gprot和1.66 0.06 mmol/gprot,均显著高于PAYCS消化产物,表明酚类化合物是复合物抗氧化活性的主要贡献者。AChE抑制活性方面,CA/PS消化产物在胃和肠道阶段的抑制率仍显著高于PAYCS,CA-PS在肠道阶段的抑制活性则显著高于CA/PS,进一步体现了不同结合方式对生物活性保留的差异。
在与消化酶的相互作用机制上,非共价和共价复合物对消化蛋白酶表现出不同的抑制模式和动力学特征。CA/PS对胃蛋白酶的抑制作用最强,且CA、PAYCS和CA/PS对胃蛋白酶呈现混合型抑制,CA-PS对胃蛋白酶的抑制也属于混合型;而CA-PS对胰蛋白酶的抑制效果最显著,CA/PS对胰蛋白酶表现为竞争性抑制,CA、PAYCS和CA-PS对胰蛋白酶呈现混合型抑制。光谱分析进一步揭示,复合物与消化酶的相互作用改变了酶的结构和微环境,从而影响酶的活性和结合亲和力。
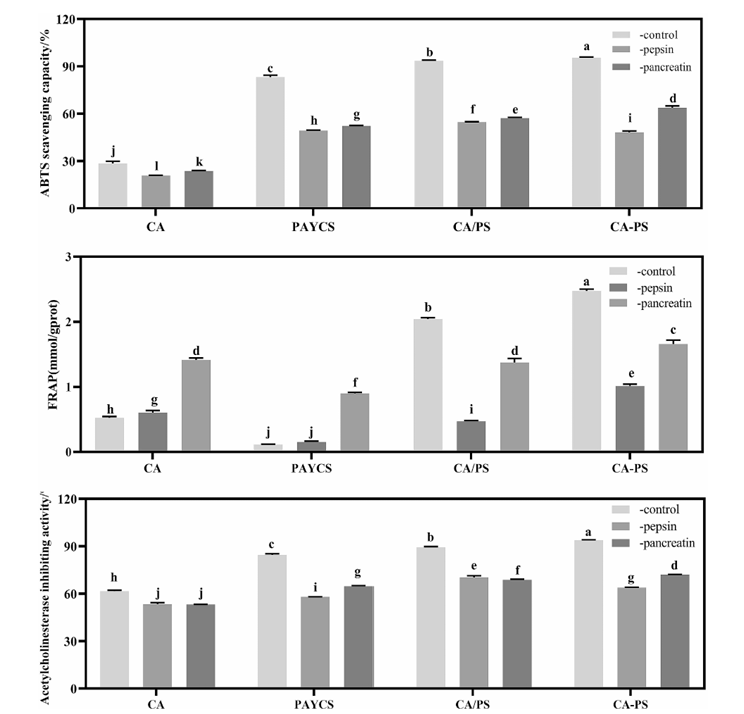
图 3. CA、PAYCS、CA/PS和CA-PS的胃肠道及非酶消化样品的抗氧化与AChE抑制活性
这项研究揭示了多酚与肽的相互作用能够调节肽的消化过程和功能活性。具体而言,CA通过非共价和共价相互作用改变了PAYCS的分子结构和消化特性:非共价复合物CA/PS通过抑制胃蛋白酶的蛋白水解活性,增强了对胃消化的抵抗能力,保留了肽-多酚结构;共价复合物CA-PS则在胰蛋白酶阶段表现出优异的稳定性并保留抗氧化活性,与其对胰蛋白酶的抑制作用一致。这些发现为设计具有理想理化性质的多酚结合肽提供了潜在的思路,有助于开发出更稳定、生物活性更持久的功能性食品,为改善记忆等健康问题提供了新的解决方案。随着对这一互作机制的深入理解,未来有望在功能食品领域实现更广泛的应用,为人们的健康带来更多益处。(100yiyao.com)
参考文献:
Chen J, Lin C, Yang L, et al. Influence of catechin-PAYCS interactions on gastrointestinal structural and bioactivity stability: Key mechanisms in digestive enzymes inhibition.Food Chem. Published online June 16, 2025. doi:10.1016/j.foodchem.2025.145132
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 《细胞·代谢》:华科大团队发现,慢性压力扰乱“肝-脑代谢轴”,促进小鼠的抑郁样行为! (2025-10-03)
- Science:生存的两种“投资学”——伪装是机会主义套利,警戒色是长期价值投资? (2025-10-03)
- Nature子刊:赵蔚团队发现,靶向相分离,治疗胶质母细胞瘤 (2025-10-03)
- 5年生存率不足10%,“癌王”难治的原因找到了!《自然》子刊发现它们有特殊入侵方式 (2025-10-02)
- Science:迄今最大规模人类蛋白互作图谱发布!系统鉴定了17849组高置信度蛋白互作,其中3631组为全新首次发现 (2025-10-02)
- Nat Neurosci: 激素调控月经周期中的全脑结构动态 (2025-10-02)
- Adv Sci:空军军医大学黄静等人研究阐明ACC依赖机制连接牙颌结构异常与慢性疼痛-情绪共病 (2025-10-02)
- 长寿可以遗传?《科学》研究发现某些优势或能传到第四代 (2025-10-02)
- Nat Commun:南方医科大学张先荣研究发现巨噬细胞双调蛋白诱导脓肿附近脂肪前体细胞肌成纤维细胞转变 (2025-10-02)
- Nature:新研究鉴定出蛋白LRP8是蜱传脑炎病毒入侵人类脑细胞的受体 (2025-10-02)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















