缺氧成肺发育“隐形推手”!Cell Stem Cell揭秘HIF-KLF通路调控肺细胞命运新机制 |
 |
来源:100医药网 2025-10-20 10:44
研究证实缺氧会推动人类肺祖细胞分化为气道细胞、抑制肺泡形成,HIF1α和HIF2α通过调控KLF4/KLF5实现这一过程,甚至能让成熟AT2细胞转变成气道样细胞。每次深呼吸时,我们享受着肺部高效的气体交换,却很少思考这套精密呼吸系统是如何在发育中一步步成型的。其实肺的生长特别依赖环境,胎儿在母体中时肺部处于低氧状态,忙着搭建气道的基础框架;出生后接触空气、氧气充足,负责气体交换的肺泡才开始慢慢成熟。这种氧环境的差异,会不会直接决定肺细胞的发展方向?
近日,Cell Stem Cell发表的一项研究Hypoxia promotes airway differentiation in the human lung epithelium就揭开了缺氧在人类肺上皮分化中的关键作用,还找到了背后的分子运作逻辑。
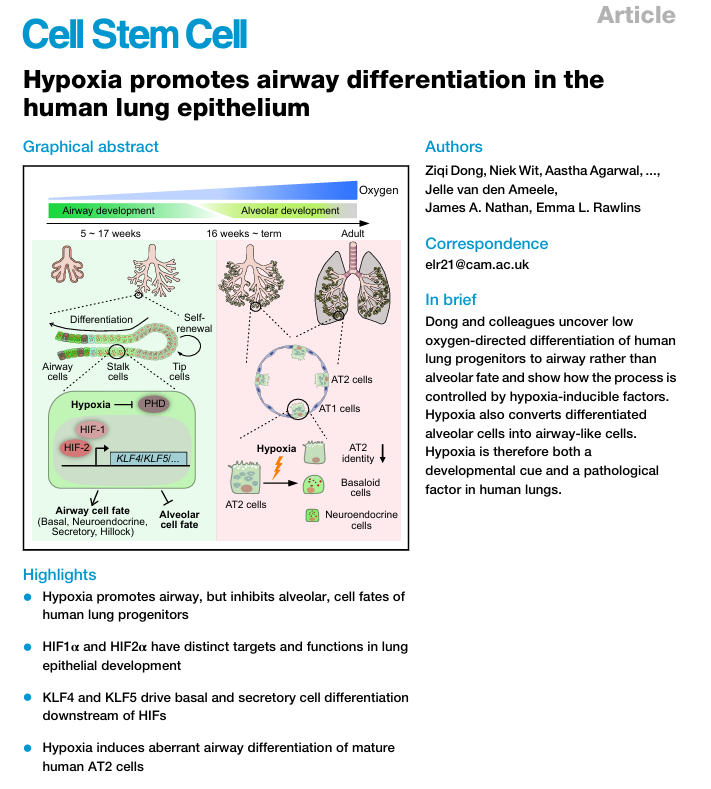
研究团队用组织来源的人类肺类器官做实验,发现孕早期(7-9周)的肺上皮祖细胞特别识环境 在常氧环境下,它们会稳稳维持身份,不轻易分化;可一旦处于2%的低氧环境,就像接到分化指令,主动变成基底细胞、分泌细胞、神经内分泌细胞等多种气道细胞,同时还会拒绝向肺泡细胞方向发展。更有意思的是,这种分化效果和氧浓度正相关,2%低氧的诱导作用比5%低氧更强,说明缺氧信号越明显,气道分化的动力就越足。就算用专门诱导肺泡形成的培养基,缺氧也能轻松干扰肺泡发育,这和体内气道形成阶段缺氧信号升高的特征完全吻合。
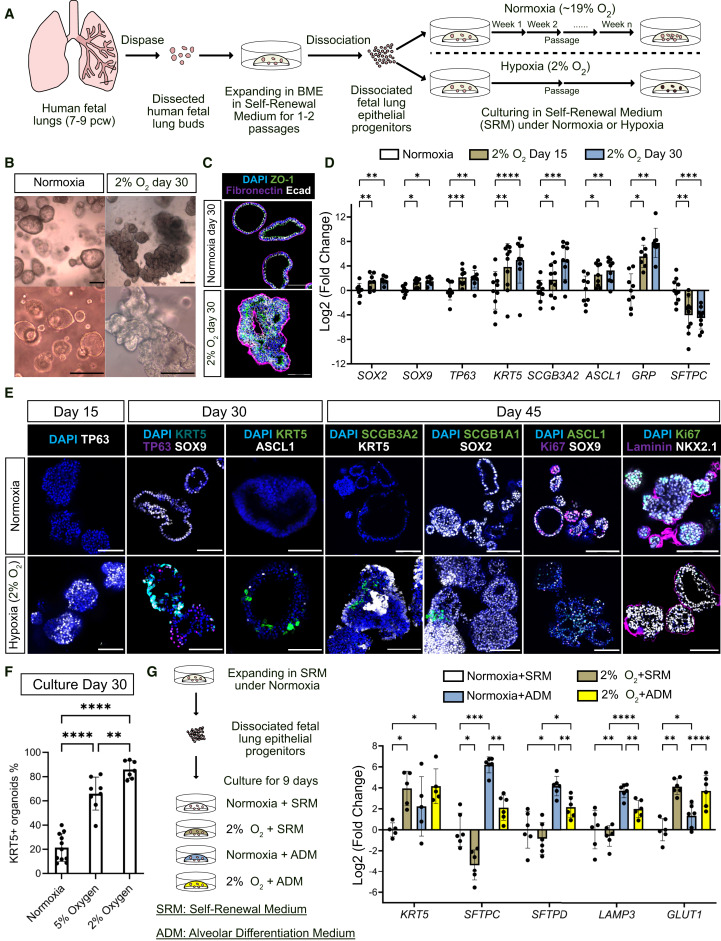
图1. 缺氧促进孕早期人类肺上皮祖细胞的气道分化
为了摸清缺氧背后的调控机制,研究团队用HRE-ODD-GFP报告系统追踪,发现缺氧会快速激活缺氧诱导因子通路(HIF)。更关键的是,用PHD抑制剂罗沙司他在常氧下稳定HIF ,居然能模拟缺氧的效果,让祖细胞乖乖向气道细胞分化。通过靶向DamID-seq分析,团队还发现HIF家族里的HIF1 和HIF2 虽有4210个共同靶基因,却各有专属分工 HIF1 更倾向调控WNT信号相关基因,HIF2 则重点关注SCGB3A2这类气道分泌细胞的标志物基因。功能实验进一步证实,HIF1 是气道分化的必需品,少了它,气道标志物的表达会大幅下降;而HIF2 更像偏向型调控者,主要推动基底细胞形成,同时抑制分泌细胞、神经内分泌细胞和肺泡细胞的发育。
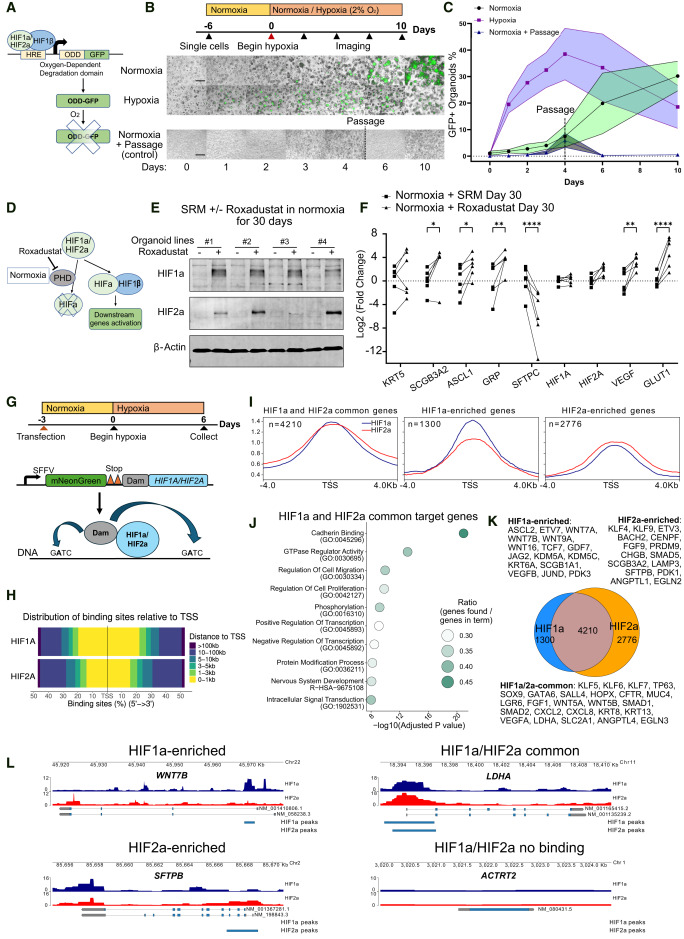
图2. 缺氧肺类器官中HIF通路被激活
顺着HIF的调控链往下找,研究团队还发现了两个关键执行分子 KLF4和KLF5。它们都是HIF的直接靶基因,KLF4主要受HIF2 调控,KLF5则是HIF1 和HIF2 的共同目标,两者都能推动基底细胞和分泌细胞的形成,但对肺泡细胞命运的影响存在差异。就算用化学方法诱导气道分化,敲掉KLF4或KLF5,气道细胞的形成也会变弱,这说明缺氧信号和化学信号,可能都靠这两个执行分子来推动气道发育。
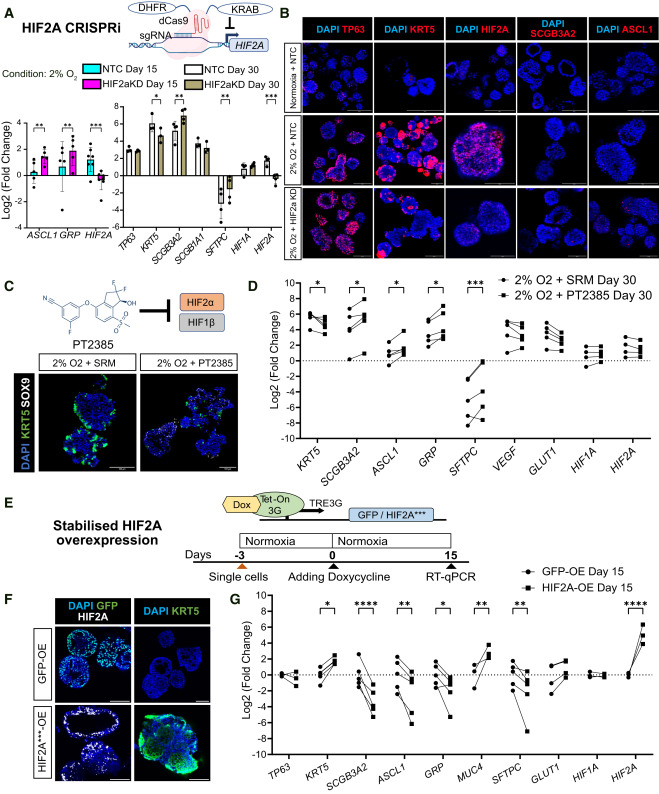
图3. HIF2 促进基底细胞命运,但抑制分泌细胞、神经内分泌细胞和肺泡细胞命运
更让人意外的是,缺氧不仅能调控未成熟的祖细胞,还能改写成熟肺泡细胞的身份。不管是胎儿还是成人来源的AT2细胞,放到缺氧环境里,都会慢慢丢掉肺泡细胞的身份标识,逐渐长出气道细胞的特征,甚至会变成在肺纤维化中常见的异常基底样细胞。虽然把它们放回常氧环境后,部分肺泡特征能恢复,但那些异常的基底样细胞却会留存下来。而用HIF2 抑制剂处理,能部分逆转AT2细胞的这种身份转变,这说明HIF2 在这个过程中起了主要作用。
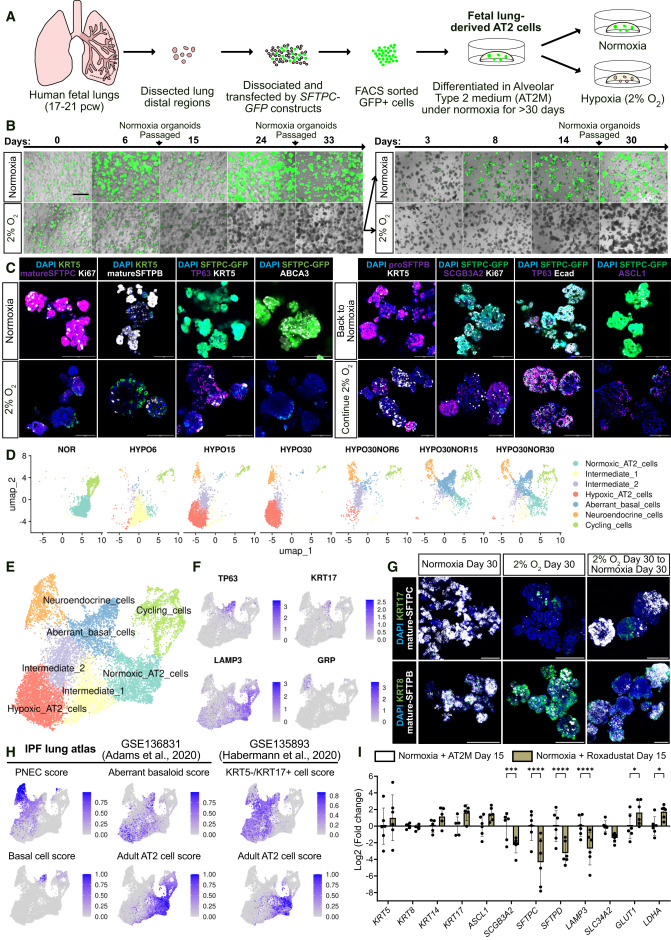
图4. 慢性缺氧将人类AT2细胞转化为气道细胞
这项研究清晰展现了缺氧在人类肺上皮发育中的双重角色 既是引导正常发育的信号,也是可能引发病理变化的因素,还明确了HIF1 /HIF2 -KLF4/KLF5这条核心调控链。它不仅解答了肺发育中的关键科学问题,还为理解肺纤维化这类缺氧相关肺病的发病机制提供了新线索 或许这些疾病中的细胞异常,正是缺氧打乱了细胞身份导致的。未来如果能调控HIF通路,说不定就能帮肺部纠正异常的细胞命运,为肺发育异常和肺纤维化等疾病的治疗开辟新方向。(100yiyao.com)
参考文献:
Dong Z, Wit N, Agarwal A, et al. Hypoxia promotes airway differentiation in the human lung epithelium.Cell Stem Cell. Published online October 10, 2025. doi:10.1016/j.stem.2025.09.007IF: 20.4Q1
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 中国微生态产业获国际认可!万泽医药入选沙利文白皮书 (2025-10-20)
- 聚焦医保惠平易近 重庆启动根本医顾全平易近参保集中鼓吹月 (2025-10-20)
- 海南自贸港封关临近 生物医药食物加工家当集聚倒退 (2025-10-20)
- 投资10亿欧元 赛诺菲北京胰岛素质料药临盆基地名目启动 (2025-10-20)
- 缺氧成肺发育“隐形推手”!Cell Stem Cell揭秘HIF-KLF通路调控肺细胞命运新机制 (2025-10-20)
- Nature Medicine:当生命走向终点——颠覆性的发现重新定义死亡的边界 (2025-10-20)
- 健康赋能每一步,扬子江龙凤堂2025泰州马拉松赛鸣枪开跑 (2025-10-20)
- 槲皮素哪个品牌好?肺结节人群看过来!2005槲皮素品牌排行榜,吉清肺改善率超93% (2025-10-20)
- 清肺润肺哪个牌子好?2025槲皮素十大护肺品牌推荐,吉清肺GRANVER针对不同人群显成效? (2025-10-20)
- Nature Medicine:这个基因突变,会导致肥胖,但能抵御心脏病 (2025-10-19)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















