Science:揭示噬菌体PP7削弱铜绿假单胞菌毒力的新机制 |
 |
来源:100医药网 2024-04-24 11:46
铜绿假单胞菌(Pseudomonas aeruginosa)是一种可引起血液、肺部感染的细菌,偶尔也会引起身体其他部位的感染。细菌感染给农业和医学带来了巨大挑战,尤其是耐药细菌的病例不断增加。对此,来自美国德克萨斯农工大学的研究人员在一项新的研究中揭示了称为噬菌体的细菌病毒使细菌失效的精确机制,从而为新型治疗方法的出现提供可能。相关研究结果发表在2024年4月5日的Science期刊上,论文标题为 Removal of Pseudomonas type IV pili by a small RNA virus 。 论文通讯作者为德克萨斯农工大学的Lanying Zeng博士和Junjie Zhang博士。

需要新的治疗方法
铜绿假单胞菌(Pseudomonas aeruginosa)是一种可引起血液、肺部感染的细菌,偶尔也会引起身体其他部位的感染。这些感染在医疗机构中尤其常见,因为医疗机构经常会遇到耐药细菌。根据美国疾病控制预防中心(CDC)的数据,2017 年住院患者中出现了 3 万多例多重耐药铜绿假单胞菌感染病例。
耐抗生素假单胞菌感染的普遍性使其成为噬菌体疗法的实际关注点。噬菌体疗法是一种使用噬菌体(bacteriophage)的治疗方法,德克萨斯农工大学噬菌体技术中心的研究人员正在探索将它作为典型药物的替代物。他们正在通过深入研究噬菌体的结构和作用机制,探索噬菌体在噬菌体疗法以外的用途。
靶向菌毛
铜绿假单胞菌之所以能相互传播抗菌基因、四处游动并形成难以治疗的生物膜(biofilm)结构,其中一个因素是一种名为菌毛(pilus)的附属物。这种圆柱形结构从细菌表面伸出。一些噬菌体利用细菌的菌毛,附着在菌毛上,让细菌把噬菌体卷到细菌表面上,然后噬菌体开始感染细菌。
在由德克萨斯农工大学研究生 Jirapat Thongchol 和 Zihao Yu 共同撰写的研究报告中,这些作者利用荧光显微镜、低温电镜和计算模型对这一过程进行了逐步研究。他们观察到一种名为 PP7 的噬菌体如何通过附着在菌毛上感染铜绿假单胞菌,然后菌毛缩回并将噬菌体拉到细菌细胞表面。在噬菌体的进入点,菌毛弯曲并折断,菌毛的失去使得铜绿假单胞菌感染宿主的能力大大降低。
正在进行的研究
这项新的研究是 2020 年发表的研究成果(PNAS, 2020, doi:10.1073/pnas.2011901117)的延续,当时Zeng的团队发现了一种噬菌体,它同样可以切断大肠杆菌细胞的菌毛,防止细菌之间共享基因,这是抗生素耐药性传播的常见方式。
这项对假单胞菌的新研究是Zeng团队近期一系列研究的一部分。2024年3月,他们在Nature Communications期刊上发表了关于另一种细菌 不动杆菌(Acinetobacter),与感染它的噬菌体之间相互作用的研究结果(Nature Communications, 2024, doi:10.1038/s41467-024-47119-5)。另一项研究预计将于 2024 年 5 月发表,涉及第三种细菌属和其他噬菌体。
Zeng团队在确定精确的蛋白结构和分子相互作用方面取得的进展得益于德克萨斯农工大学农业与生命科学学院的新型低温电镜,该低温电镜于2022年底在德克萨斯农工大学启用,可以解析原子级别的结构。
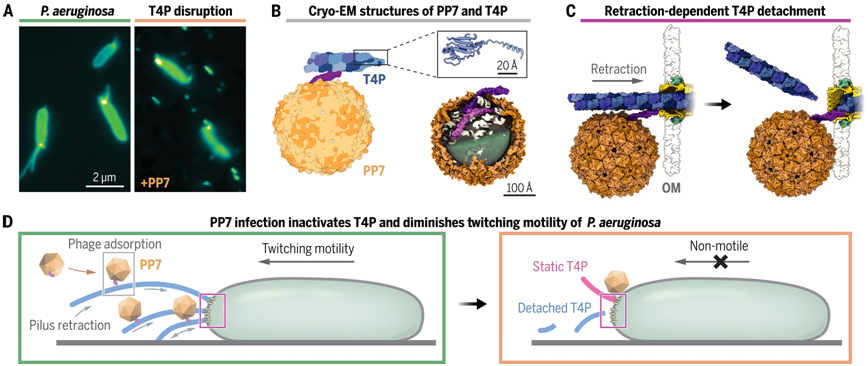
噬菌体PP7感染会损害铜绿假单胞菌的移动能力。图片来自Science, 2024, doi:10.1126/science.adl0635
Zeng 说, 在我们早期对大肠杆菌的研究中,我们并没有真正深入探讨其机制。在对假单胞菌的研究中,我们能够解释更多究竟发生了什么,包括菌毛脱落的力量和速度,并理解这种情况发生的原因和方式。
医学用途
这项正在进行的研究可能会对治疗抗菌感染产生重要影响。Zhang说,医生不需要像噬菌体疗法那样使用噬菌体杀死细菌,而只需让噬菌体解除细菌的武装,这可能会让系统有机会自行对抗感染,或让医生用较低剂量的抗生素治疗患者。
Zhang说, 如果只是简单地杀死细菌,就会破坏细菌细胞,细菌细胞内的有毒物质就会释放到宿主体内。我们的方法是使用一种特殊的噬菌体来解除细菌的武装。我们通过切断这种附属物来消除它们交换抗药性基因或四处移动的能力。
Zhang团队表示,他们将继续寻找噬菌体抑制病原菌毒力的类似实例。Zhang说, 我们正在采取一种协同方法。我们正试图了解这种类型噬菌体的通用机制,以及它们如何能够影响其他类型的细菌。这就是我们合作的总体目标:努力解决多重耐药细菌的问题。 ( 100yiyao.com)
参考资料:
Jirapat Thongchol et al. . Science, 2024, doi:10.1126/science.adl0635.
Researchers Solve Mystery Of How Phages Disarm Bacteria
https://today.tamu.edu/2024/04/17/researchers-solve-mystery-of-how-phages-disarm-bacteria/
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 皖医二附院成功救治一名重症急性胰腺炎合并极危高甘油三酯血症患者 (2025-07-12)
- 默沙东百亿美元收购打开BD新风口,中国药企机会来了 (2025-07-12)
- 中国农业科学院发表最新Nature论文 (2025-07-12)
- 中国科学技术大学最新Cell论文,登上Nature头条,首次实现小鼠全身神经系统微米级高清成像 (2025-07-12)
- 民泰医药全面升级:2025年搬迁新址,打造中药智能化生产新标杆 (2025-07-11)
- 第一次为爱鼓掌要做好准备!快男备好爱廷玖盐酸达泊西汀 (2025-07-11)
- 《Science》刊发上海六院与复旦大学脑科学转化研究院联合成果:揭示造血干细胞移植治疗致死性遗传性脑白质病的有效性及其核心机制 (2025-07-11)
- 青海首批外乡产3D打印医疗东西获批上市 (2025-07-11)
- 全国药品运营监管任务会暨“清源”行为推动会召开 (2025-07-11)
- 软骨发育不全等86个常见病病种诊疗指南宣布 (2025-07-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















