T细胞淋巴瘤新药!强效法尼基转移酶抑制剂tipifarnib获美国FDA快速通道资格,总缓解率达70% |
 |

2020年3月5日讯 /BIOON/ --Kura Oncology是一家临床阶段的生物制药公司,专注于学精准药物的开发。近日,该公司宣布,美国食品和药物管理局(FDA)已授予其先导候选药物tipifarnib快速通道资格(FTD),用于治疗成人复发或难治性血管免疫母细胞性T细胞淋巴瘤(AITL)、滤泡性T细胞淋巴瘤(FTCL)、淋巴结外周T细胞淋巴瘤(TFH)。2019年12月,还授予了tipifarnib一个FTD,用于治疗接受含铂化疗后病情进展、携带HRAS突变的头颈部鳞状细胞癌(HNSCC)患者。
快速通道资格(FTD)旨在加速针对严重疾病的药物开发和快速审查,以解决关键领域严重未获满足的医疗需求。实验性药物获得快速通道资格,意味着药企在研发阶段可以与进行更频繁的互动,在提交上市申请后如果符合相关标准则有资格进行加速审批和优先审查,此外也有资格进行滚动审查。
tipifarnib是一种强效、高度选择性法尼基转移酶抑制剂,于2014年12月从杨森获得许可。法尼基化是一个关键的细胞信号传导过程,与癌症的发生和发展有关。目前,tipifarnib处于临床开发,用于多种实体肿瘤和血液学适应症的治疗。此前,该药已在超过5000例癌症患者中进行了研究,在特定患者亚组中表现出了令人信服和持久的抗癌活性,包括携带突变HRAS的鳞状肿瘤以及不携带突变HRAS的淋巴、骨髓和实体。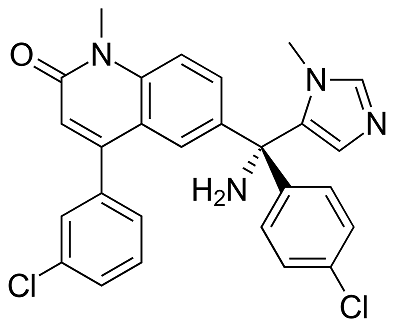
tipifarnib分子结构式(图片来源:Wikipedia)
2019年12月,Kura公司在美国血液学会年会(ASH 2019)上报告了最新的临床数据,显示tipifarnib作为单药疗法治疗复发或难治性AITL具有强大和持久的活性。数据显示,在先前已接受疗法中位数为3种的一个重度预治疗患者群体中,客观缓解率(ORR)约为50%。此外,在携带杀伤细胞免疫球蛋白样受体(KIR,一种CXCL途径相关的生物标记物)突变的患者中,发现tipifarnib的抗活性增强,这些患者中的ORR为70%,完全缓解率(CR)为40%。
2019年10月底,Kura公司公布了tipifarnib治疗HRAS突变头颈部鳞状细胞癌(HNSCC)II期RUN-HN试验的更新数据。结果显示:在先前接受过多种疗法(中位数:2种,范围:0-6)但病情进展的HRAS突变HNSCC患者中,tipifarnib作为单药疗法显示出强效、持久的抗活性:总缓解率(ORR)为56%,中位无进展生存期(PFS)为6.1个月。而目前,已被批准二线治疗HNSCC的三种疗法——Keytruda、Opdivo、Erbitux的总缓解率(ORR)范围在13-16%,PFS约为2个月。
Kura公司首席医疗官Bridget Martell医学博士表示:“继授予治疗HRAS突变HNSCC的快速通道资格2个月后,又授予了tipifarnib治疗T细胞淋巴瘤的快速通道资格,这些资格认定反映了tipifarnib在治疗这些毁灭性疾病中的巨大潜力,我们现在正积极准备在TFH表型的晚期淋巴结淋巴瘤(包括AITL)中启动tipifarnib的第二项注册指导试验。”(100医药网100yiyao.com)
原文出处:
医药网新闻
- 相关报道
-
- 十大护肝片品牌测评分析,排名top的护肝官方旗舰店,科学守护肝脏健康 (2025-08-14)
- 张锋最新论文:把“细菌注射器”升级改造为递药系统,实现多种生物分子的靶向递送 (2025-08-14)
- 共筑抗体发现新高地!强强联手,自主可控!追光生物与华大智造达成战略合作 (2025-08-14)
- 极限赛事的 "隐形铠甲":北京和睦家多学科协同为1.5万名斯巴达勇士护航 (2025-08-14)
- 《自然·神经科学》:重启病变运动神经元!哥大学者发现,再表达ISL1和LHX3,可以减轻渐冻症表型 (2025-08-14)
- Cell子刊:我国学者研究证实,微塑料/纳米塑料已全面侵入珠峰生态系统的各个部分 (2025-08-14)
- 首届中国-东盟药膳博览会新闻发布会在京隆重召开 (2025-08-13)
- 师恩入海,核美丽助您社交无痕 (2025-08-13)
- 申报:脑机接口技术向理论利用畛域迈进的过程显著提速 (2025-08-13)
- 解读:通过初步模式审查的药品及相关信息的布告 (2025-08-13)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















