PNAS:揭示杀虫真菌调控附着胞膨压产生机制 |
 |
中国科学院分子植物科学卓越创新中心王四宝研究组在《美国国家科学院院刊》(PNAS)上,在线发表了题为The ASH1-PEX16 regulatory pathway controls peroxisome biogenesis for appressorium-mediated insect infection by a fungal pathogen的研究论文。该研究发现并阐明了杀虫真菌组蛋白修饰介导的调控通路ASH1-PEX16通过控制附着胞中过氧化物酶体的生成来协作调控脂滴降解产生膨压的机制。
病原真菌是昆虫病原微生物中的最大类群,是自然界昆虫种群消长的重要调节因子,已被开发为环境友好的微生物杀虫剂,用于防治多种农林和卫生害虫。杀虫真菌是唯一一类可通过接触昆虫体表直接侵染并致死昆虫的病原微生物,在对刺吸式口器害虫的防治上具有独特优势。许多病原真菌的孢子在昆虫体表萌发后,芽管顶端膨大并分化形成一种高度特化的侵染结构 附着胞(appressorium),分生孢子中的脂滴随后迁移到附着胞中,通过脂解生成甘油,甘油累积产生巨大的膨压,为附着胞基部产生的侵染钉(penetration peg)穿透昆虫体壁提供不可或缺的机械力。因此,附着胞膨压的产生对真菌穿透体表侵染昆虫至关重要。尽管目前已基本了解病原真菌的入侵方式,但对附着胞介导的侵染机制,特别是其产生巨大膨压的调控机制尚不清楚。
该研究基于前期开展的真菌与蚊虫互作过程中的基因表达谱分析(Lai et al., 2017. Science China Life Sciences),鉴定到一个在绿僵菌早期侵染蚊虫体壁时特异上调表达的基因Mrash1(与果蝇ash1,即discs absent, small or homeotic-1基因同源)。研究发现,敲除Mrash1导致真菌穿透昆虫体壁能力显著下降,进一步发现这一表型缺陷是附着胞内脂滴降解受阻、甘油产量下降、从而无法产生足够膨压引起的。和Western blot分析发现,Mrash1编码一个组蛋白赖氨酸甲基转移酶,负责催化组蛋白H3K36me2修饰。RNA-seq和ChIP-seq联合分析发现,MrASH1通过催化H3K36me2修饰激活过氧化物酶体相关蛋白基因Mrpex16的转录表达。敲除Mrpex16导致真菌产生与Mrash1突变体相似的表型,即对昆虫体壁穿透能力下降、附着胞内脂滴降解受阻、甘油产量及膨压下降,致病力显著减弱。附着胞脂滴降解产生甘油的同时也产生脂肪酸,脂肪酸需及时分解代谢以避免脂肪酸积累对细胞造成的脂毒性和对脂滴降解的抑制。过氧化物酶体是脂肪酸b-氧化的重要场所。通过建立过氧化物酶体荧光蛋白示踪方法,研究发现敲除Mrpex16或Mrash1均阻碍过氧化物酶体的生成,抑制真菌在脂肪酸培养基上生长,使得脂肪酸分解代谢受阻,进而反馈抑制脂滴降解,导致甘油产量减少、附着胞膨压降低,进而降低真菌穿透体壁和致病的能力;而在Mrash1突变体中过表达Mrpex16可以恢复过氧化物酶体的生成,表明MrASH1通过激活Mrpex16来调控过氧化物酶体的生成。
综上,ASH1通过H3K36me2修饰激活pex16基因的转录表达,调控附着胞中过氧化物酶体的生成,通过脂肪酸的氧化分解代谢促进脂滴降解,产生的甘油累积形成膨压,最终帮助病原真菌穿透体壁侵染寄主昆虫(如图),揭示了ASH1-PEX16通过调控过氧化物酶体的生成来协作调控脂滴降解和附着胞膨压产生的新途径。该研究发现了组蛋白修饰在过氧化物酶体生成中的调控作用,阐释了过氧化物酶体-脂滴协作调控脂滴降解和膨压形成的机制。这为病原真菌附着胞介导的侵染机制提供了新见解,为增强生防真菌的杀虫效力提供了新的思路和潜在靶标。
这一成果是王四宝研究组继发现生防真菌侵染结构附着胞分化形成的表观遗传机制(Lai et al., 2020. Science Advances)后,再次在昆虫病原真菌附着胞介导的体壁侵染机制领域取得的重要进展。研究工作得到国家重点研发计划重点专项、国家、中科院战略性先导科技专项培育项目、中科院青年创新促进会、上海市等的支持。营养与健康所科研人员参与研究。
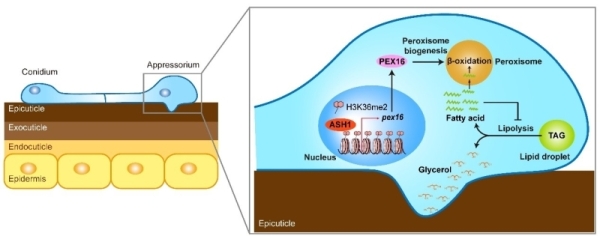
杀虫真菌通过组蛋白修饰介导的调控通路ASH1-PEX16控制附着胞过氧化物酶体的生成来协作调控脂滴降解产生膨压的分子机制
医药网新闻
- 相关报道
-
- 上海药物所×临港实验室合作发表Cell论文:基于结构发现新型抗抑郁小分子 (2025-10-26)
- Mol Cancer:阻断甲状腺激素受体为前列腺癌治疗提供了新的途径 (2025-10-26)
- Science子刊:卞修武团队发现增强CAR-T细胞抗肿瘤效果的基因修饰策略 (2025-10-26)
- Nature Biotechnology:直击囊胚“混沌期”——长时程活体成像首次捕捉人类囊胚的染色体分离灾难 (2025-10-26)
- JNCCN:戒烟也应当是癌症治疗的一环!13万名癌症患者数据分析结果显示,癌症确诊后及时戒烟可大幅降低死亡风险,改善手术预后 (2025-10-26)
- NEJM:人工视网膜,帮助老年性黄斑变性患者恢复视力 (2025-10-25)
- 华中师范大学最新Cell子刊论文:开发治疗白血病的多肽类药物 (2025-10-25)
- 《科学》:膳食脂肪重塑昼夜节律!加州大学科学家发现,饮食中不饱和脂肪酸比例会影响昼夜节律,是人体生物钟与季节匹配与否的关键 (2025-10-25)
- 河南中州实验室发表Nature Metabolism论文:揭开大脑髓鞘再生修复的关键 (2025-10-25)
- Nature Medicine:为疲惫的心脏“重启引擎”——基因疗法AB-1002能否逆转心力衰竭的宿命? (2025-10-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















