MN:阿尔茨海默病候选药物BACE1抑制剂为何败走?科学家找到了它促进认知衰退的机制! |
 |
来源:奇点糕 2023-03-22 10:35
这项研究首次清晰地证明了BACE1可以切割gp130产生sgp130,抑制BACE1的活性会导致BACE1对神经元上gp130的裂解减少,增加神经元上gp130的含量并减少大脑中sgp130的含量,这(AD)是导致痴呆的重要因素,随着人口老龄化的不断加重,AD已经成为近在眼前的危机。
经典理论认为A 沉积是AD的病理原因之一,因此针对性地开发了多款药物。 分泌酶BACE1是将淀粉样前体蛋白(APP)转变为A 的催化酶之一,抑制BACE1的活性能够减少A 蛋白的产生。
已有多款BACE1抑制剂进入临床试验,它们可以有效地抑制BACE1的活性,并减少大脑以及脑脊液中的A 蛋白,但是由于存在包括非进展性认知衰退在内的副作用[1-3],多数药物止步于2/3期临床试验。目前还不清楚为何BACE1抑制剂会引起患者认知衰退。
近期,由德国神经退行性疾病中心的Stefan F. Lichtenthaler领衔的研究团队,在Molecular Neurodegeneration上发表最新研究成果[4],揭示了BACE1不为人知的新功能。
他们发现,在非人类灵长类动物以及人类中,BACE1可以切割IL-6受体 亚基(gp130),从而影响神经元中IL-6的信号转导。由于可溶性gp130(sgp130)在健康状态下可以作为一种缓冲体系,防止过度的IL-6信号对神经元造成不利影响,因此长期抑制BACE1使得接受治疗的个体对IL-6信号的不利影响更为敏感。

论文首页截图
由于不同分子结构的BACE1抑制剂均可以引起认知衰退,并且这些药物对中枢神经系统BACE1的活性抑制可以达到75%以上,Lichtenthaler团队猜测这可能是由于过强地抑制了BACE1对某一个或某几个底物的裂解,从而引起神经系统的副作用。
为了寻找可能被BACE1裂解的蛋白,他们收集了3只猕猴在口服BACE1抑制剂MBI-4前后的脑脊液样品,利用质谱寻找差异蛋白质。他们发现服用BACE1抑制剂后,脑脊液中SEZ6、IL6ST(gp130)、VCAM1胞外结构域的丰度以剂量依赖的方式显著降低。其中,SEZ6是已知的BACE1底物;IL6ST是细胞因子受体gp130,已有的研究认为它可能是BACE1底物[5,6]。
为了进一步确认上述的发现,他们又进行了一次独立实验,给猕猴服用正在进行临床试验的BACE1抑制剂verubecestat,检测其脑脊液中含量变化的蛋白质。结果显示,服用verubecestat后,脑脊液中的SEZ6、CACHD1、LRRN1、L1CAM和sgp130表现出剂量依赖性的减少。
以上两次实验均表明,抑制BACE1的活性能够减少sgp130,提示gp130是一种潜在的BACE1底物。
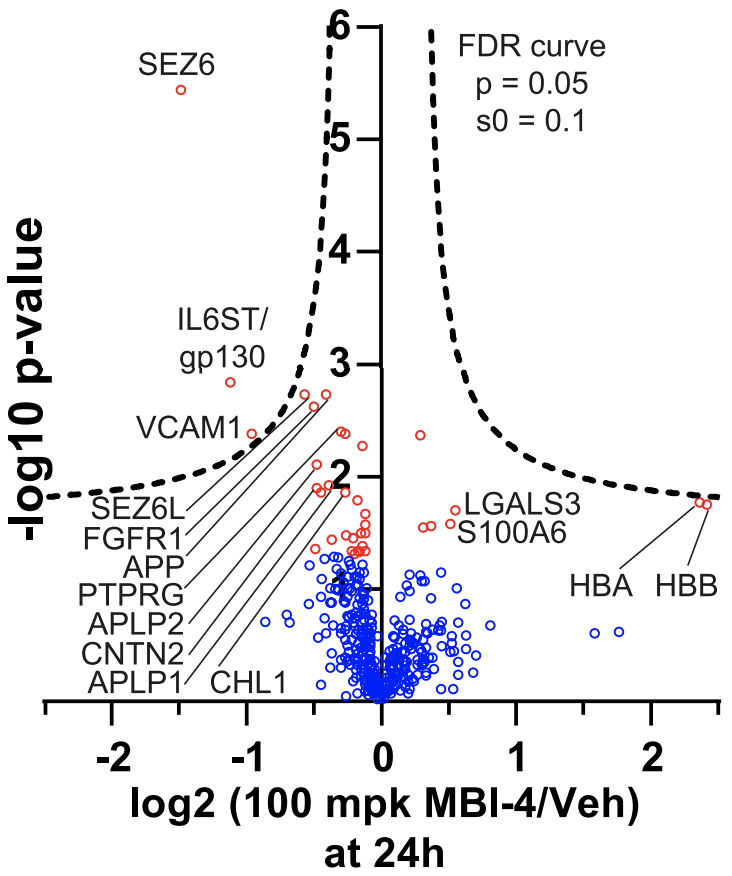
gp130可能是BACE1的底物
为了探究上述现象在人类中是否也存在,Lichtenthaler团队收集了健康年轻人服用BACE1抑制剂verubecestat前后的脑脊液样品,通过WB以及ELISA检测脑脊液中的SEZ6以及sgp130的含量。
结果显示,服用verubecestat后,人类脑脊液中SEZ6以及sgp130的含量显著减少。这些数据提示,SEZ6和sgp130可以作为BACE1的药效学活性标记物。
既然来自非人灵长类以及人类志愿者的数据均表明gp130可能是BACE1的底物,那么接下来就是要证实BACE1是否真能够切割gp130。通过体外实验,Lichtenthaler团队直接地证实BACE1确实能够切割膜结合型gp130产生sgp130。
基于小鼠原代神经元的实验也表明,在活体神经元中BACE1确实可以切割gp130产生sgp130。
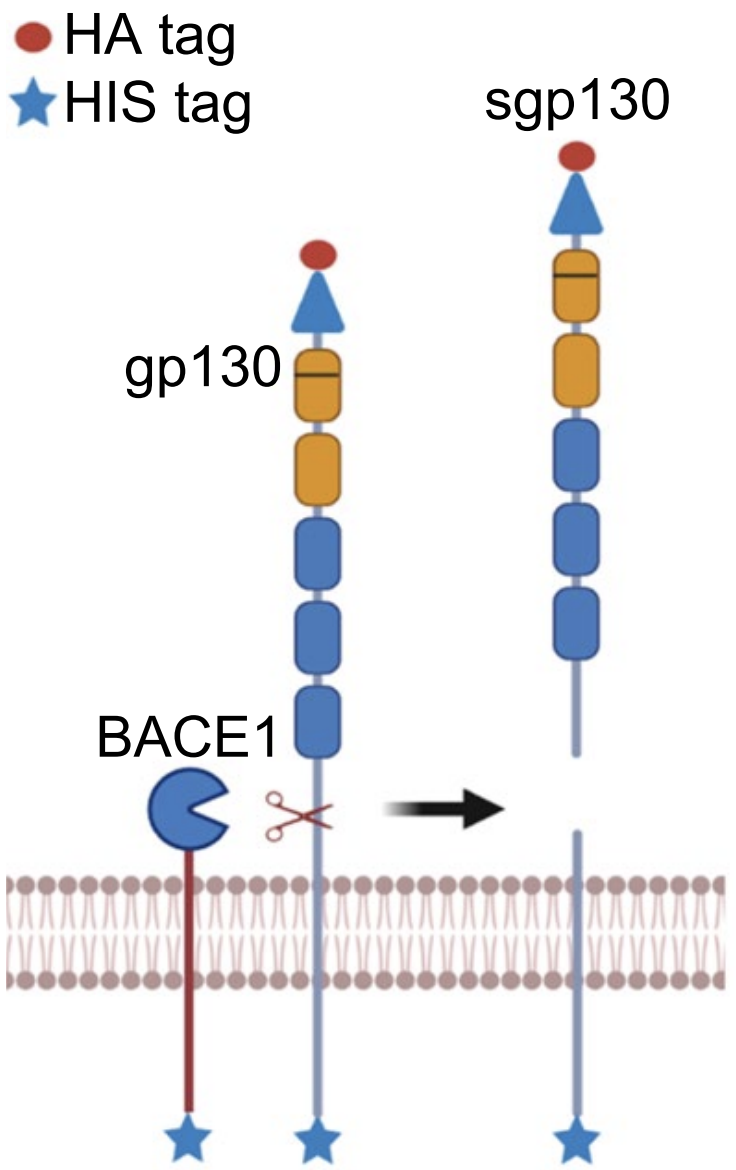
BACE1对gp130的体外切割作用
由于gp130介导IL-6的下游信号转导,且sgp130能够抑制IL-6的反式信号,因此Lichtenthaler团队想知道抑制BACE1的活性,是否会通过影响sgp130的丰度,从而影响神经元对IL-6的应答。
为此,他们使用小鼠原代神经元进行实验,使用IL-6和IL6R复合物(H-IL-6)刺激神经元,通过添加C3来抑制BACE1的活性。结果显示,抑制BACE1后,IL-6下游的STAT3磷酸化水平显著升高。
这可能是因为抑制BACE1活性后,细胞膜上的gp130增加,因此增强了IL-6的下游信号转导。如果将H-IL-6与sgp130共孵育一段时间再添加至培养基中,神经元中STAT3的磷酸化水平会显著降低,这表明sgp130可以与膜结合型gp130竞争性结合H-IL-6,从而阻碍神经元响应IL-6刺激。
医药网新闻
- 相关报道
-
- 为什么有人喝凉水都长肉?50 万人基因研究揭密:249 种代谢物背后,这些基因是“隐形操控者” (2025-10-20)
- 中国微生态产业获国际认可!万泽医药入选沙利文白皮书 (2025-10-20)
- 聚焦医保惠平易近 重庆启动根本医顾全平易近参保集中鼓吹月 (2025-10-20)
- 海南自贸港封关临近 生物医药食物加工家当集聚倒退 (2025-10-20)
- 投资10亿欧元 赛诺菲北京胰岛素质料药临盆基地名目启动 (2025-10-20)
- 缺氧成肺发育“隐形推手”!Cell Stem Cell揭秘HIF-KLF通路调控肺细胞命运新机制 (2025-10-20)
- Nature Medicine:当生命走向终点——颠覆性的发现重新定义死亡的边界 (2025-10-20)
- 健康赋能每一步,扬子江龙凤堂2025泰州马拉松赛鸣枪开跑 (2025-10-20)
- 槲皮素哪个品牌好?肺结节人群看过来!2005槲皮素品牌排行榜,吉清肺改善率超93% (2025-10-20)
- 清肺润肺哪个牌子好?2025槲皮素十大护肺品牌推荐,吉清肺GRANVER针对不同人群显成效? (2025-10-20)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















