《科学·进展》:STK11突变的肺癌,有救了! |
 |
来源:奇点糕 2023-04-25 07:49
本次研究的发现表明,在NSCLC基因工程小鼠模型中,同时使用MEK抑制剂曲美替尼和HDAC3抑制剂entinostat可以有效抑制肿瘤进展。先前已有诸多研究表明,在黑色素瘤和胰腺癌患者中,HDAC抑制靶向治疗凭借着 肿瘤细胞针对性强+低副作用 的特点,已逐渐成为目前癌症治疗领域冉冉升起的一颗新星[1]。然而,靶向治疗并非对所有肿瘤都有奇效,例如具有LKB1基因突变(又称STK11突变)的非小细胞()。
NSCLC是最常见的肺癌类型,其中约有20%-30%的患者带有LKB1突变,这部分患者对标准化疗与+化疗方案的应答均不理想,既往也没有直接针对LKB1突变的酪氨酸激酶抑制剂(TKIs)类靶向药物。
传统TKIs做不到的事,不代表表观遗传类靶向药做不到,例如组蛋白去乙酰化酶(HDAC)抑制剂,目前已有多种HDAC抑制剂被美国批准,用于治疗血液系统恶性肿瘤[2-3]。那么HDAC抑制剂是否可以用于LKB1突变型NSCLC的治疗呢?
近日,由索尔克研究所教授Reuben Shaw和前博士后Lillian Eichner(现为美国西北大学助理教授)领导的研究团队在Science Advances期刊发表了最新研究成果[4]。研究发现,HDAC家族中的HDAC3是LKB1突变型NSCLC生长所必需的,先前未被发现的HDAC3靶基因 FGFR1,还介导了此类肿瘤对MEK抑制剂曲美替尼的耐药。
基于上述发现,Reuben等人提出了针对LKB1突变型NSCLC的靶向联合治疗新策略:HDAC3抑制剂entinostat联合MEK抑制剂曲美替尼,二者联合用药在动物实验中有效抑制了NSCLC的肿瘤进展。

论文首页截图
尽管HDAC3抑制剂作为治疗药物取得了很大的临床进展,但HDAC3在肿瘤发生中的潜在作用在很大程度上仍然是未知的,因为之前的许多研究都着眼于其在代谢组织中的功能和作用机制。
鉴于此,Reuben等人首先利用KRAS突变基因工程小鼠模型探索了HDAC3在NSCLC肿瘤发生中的作用。研究者们发现,不论是在KRAS突变合并LKB1缺失(KL),还是KRAS突变合并p53缺失(KP)的NSCLC小鼠中,与同窝对照组相比,HDAC3敲除小鼠的肿瘤生长在早期和晚期均明显被抑制,其肿瘤数量明显减少,肿瘤大小明显减小。
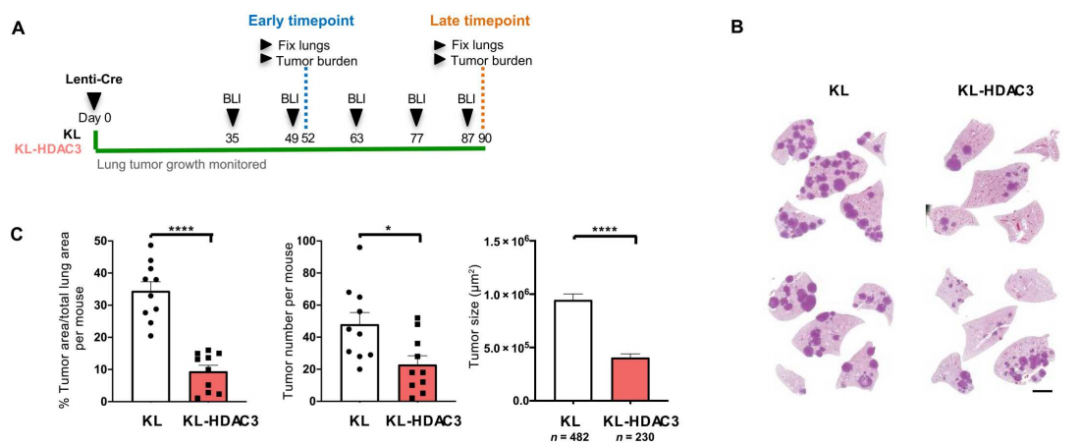
HDAC3对NSCLC的发生至关重要
因此,研究人员得出初步结论,HDAC3对KL和KP基因型驱动的NSCLC肿瘤生长至关重要,那么这种作用是通过怎样的分子机制实现呢?
为了回答这一问题,研究人员对KL和KP原发NSCLC肿瘤细胞进行了HDAC3的ChIP-seq测序,以识别全基因组内源性结合的HDAC3靶位点。结果显示,在KL和KP肿瘤中,共有1522个峰被HDAC3结合,对应于753个非冗余基因,其中富集程度最高的是转录因子NK2同源盒子1(NKX2-1)。
接下来研究人员评估了HDAC3和NKX2-1是否在NSCLC细胞中协调控制一组共同的靶基因,数据显示,在来源于KL原发性NSCLC肿瘤的永生化细胞系LJE1细胞中,HDAC3-KO和NKX2-1-KO以相同的方向影响基因表达变化。
RNA-seq结果表明,在NKX2-1-KO调控的基因中,83%也受到HDAC3-KO的调控,这表明大多数依赖NKX2-1的基因几乎都受到HDAC3的调控。
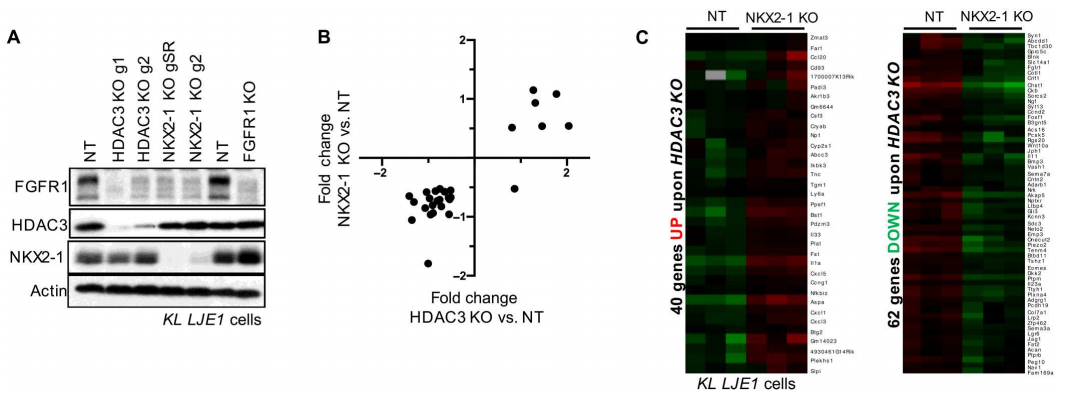
HDAC3与NKX2-1调控一组共同的靶基因的表达
在HDAC3和NKX2-1共同调控的靶基因中,Reuben等人选择了成纤维细胞生长因子受体1(FGFR1)进行进一步验证,它是组成FGFR蛋白家族的四种受体酪氨酸激酶之一,广泛参与促进肿瘤生长[5]。
RNA-seq分析结果表明,FGFR1的mRNA水平在NKX2-1-KO和HDAC3-KO的NSCLC细胞系中均下调;此外HDAC3和NKX2-1敲除,也显著下调了NSCLC细胞中FGFR1蛋白的表达水平。
值得注意的是,FGFR1已被证明介导了肿瘤患者对MEK抑制剂曲美替尼耐药的产生,MEK抑制剂是FDA批准的适用于包括NSCLC在内的多种肿瘤的临床用药,但是肿瘤患者极易对其产生耐药,其单药缓解率仅为12-30%,因此MEK抑制剂在临床中往往和其它靶向药物,如BRAF抑制剂联合使用 [6]。
既然在NSCLC中,HDAC3是FGFR1蛋白表达所必需的,那么使用HDAC3抑制剂,能否克服肺癌患者对曲美替尼的耐药呢?
为了验证这一点,研究人员首先在体外用曲美替尼对NSCLC细胞系进行了处理,可以看到,在长期曲美替尼处理后,NSCLC细胞表现出明显的耐药性,其FGFR1蛋白水平显著提高,但曲美替尼联合HDAC3抑制剂entinostat则可以逆转这一现象,也就是说,HDAC3抑制剂可以克服肺癌细胞对曲美替尼治疗的耐药。
接下来,研究者评估了上述HDAC3抑制剂entinostat联合MEK抑制剂曲美替尼,在LKB1突变型NSCLC小鼠模型体内的疗效:相比于曲美替尼单独治疗组,entinostat联合曲美替尼治疗组处理的小鼠表现出更低的肿瘤负荷,其肺部肿瘤体积减少79%,肿瘤数量减少63%。
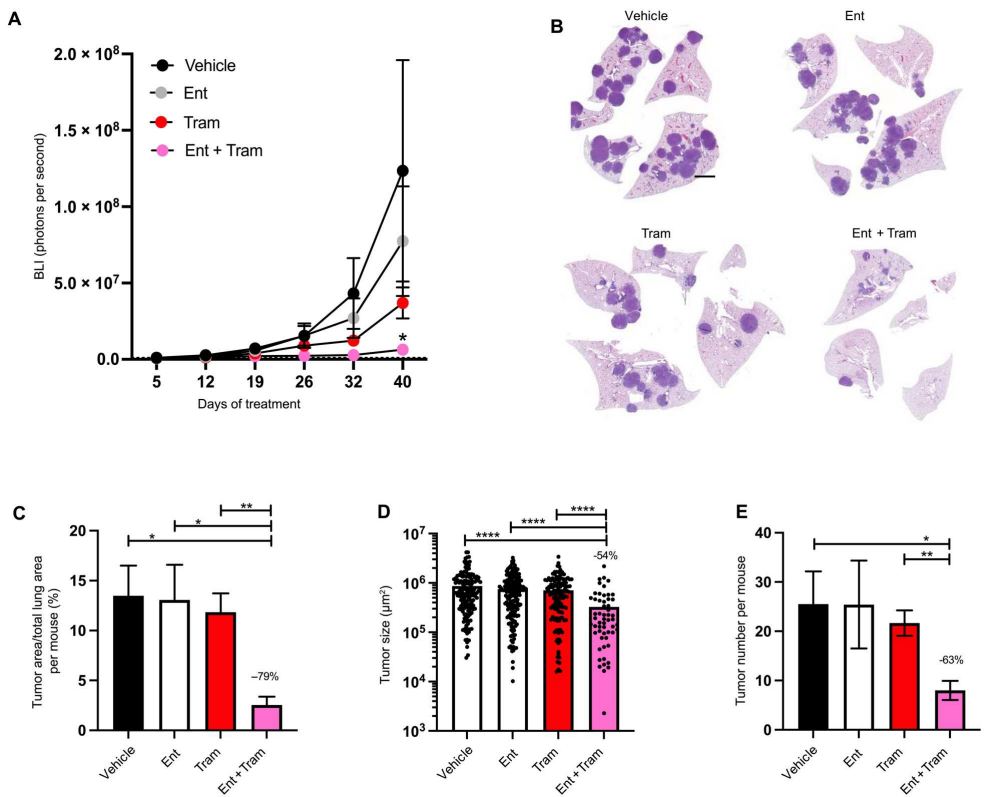
曲美替尼联合entinostat可有效抑制NSCLC的发展
H E染色切片中定量的肿瘤负荷也显示出类似的结果,与对照组相比,单独使用曲美替尼或entinostat都不会减轻肿瘤负荷,但二者的联合用药则可显著降低肿瘤负荷。
总之,本次研究的发现表明,在NSCLC基因工程小鼠模型中,同时使用MEK抑制剂曲美替尼和HDAC3抑制剂entinostat可以有效抑制肿瘤进展。先前已有诸多研究表明,在黑色素瘤和患者中,HDAC抑制剂可有效克服曲美替尼耐药的产生,而HDAC3正是克服曲美替尼耐药的关键靶点[7]。
而此次Reuben等人将上述联合用药方案在NSCLC治疗中的可行性进行了验证,并阐明了其具体机制,提出了一项有效的针对LKB1突变型NSCLC的靶向联合治疗新策略。论文第一作者兼共同通讯作者Lillian Eichner博士表示,这项研究证明HDAC3对于LKB1突变型NSCLC是不可或缺的,将有望成为治疗新靶点,后续将基于研究结论尽快开展临床研究。
参考文献:
[1]肖天龄,李娜,王娅丹等.靶向治疗在中的研究进展[J].癌症进展,2022,20(14):1428-1433.
[2] A. C. West, R. W. Johnstone, New and emerging HDAC inhibitors for cancer treatment.J. Clin. Invest. 124, 30 39 (2014).
[3] E. Ceccacci, S. Minucci, Inhibition of histone deacetylases in cancer therapy: Lessons from leukaemia. Br. J. Cancer 114, 605 611 (2016).
[4] Eichner LJ, Curtis SD, Brun SN, et al. HDAC3 is critical in tumor development and therapeutic resistance in Kras-mutant non-small cell lung cancer. Sci Adv. 2023.
[5] S. Dai, Z. Zhou, Z. Chen, G. Xu, Y. Chen, Fibroblast growth factor receptors (FGFRs):Structures and small molecule inhibitors. Cell 8, 614 (2019).
[6] E. Manchado, S. Weissmueller, J. P. Morris, C. C. Chen, R. Wullenkord, A. Lujambio, E. de Stanchina, J. T. Poirier, J. F. Gainor, R. B. Corcoran, J. A. Engelman, C. M. Rudin, N. Rosen,S. W. Lowe, A combinatorial strategy for treating KRAS-mutant lung cancer. Nature 534,647 651 (2016).
[7] Z. Wang, S. Hausmann, R. Lyu, T.-M. Li, S. M. Lofgren, N. M. Flores, M. E. Fuentes,M. Caporicci, Z. Yang, M. J. Meiners, M. A. Cheek, S. A. Howard, L. Zhang, J. E. Elias, M. P. Kim,A. Maitra, H. Wang, M. C. Bassik, M.-C. Keogh, J. Sage, O. Gozani, P. K. Mazur, SETD5-coordinated chromatin reprogramming regulates adaptive resistance to targeted pancreaticcancer therapy. Cancer Cell 37, 834 849.e13 (2020).
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 终结持续25年的争论!娄智勇/饶子和等团队合作最新Cell (2025-10-26)
- 上海药物所×临港实验室合作发表Cell论文:基于结构发现新型抗抑郁小分子 (2025-10-26)
- Mol Cancer:阻断甲状腺激素受体为前列腺癌治疗提供了新的途径 (2025-10-26)
- Science子刊:卞修武团队发现增强CAR-T细胞抗肿瘤效果的基因修饰策略 (2025-10-26)
- Nature Biotechnology:直击囊胚“混沌期”——长时程活体成像首次捕捉人类囊胚的染色体分离灾难 (2025-10-26)
- JNCCN:戒烟也应当是癌症治疗的一环!13万名癌症患者数据分析结果显示,癌症确诊后及时戒烟可大幅降低死亡风险,改善手术预后 (2025-10-26)
- NEJM:人工视网膜,帮助老年性黄斑变性患者恢复视力 (2025-10-25)
- 华中师范大学最新Cell子刊论文:开发治疗白血病的多肽类药物 (2025-10-25)
- 《科学》:膳食脂肪重塑昼夜节律!加州大学科学家发现,饮食中不饱和脂肪酸比例会影响昼夜节律,是人体生物钟与季节匹配与否的关键 (2025-10-25)
- 河南中州实验室发表Nature Metabolism论文:揭开大脑髓鞘再生修复的关键 (2025-10-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















