Cell子刊:刘星吟团队揭示肠道微生物代谢物吲哚 |
 |
来源:生物世界 2023-05-17 18:17
该研究首次阐释了肠道微生物代谢物吲哚-3-乳酸通过调控染色质的可及性进而调控胆固醇代谢影响结直肠癌发生发展的表观遗传学机制,为肠道微生物介导的抗肿瘤免疫的表观遗传机制提供了全新的见解,为CRC患者的防(Colorectal Cancer,CRC)是全世界范围内发病率第三的癌症,每年新增发病人数近200万(仅次于和),每年导致的死亡人数接近100万(仅次于肺癌)。大约每25个人就有1人会在其一生中患上结直肠癌。而在我国,结直肠癌年发病人数仅次于,2020年新增56万结直肠癌患者。更重要的是,近30年来,50岁以下的年轻人群中结直肠癌的发病率一直在上升。
肠道微生态失衡以及肠道微生物衍生代谢物的改变与结直肠癌有关。先前的研究表明,肠道益生菌,包括乳杆菌和双歧杆菌,在小鼠模型中具有改善炎症性肠病和结直肠癌发生发展的作用【1-3】。越来越多的研究表明,肠道菌群及其代谢物通过调节CD8+T细胞的活性发挥抗肿瘤作用【4】。然而肠道微生物产生的代谢物如何增强CD8+T细胞抗肿瘤功能的分子机制目前还不清楚。
新的研究表明,微生物衍生的代谢物可以诱导表观遗传修饰,对健康状况和疾病易感性具有潜在的影响。然而目前对结直肠癌中肠道微生物群与宿主表观遗传相互作用的分子机制还知之甚少。
2023年5月15日,南京医科大学刘星吟课题组在Cell Metabolism期刊发表了题为:Lactobacillus plantarum-derived indole-3-lactic acid ameliorates colorectal tumorigenesis via epigenetic regulation of CD8+ T cell immunity的研究论文。
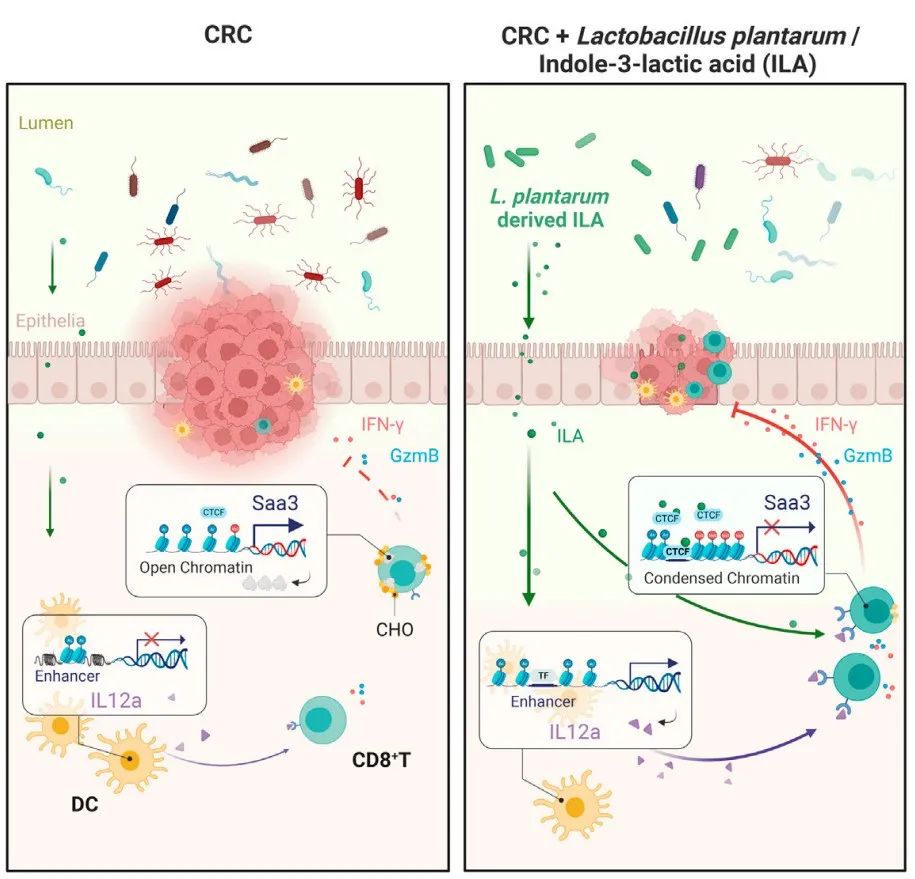
该研究发现,肠道微生物植物乳杆菌及其衍生代谢产物吲哚-3-乳酸(ILA)通过改变染色质的可及性增强CD8+T细胞抗结直肠肿瘤的表观遗传学新机制。

在该研究中,研究人员相继构建了急性小鼠肠炎模型,原位化学诱导的结直肠癌动物模型,结直肠癌皮下瘤模型,发现植物乳杆菌及其衍生的代谢物ILA能显著改善了小鼠的肠道炎症、肠道微生态失衡,抑制了结直肠癌肿瘤的生长。通过注射抗CD8抗体到皮下瘤小鼠以及荷瘤免疫缺陷Rag1 / 小鼠,研究者证实ILA的抑瘤作用部分是由肿瘤浸润的CD8+T细胞介导的。接着,研究者通过转移经ILA诱导BMDCs 和CD8+T细胞到荷瘤小鼠进一步证实,一方面ILA通过增强IL12a增强子区域周围的H3K27ac富集和染色质可及性来促进DCs的IL12a产生,从而启动CD8+ T细胞的抗肿瘤活性,另一方面它也可以直接增强肿瘤侵润CD8+T细胞分泌IFN- +和GzmB+而起到杀伤肿瘤细胞的功能。
大量证据表明,高饮食的摄入会增加患各种癌症的风险,包括结肠直肠癌【5】。研究者构建了高胆固醇饮食诱导下的原位结直肠癌模型,发现植物乳杆菌及其ILA可提高由HCD导致的脾脏、肠系膜淋巴结,肠道固有层中IFN- + GzmB+ CD8+T细胞的下降,而在高脂诱导的皮下瘤模型中,研究者发现植物乳杆菌及其ILA显著降低了肿瘤组织的胆固醇水平,提升了高脂导致的瘤微环境中IFN- + GzmB+ CD8+T细胞的比例。
为了进一步揭示ILA增强肿瘤侵润CD8+ T细胞功能的分子机制,研究者进一步通过ATAC-seq 和CUT&Tag等技术证实ILA通过与CD8+T 细胞的染色质绝缘子蛋白CTCF相互作用,改变染色质的可及性,调控了CD8+ T细胞中 CTCF与转录活性边界的差异结合并降低CD8+T细胞中调节胆固醇代谢的重要基因Saa3的表达,进而降低CD8+ T细胞的胆固醇水平,从而增强肿瘤浸润性CD8+T细胞的功能,抑制肿瘤的生长。
该研究首次阐释了肠道微生物代谢物吲哚-3-乳酸通过调控染色质的可及性进而调控胆固醇代谢影响结直肠癌发生发展的表观遗传学机制,为肠道微生物介导的抗的表观遗传机制提供了全新的见解,为CRC患者的防治策略的提供了重要的理论基础和实验依据。
南京医科大学基础医学院,生殖医学及其子代健康全国重点实验室,刘星吟教授为该论文通讯作者,南京医科大学基础医学院2018级博士研究生张青青为该论文的第一作者,2020级硕士研究生赵晴为该论文的第二作者,其他对该论文做出重要贡献的还包括刘星吟教授课题组研究生李涛,路龙娅,张鸿,王飞等人,南京医科大学胡志斌教授为该论文提供了重要的建议和支持。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 10月Nature杂志重磅级亮点研究成果解读! (2025-10-27)
- Sci Immunol:免疫细胞“精准打击”的背后——脂肪代谢或是关键指挥官 (2025-10-27)
- Nature:华人学者首次证实,新冠mRNA疫苗增强癌症免疫疗法,显著延长癌症患者生存期 (2025-10-26)
- 《自然·医学》:ctDNA可以指导肠癌治疗!3期临床结果显示,ctDNA阴性肠癌患者或可接受强度较低的治疗 (2025-10-25)
- 唐亚梅教授团队新研究提出卒中治疗优化方案 (2025-10-25)
- 迈迪斯亮相HICOOL2025全球创业者峰会 微创导航技术破解临床穿刺难题 (2025-10-24)
- 清华大学最新Cell论文:娄智勇/饶子和团队发现冠状病毒复制模板循环与RNA加帽的协同机制 (2025-10-24)
- 攻克LAM肺修复难题!Nature Communications重磅:mTOR-IL-6轴驱动肺泡细胞衰老,双靶联合治疗或成破局关键 (2025-10-24)
- 抗肿瘤药物甲氨蝶呤血药浓度快速监测研究获进展 (2025-10-24)
- 每 36 个娃就有 1 例,但病因成谜?! Transl Psychiatry:科学家破译自闭症患者的细胞“求救信” (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















