颜宁最新论文:Nav1.7拮抗剂的结构映射,为止痛药开发奠定基础 |
 |
来源:生物世界 2023-06-09 09:37
在这项研究中,研究团队将已知的配体结合位点映射到Nav通道的解析结构上,并提出了一个字母编码的命名系统来描述这些三维空间中的可成药位点。电压门控钠(Nav)通道是表达于细胞膜上的多亚基跨膜糖蛋白,由 和 亚基构成。在人体中, 亚基有9种不同的亚型,分别被命名为Nav1.1-1.9,负责发射具有组织特异性的电信号,它们的异常失活或激活与多种严重的神经、心和肌肉系统疾病相关。因此,Nav也成为重要的药物研发靶点,批准的多款抗癫痫药物、止痛药和抗药物就是以Nav为直接靶点。
近年来报道的真核Nav通道的高分辨率冷冻电镜结构帮助我们原子水平对某些药物的作用方式有了更深入的理解。但目前大多数以Nav为靶点的药物与Nav的准确结合模式尚不清楚,解析这些信息不仅有助于理解临床药物的作用方式的化学基础,也为今后的药物开发奠定重要基础。
Nav1.7是由SCN9A基因编码,主要定位于背根神经节神经元,被认为是疼痛治疗的重要靶点。Nav1.7的功能丧失会导致对疼痛不敏感,而在原发性红斑性肢痛症、阵发性剧痛症和小纤维神经病患者中,则发现了Nav活性增强突变。尽管许多卓越的制药公司付出了巨大努力,但大多数靶向Nav1.7的候选药物未能达到2期临床试验终点。Nav1.7与临床药物或先导化合物结合的复合物结构细节可能为我们提供分子水平的洞察力,这将有助于合理的药物设计或/和优化。
2023年6月3日,颜宁团队与清华大学潘孝敬团队合作,在Nature Communications期刊发表了题为:Structural mapping of Nav1.7 antagonists的研究论文。
该研究报告了用具有代表性化学骨架的药物和先导化合物处理过的人类Nav1.7的高分辨率冷冻电镜结构,分辨率为2.6-3.2 。并进一步提出了一个字母编码的命名系统来描述Nav1.7三维空间中的可成药位点。该研究所报道的结构分析为合理设计靶向Nav通道的药物开发提供了重要基础。
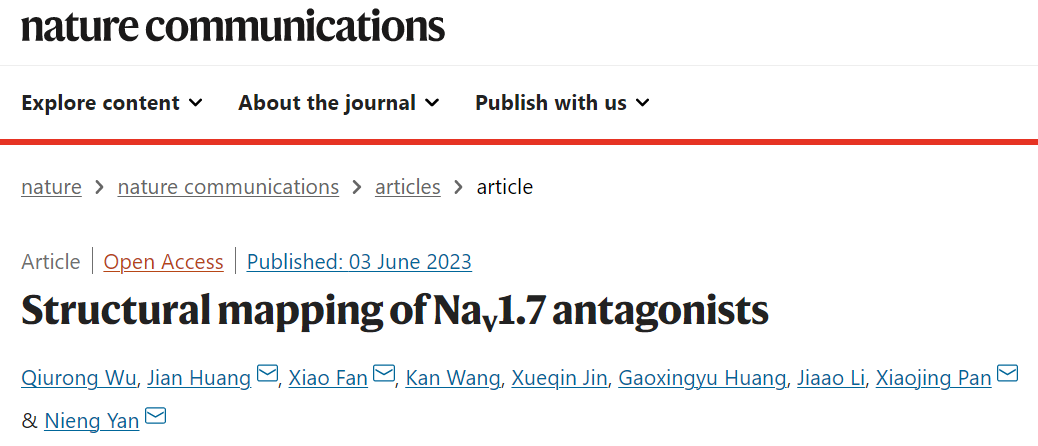
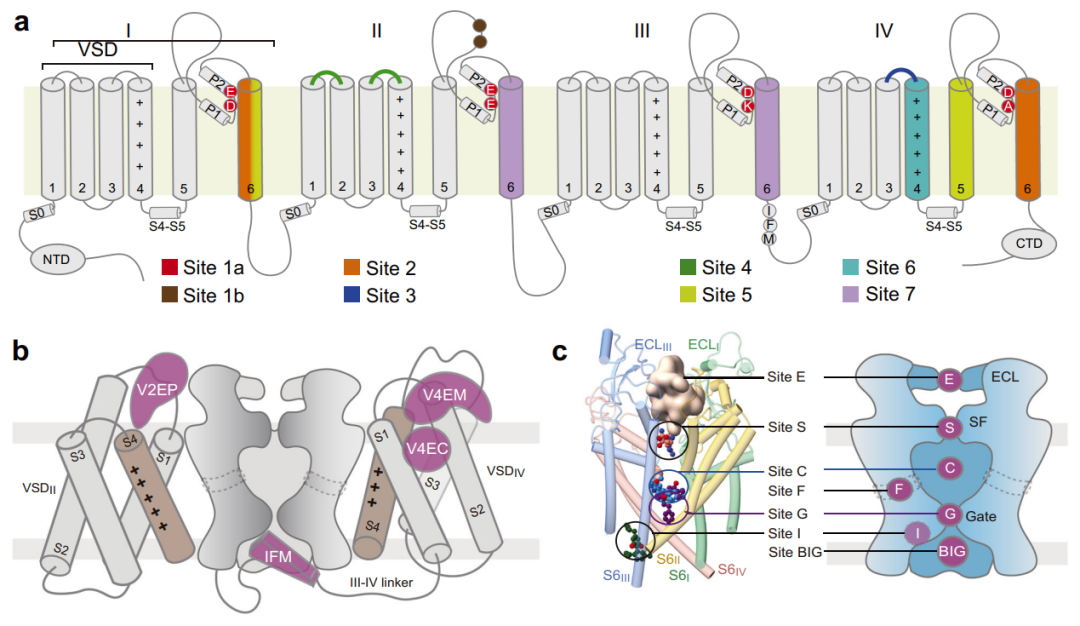
在真核Nav通道结构中,核心 亚基通常由1500-2200个残基组成,在跨膜和细胞外区域被很好地分解, 亚基由4个同源跨膜结构域构成,每个结构域包含6个跨膜的疏水 螺旋(S1-S6)。S1-S4构成电压感受器,能够调控S5和S6中间的钠离子通道的亲水性,引起细胞去极化或超极化,完成信号跨膜传递。
在这项研究中,为了探索Nav1.7上的可成药位点,研究团队选择了具有代表性的药物和 具有不同化学骨架的先导化合物,其中部分化合物受到化学品供应限制。
研究团队解析了以下药物与Nav1.7作用的冷冻电镜结构:布比卡因(bupivacaine,局部麻醉药物)、拉考沙胺(lacosamide,抗癫痫药物)、卡马西平(carbamazepine,抗惊厥药物,也用于治疗三叉神经痛和癫痫)、长春西汀(Vinpocetine,治疗脑血管疾病)、左旋哈氏豆属酸(hardwickiic acid,抗伤害性感受作用)、维索三嗪(vixotrigine,Nav1.7阻断剂,用于治疗三叉神经痛,临床试验未获成功)。
研究团队目前及之前的研究揭示了孔结构域(pore domain,PD)是一种具有不同化学式和结构的配体的多功能受体。
该研究报告了用具有代表性化学骨架的药物和先导化合物处理过的人类Nav1.7的高分辨率冷冻电镜结构,分辨率为2.6-3.2 。具体来说,Nav1.7的BIG位点容纳卡马西平、布比卡因、拉考沙胺,出乎意料的是,第二个拉考沙胺分子从中央腔插入选择性过滤器(selectivity filter,SF)。膜内开口(Fenestrations)是各种状态依赖性药物的热门位点。该研究还显示,长春西汀以及左旋哈氏豆属酸结合到孔结构域的III-IV膜内开口,而维索三嗪则穿过孔结构域的IV-I膜内开口。
这项研究结果建立一个三维结构图,从现有和以前的结构中总结出Nav通道上已知的药物结合位点。
Nav拮抗剂结合位点的结构图
Nav通道是众所周知的天然毒素和临床应用药物靶点,随着毒素和药物作用下的Nav通道的高分辨率结构越来越多,传统的结合位点定义可能不再能反映药物结合位点的多样性和复杂性,特别是孔结构域(PD)上的结合位点。
在这项研究中,研究团队将已知的配体结合位点映射到Nav通道的解析结构上,并提出了一个字母编码的命名系统来描述这些三维空间中的可成药位点。
非成瘾性止痛药是目前未满足的医疗保健需求,长期以来,由于缺乏精确的结构,阻碍了靶向Nav通道药物的合理设计。尽管近年来Nav通道的结构蓬勃发展,但人工智能(AI)促进的药物发现仍然受到训练数据库的限制,其中配体结合结构的数量仍然很少。此外,构象动力学超出了目前结构预测的能力,因此,与配体结合的靶蛋白的实验结构解析对于药物发现是必不可少的。该研究所报道的结构分析为合理设计靶向Nav通道的药物开发提供了重要基础。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- STTT:AAV基因治疗阿尔茨海默病 (2025-06-09)
- 首款国产冠脉负压机械抽吸导管获批 (2025-06-09)
- 空气污染会诱发早产?!Environ Sci Technol首次揭示PM2.5是如何通过干扰孕妇的新陈代谢增加早产风险 (2025-06-09)
- 十年顽疾终获确诊:上海六院风湿免疫科成功诊治罕见Buschke硬肿病 (2025-06-09)
- Nature:突破性发现,CREM揭示CAR (2025-06-08)
- BMJ:张惠杰团队发表SGLT2抑制剂治疗代谢功能障碍相关性脂肪性肝炎的原创性临床研究成果 (2025-06-08)
- 《自然》:按摩这个位置,加速大脑“排毒”!逆转大脑衰老的新方法来了 (2025-06-08)
- 《自然·衰老》:又发现近300种蛋白与阿尔茨海默病相关,7蛋白模型预测AD状态AUC最高可达0.88! (2025-06-07)
- 刷新记录!瑞康曲妥珠单抗获批治疗HER2突变非小细胞肺癌,中国患者迎来高效低毒新疗法 (2025-06-07)
- 你是一喝酒就脸红吗?多项研究:喝酒脸红者更易衰老、出现大脑中Aβ病理加重、炎症因子分泌减少等问题,增加阿尔茨海默病发生风险 (2025-06-07)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















