2023年7月Cell期刊精华 |
 |
来源:100医药网原创 2023-07-31 10:33
2023年7月份即将结束,7月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。2023年7月份即将结束,7月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.
doi:10.1016/j.cell.2023.06.009
在一项新的研究中,来自中国多家研究机构的研究人员利用自主研发的空间转录组测序技术Stereo-seq以及snRNA-seq技术,绘制了猕猴大脑皮层细胞类型分类图谱,揭示了细胞类型组成与灵长类动物各个脑区的关系,为进一步研究神经回路提供了分子和细胞基础。相关研究结果于2023年7月12日在线发表在Cell期刊上,论文标题为 Single-cell spatial transcriptome reveals cell-type organization in the macaque cortex 。

图片来自Cell, 2023, doi:10.1016/j.cell.2023.06.009。
在这项新的研究中,这些作者利用一种新开发的大视场空间转录组方法---Stereo-seq和一种独立开发的方法制备了用于实验的厘米级猕猴大脑薄片。
通过结合大规模单细胞转录组分析,他们获得了食蟹猕猴整个大脑皮层的全面的三维单细胞图谱,为系统分析大脑皮层内细胞类型分布特异性和区域特异性以及分子特征提供了指导。
此外,他们还发现,谷氨酸能神经元、GABA能神经元和非神经元细胞在整个大脑皮层的分布表现出明显的皮层特异性和区域特异性。有趣的是,细胞类型组成与视觉和躯体感觉系统中脑区的分层组织之间存在着明显的相关性。同一层次的脑区往往具有相似的细胞类型组成,从而揭示了细胞组成与脑区结构之间的关系。通过与可公开获得的人脑和小鼠大脑单细胞数据进行跨物种比较,这些作者发现了灵长类动物特有的谷氨酸能神经元,它们主要位于第4层,高度表达与人类疾病相关的基因,包括FOXP2、DCC和EPHA3。
2.
doi:10.1016/j.cell.2023.06.019
一条腿受伤的小鼠在另一条腿上经历了的 苏醒 ,就好像这些干细胞正在准备愈合伤口一样。类似的事情也发生在蝾螈身上,它们是肢体再生的大师。斑马鱼的心脏损伤会引发肾脏和大脑等远处器官的某些变化。
美国斯坦福大学生物工程助理教授Bo Wang说, 在许多不同的有机体中,你可以看到整个身体对损伤做出反应。但这些反应是否真地有任何功能一直不清楚,因此这就是我们关注的重点。
在一项新的研究中,Wang和他的同事们发现这种全身协调是真涡虫(planarian worm)伤口愈合和随后组织再生的关键部分。了解是什么开启和关闭了再生,以及再生是如何协调的,也有助于为针对癌症的研究提供信息,毕竟癌症通常被认为是永不愈合的伤口。相关研究结果于2023年7月21日在线发表在Cell期刊上,论文标题为 Ultrafast distant wound response is essential for whole-body regeneration 。
Wang希望了解这些反应是如何协调的。一种可能的机制是细胞外信号相关激酶(extracellular signal-related kinase, ERK)通路。细胞利用ERK通路相互交流,并以某种波形向外发送信号。如果组织受伤,最近的细胞会将这种受伤信息 传递 给邻近的细胞,然后邻近的细胞又会将信息告诉它们的邻居。这种信号波以一种电话游戏的方式传遍整个有机体。
只是有一个问题:过去的研究已表明,ERK信号波的移动速度太慢,没有任何作用。Wang说, 如果我以每小时 10 微米的速度传播信号,那么它需要几天才能通过一毫米。在这种速度下,信号从真涡虫的一个区域传递到另一个区域的速度太慢,无法帮助伤口愈合和再生。 这在人类身上可能不是问题。我们的循环系统可以让信号迅速传遍全身。但真涡虫没有循环系统来加速这一过程。
因此,Wang和他的同事们开始追踪ERK信号波从真涡虫的一端传播到另一端的过程。他们发现信号的传播速度比以前观察到的快 100 多倍。ERK信号波不是以小步从一个细胞移动到另一个细胞,而是沿着超长的体壁肌肉细胞移动。这些细胞就像 超级高速公路 ,将信号从身体的一端加速传到另一端。时间从之前认为的几天缩短到几小时。
3.
doi:10.1016/j.cell.2023.07.018
原肠胚形成(gastrulation)是胚胎从空心球体重组装为多层结构的过程,被认为是人类发育的 黑匣子 。这是因为出于生物伦理的考虑,人类胚胎的培养时间通常不会超过14天,而原肠胚形成发生在受精后17至21天之间。此外,目前模拟原肠胚形成的干细胞模型还不能包括产生卵黄囊和胎盘所需的胚胎外组织。
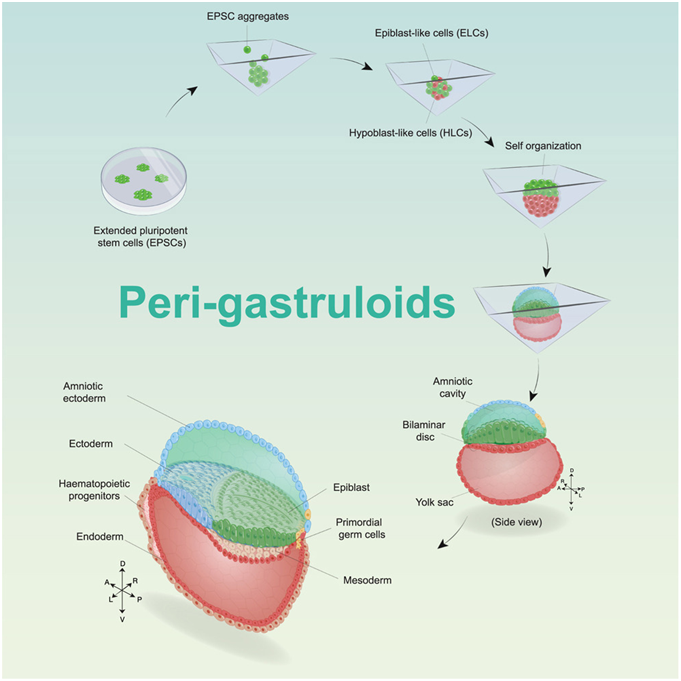
图片来自Cell, 2023, doi:10.1016/j.cell.2023.07.018。
在一项新的研究中,来自美国德克萨斯大学西南医学中心的研究人员报告了一种开发 外周类原肠胚(peri-gastruloids) 的新方法。外周类原肠胚是一种类似胚胎的结构,包括支持组织之一的卵黄囊,而卵黄囊是以前的模型所缺少的。相关研究结果于2023年7月20日在线发表在Cell期刊上,论文标题为 Modeling post-implantation stages of human development into early organogenesis with stem-cell-derived peri-gastruloids 。
论文通讯作者、德克萨斯大学西南医学中心干细胞生物学家Jun Wu说, 虽然人类原肠胚形成和早期器官形成的非整合模型是由始发态(primed)的人类多能干细胞开发的,但这些模型缺乏在胚胎发育模式(embryo patterning)和形态发生中发挥重要作用的胚胎外细胞。胚胎组织和胚外组织的存在使得科学家们能够研究原肠胚形成期间外胚层(epiblast)、羊膜和卵黄囊之间的相互作用---这在人类以前是无法实现的。
4.
doi:10.1016/j.cell.2023.06.004
脑成像扫描是帕金森病(PD)和排除其他运动障碍的有力工具。PD患者大脑---特别是大脑中的黑质(substantia nigra)---的路易体(Lewy body)和路易神经突(Lewy neurites)中存在的 -突触核蛋白( -synuclein, -Syn)可将这种疾病与其他类帕金森病(parkinsonism)区分开来。遗憾的是,目前还没有有效的 -Syn PET示踪剂。
如今,在一项新的研究中,中国科学院深圳先进技术研究院(SIAT)研究员叶克强(Ye Keqiang)教授领导的一个研究团队发现了一种名为F0502B的化合物,有望用于 -Syn的成像和突触核蛋白病(synucleinopathy)的诊断。相关研究结果于2023年7月7日在线发表在Cell期刊上,论文标题为 Development of an -synuclein positron emission tomography tracer for imaging synucleinopathies 。
这些作者发现,在PD猴子模型中,[18F]标记的F0502B以高亲和力与 -Syn原纤维特异性结合,将它们与A 和Tau原纤维区分开来。
对PD猴子模型的PET成像显示,[18F]-F0502B可特异性检测到 -Syn聚集物。聚集的 -Syn水平可能随着时间的推移而增加,从而导致PET特异性结合信号升高。
5.
doi:10.1016/j.cell.2023.05.012
从俄克拉荷马州一条受污染的沟渠中分离出来的一种地杆菌(Geobacter)有一种不寻常的附属物---一条长的细胞外纳米线,可以导电。这种纳米线中的电子传递链将电子从细菌中带到一种不溶性的外部电子受体,以帮助这种细菌制造能量。这种微米级的长程电子传递被认为在早期地球的微生物代谢中发挥了重要作用。
如今,在一项新的研究中,来自美国阿拉巴马大学伯明翰分校、弗吉尼亚大学医学院和法国巴斯德研究所的研究人员利用和低温电镜,发现这类由细胞色素(cytochrome)蛋白长链组成的纳米线似乎在原核微生物中无处不在---在细菌和古生菌中都是如此。相关研究结果发表在2023年6月22日的Cell期刊上,论文标题为 Extracellular cytochrome nanowires appear to be ubiquitous in prokaryotes 。

图片来自Cell, 2023, doi:10.1016/j.cell.2023.05.012。
除了强烈表明这些细胞外细胞色素纳米线(extracellular cytochrome nanowire, ECN)在许多依靠长距离电子传递进行代谢的原核生物中无处不在,论文共同通讯作者、阿拉巴马大学伯明翰分校的Fengbin "Jerry" Wang博士;论文共同通讯作者、巴斯德研究所的Mart Krupovic博士;论文共同通讯作者、弗吉尼亚大学医学院的Edward H. Egelman博士说,他们的研究结果还证实,在硫还原地杆菌(Geobacter sulfurreducens)中发现的ECN并非独一无二。
硫还原地杆菌有三种ECN,每种都是由三种不同的c型细胞色素(c-type cytochrome)中的一种组成的长链。每个c型细胞色素分子包含多个血红素(heme),即附着在这个细胞色素上的含铁卟啉,并在电子转移中发挥作用。血红素更多地被称为红细胞血红蛋白中的氧载体。
6.
doi:10.1016/j.cell.2023.06.002
利用工程化的T细胞来破坏癌细胞目前在治疗某些类型的癌症上已经表现出了成功,比如和,然而,其对于实体瘤的治疗效果并不理想。而缺乏成功的原因之一在于T细胞仅能靶向作用一种抗原(肿瘤上发现的靶向性蛋白),如果某些肿瘤细胞不表达这种抗原的话,其就会逃避T细胞的攻击。近日,一篇发表在国际杂志Cell上题为 Vaccine-boosted CAR T crosstalk with host immunity to reject tumors with antigen heterogeneity 的研究报告中,来自MIT等机构的科学家们通过研究发现了一种克服这一障碍的方法,其能利用一种疫苗来增强名为嵌合抗原受体(CAR)T细胞的工程化T细胞的反应,同时还能帮助系统产生新的T细胞从而靶向作用其它的肿瘤抗原;在对小鼠进行的研究中,研究人员发现,这种方法或许会使得肿瘤更有可能被根除。
研究者Darrell Irvine教授说道,这种疫苗的增强似乎能驱动一种名为抗原扩散(antigen spreading)的过程,在该过程中,机体自身的免疫系统就能与工程化的CAR T细胞合作从而拒绝那些并非所有细胞都表达被CAR T细胞所靶向作用的抗原的肿瘤。目前批准了多种T细胞疗法来治疗血液癌症,这些疗法都是基于细胞,其能被工程化改造来展示受体从而识别癌细胞上存在的特殊抗原。
为了尝试将这种疗法应用到胶质母细胞瘤(一类脑癌)中,研究人员设计了CAR-T细胞来靶向作用EGFR受体的一个突变版本,然而,并非所有的胶质母细胞瘤细胞都会表达这种抗原,而且当其被CAR-T细胞攻击时,有些胶质母细胞瘤细胞就会通过停止靶向性抗原的产生来产生反应。在2019年的一项研究中,研究者Irvine及其同事通过在使用工程化T细胞后不久将疫苗直接输注到小鼠体内来增强CAR-T细胞抵御胶质母细胞瘤的疗效,这种携带被CAR-T细胞靶向作用的相同抗原的疫苗就会被淋巴结中的免疫细胞所摄取,而CAR-T细胞则会在淋巴结中接触到它。
这项研究中,研究人员发现,这种疫苗的提升不仅能帮助工程化的CAR-T细胞攻击肿瘤,还会产生另一种意想不到的效应,其或许还有助于产生靶向作用其它肿瘤抗原的宿主T细胞。这种被称之为 抗原扩散 (antigen spreading)的现象是可取的,因为其能产生一类特殊的T细胞群,当其在一起发挥作用时就能完全根除肿瘤病预防肿瘤再生。研究者Irvine表示,这或许正是能帮助你处理实体瘤中抗原异质性的东西,因为如果让宿主T细胞来攻击其它抗原,其就能够进来并杀灭CAR-T细胞无法杀灭的肿瘤细胞。
7.
doi:10.1016/j.cell.2023.05.044
我们DNA中的遗传计划通过蛋白实现了功能,而蛋白是我们身体结构和活动的基础。然而,蛋白质组---细胞或特定区域内的所有蛋白---仍然是相对神秘的,因为蛋白景观是非常复杂的。例如,人类制造了数以万计的不同蛋白。
为了帮助破译这种复杂性,在一项新的研究中,来自美国斯坦福大学的研究人员领导开发了一种名为TransitID的新方法,用于追踪活细胞中蛋白的完整活性。相关研究结果于2023年6月28日在线发表在Cell期刊上,论文标题为 Dynamic mapping of proteome trafficking within and between living cells by TransitID 。

图片来自Cell, 2023, doi:10.1016/j.cell.2023.05.044。
实现这一任务的现有技术,即显微镜和质谱蛋白质组学,要么允许科学家们在活细胞中一次只研究少数几种蛋白,要么提供一个非常详细的但仍然是死细胞中所有蛋白的快照。
论文通讯作者、斯坦福大学医学院遗传学教授Alice Ting说, 我们的新技术允许人们结合显微镜和质谱蛋白质组学的优势,实际观察活体样本--包括它们移动和发挥功能时的动态变化,并以无偏见的方式一次观察到所有的蛋白。以前还没有结合这些优势的方法。
TransitID也适用于追踪在细胞间移动的蛋白。在这种水平上追踪蛋白的细节和活性,可能能够揭示关于细胞如何交流的未知信息。此外,它在各种疾病和治疗方法的研究中也有明显的应用,包括在癌症和神经退行性疾病的领域。
8.Cell:新型疫苗技术在小鼠体内产生更多针对的抗体
doi:10.1016/j.cell.2023.04.024
在一项新的研究中,美国加州理工学院开发的一项新技术旨在制造更强效的疫苗,首先从 SARS-CoV-2(引起 的冠状病毒)开始。在小鼠研究中,这种原型疫苗激发的抗体是目前 COVID-19 疫苗的五倍。这种新疫苗产生的抗体对 SARS-CoV-2 原始毒株、delta 变种和 omicron 变种均有效。相关研究结果近期发表在Cell期刊上,论文标题为 ESCRT recruitment to SARS-CoV-2 spike induces virus-like particles that improve mRNA vaccines 。这项新的研究是在加州理工学院生物学与生物工程学教授Pamela Bj rkman的实验室进行的。这项研究由Magnus Hoffmann领导。
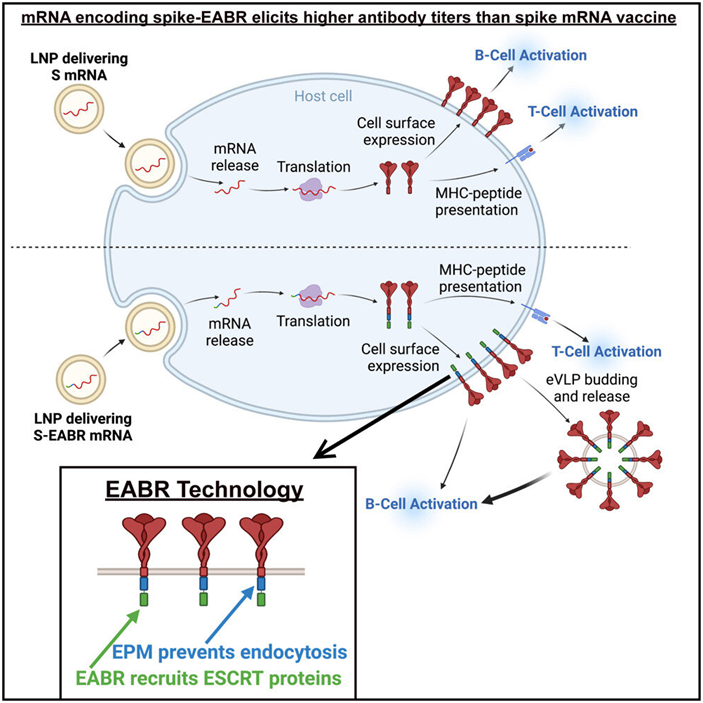
图片来自Cell, 2023, doi:10.1016/j.cell.2023.04.024。
这种新的候选疫苗被称为 混合(hybrid) 疫苗,因为它结合了辉瑞公司和莫德纳公司疫苗使用的 mRNA 技术的特点和基于蛋白纳米颗粒的疫苗(如 Novavax 疫苗)的特点。除了帮助对抗 COVID-19,这种技术有朝一日还可能改进针对HIV、流感病毒和其他多种病原体的疫苗。
Bj rkman说, 对于任何疫苗接种或感染,抗体水平都会随着时间的推移而降低。理想的疫苗能产生强大的免疫反应,引起高水平的抗体,减轻病毒多种变种的感染,并引起细胞毒性T细胞反应,杀死受感染的细胞,防止严重疾病和死亡。
9.Cell:表观遗传改变也可导致神经胶质瘤产生
doi:10.1016/j.cell.2023.06.022
癌症通常源于细胞DNA的突变和其他改变,不过来自美国丹娜-法伯癌症研究所和布罗德研究所的研究人员发现神经胶质瘤---无法治愈的脑瘤---可能源于表观基因组(epigenome)的变化,其中表观基因组是沉积在DNA上的化学修饰(比如甲基化)的集合,这些化学修饰在不改变DNA本身序列的情况下改变基因活性。相关研究结果于2023年7月25日在线发表在Cell期刊上,论文标题为 Modeling epigenetic lesions that cause gliomas 。
破坏调控元件的表观遗传病变是潜在的癌症驱动因素。然而,我们缺乏验证其致癌影响的实验模型。在这项新的研究中,这些作者模拟了异柠檬酸脱氢酶(isocitrate dehydrogenase)突变神经胶质瘤中出现的畸变,这种胶质瘤表现出 DNA 过度甲基化。
这些作者确定了人类神经胶质瘤中活性发生表观遗传改变的两个基因,包括一个致癌的癌基因--- PDGFRA---和一个预防癌症的肿瘤抑制基因:Cdkn2a。
他们在动物模型中发现这种表观基因组的变化激活了癌基因PDGFRA,同时沉默了肿瘤抑制基因Cdkn2a,这两者同步作用,刺激了神经胶质瘤的形成。这些发现强调了通过靶向表观基因组来抑制神经胶质瘤的疗法的潜力。
10.Cell:在癌症幸存者体内发现能够同时识别多种不同癌症相关靶标的杀伤性T细胞
doi:10.1016/j.cell.2023.06.020
在一项新的研究中,来自英国卡迪夫大学等研究机构的研究人员在成功治愈晚期实体癌的患者体内发现了一类高级杀伤性T细胞。他们指出这些占主导地位的、成功的杀伤性T细胞能够同时识别多种不同的癌症相关靶标。相关研究结果于2023年7月24日在线发表在Cell期刊上,论文标题为 Targeting of multiple tumor-associated antigens by individual T cell receptors during successful cancer immunotherapy 。
这些作者研究了在丹麦国家癌症免疫治疗中心(CCIT-DK)接受肿瘤浸润淋巴细胞(tumor-infiltrating lymphocyte, TIL)疗法的晚期实体癌患者。TIL疗法是从患者的肿瘤中提取白细胞(T细胞),在实验室中大量培养它们,然后将它们回输给患者,帮助免疫系统杀死癌细胞。CCIT-DK是欧洲TIL疗法的先驱。
在过去十年进行的I/II期临床试验中,31名患者接受了TIL疗法。为这些患者提供的所有 TIL 细胞都是 T 细胞。然后,这些作者等待观察这些患者中哪些人清除了癌症,并将重点放在他们身上。然后,他们用储存的患者自身肿瘤细胞样本挑战这些患者的血细胞,看看哪些 T 细胞有反应。他们发现,癌症幸存者在清除癌症一年多后,仍然对自己的癌症表现出非常强的杀伤性 T 细胞反应。

图片来自Cell, 2023, doi:10.1016/j.cell.2023.06.020。
随后,这些作者继续研究这些杀伤性 T 细胞是如何区分癌细胞和正常细胞的。通过使用算法,他们成功地预测了癌症特异性T细胞能识别什么,预测的依据是T细胞对什么产生反应,以及已知健康细胞和癌细胞之间存在哪些蛋白差异。
他们发现,这些新的能够识别多种靶标的 T 细胞能够识别癌细胞内蛋白的多种变化。总之,他们在几名癌症幸存者体内发现了这些能够识别多种靶标的 T 细胞。论文通讯作者、卡迪夫大学医学院的Andy Sewell教授说, 我们想知道一些接受过TIL疗法治疗的晚期癌症患者是如何成功清除癌症的,因此我们去寻找答案。通过观察TIL疗法治疗后癌症被完全清除的患者的血液,我们追踪到了成功的T细胞。我们用患者自身的癌症、其他患者的癌症以及其他癌症类型对它们进行了测试。
结果表明,癌症幸存者体内能够识别多种靶标的杀伤性 T 细胞识别癌症的能力大大优于普通的抗癌杀伤性 T 细胞。此外,同时对多种癌症相关蛋白做出反应的能力意味着这些T细胞可以对大多数类型的癌症做出反应,因为癌症只需要表达其中一种异常的靶标就会被识别为危险的靶标并被杀死。重要的是,我们在癌症幸存者的血液中发现了大量能够识别多种靶标的 T 细胞。迄今为止,我们还没有在癌症进展患者体内发现这类能够识别多种靶标的 T 细胞。到目前为止,患者人数还很少,但是能够识别多种靶标的T细胞仍有可能与完全缓解或癌症清除有关。 ( 100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 明眸皓齿打一个正确的生肖,最佳资询落实 (2025-09-13)
- Nature:DNA甲基化“随机时钟”——EVOFLUX破译肿瘤演化史,重塑临床预后新维度 (2025-09-13)
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















