Science:重大进展!利用经过基因改造的益生菌引导CAR |
 |
来源:100医药网原创 2023-10-16 17:25
几年来,科学家们已经成功地利用嵌合抗原受体(CAR)T细胞(CAR-T)靶向血细胞表面上的特定抗原来治疗白血病和淋巴瘤患者。但事实证明,利用CAR-T细胞靶向实体瘤(如乳腺癌和结肠癌)是特别困难的。几年来,科学家们已经成功地利用嵌合抗原受体(CAR)T细胞()靶向血细胞表面上的特定抗原来治疗和患者。但事实证明,利用CAR-T细胞靶向实体瘤(如和)是特别困难的。
实体瘤含有一系列显示出不同抗原的细胞,而且体内的健康细胞也往往携带这些抗原。因此,确定一种一致且安全的靶标阻碍了大多数治疗实体瘤的 CAR-T 细胞疗法在开发的第一阶段取得成功。
抗癌的突破性方法
在一项新的研究中,来自美国哥伦比亚大学的研究人员报告了一种攻击肿瘤的新方法。他们设计了肿瘤定植细菌(益生菌),让定植在肿瘤中的它们产生合成靶标,从而引导 CAR-T 细胞消灭这些含有合成靶标的。相关研究结果发表在2023年10月13日的Science期刊上,论文标题为 Probiotic-guided CAR-T cells for solid tumor targeting 。

论文通讯作者、哥伦比亚大学生物医学工程学副教授Tal Danino说, 我们的益生菌平台能让CAR-T细胞攻击多种类型的肿瘤。传统的 CAR-T细胞疗法依赖于靶向天然肿瘤抗原。这是第一个将经过基因改造的T 细胞与经过基因改造的细菌配对,安全、系统、有效地向实体瘤递送合成抗原的例子。这将对许多癌症的治疗产生重大影响。
在实体瘤上产生合成靶标
Danino实验室通过对寻找肿瘤的细菌进行编程,在实体瘤上涂上CAR-T细胞能够识别的合成抗原,从根本上构建出能够攻击通用抗原的通用CAR-T细胞。
这些作者预计,随着进一步的改进,这一平台将能够治疗任何类型的实体瘤,而无需识别特定的肿瘤抗原,从而避免了为每种癌症类型和每位患者定制 CAR-T 细胞产品的需要。
设计 活药物
这种益生菌引导的CAR-T细胞(probiotic-guided CAR-T cell, ProCAR)平台是这些作者首次成功地将经过基因改造的益生菌与CAR-T细胞结合在一起,而且还首次证明了CAR-T细胞对直接在肿瘤内产生的合成抗原有反应。
论文共同第一作者、Danino实验室博士生Rosa Vincent说, 将靶向肿瘤的细菌和CAR-T细胞结合在一起的优势,提供了一种新的肿瘤识别策略,这为开发经过基因改造后用于活体疗法的细菌群落奠定了基础。我们选择将这两种细胞疗法的最佳特点---利用细菌产生肿瘤靶标,利用T细胞消灭恶性---结合起来,从而弥补这两种疗法各自的局限性。
安全有效的平台
这些作者证实在力低下和免疫力健康的小鼠身上,该平台在多种人类和小鼠癌症模型中都是安全有效的。事实上,这项新的研究表明人类 T 细胞尤其受益于肿瘤内免疫刺激性细菌的存在,它们的杀伤肿瘤的功能得到了进一步增强。
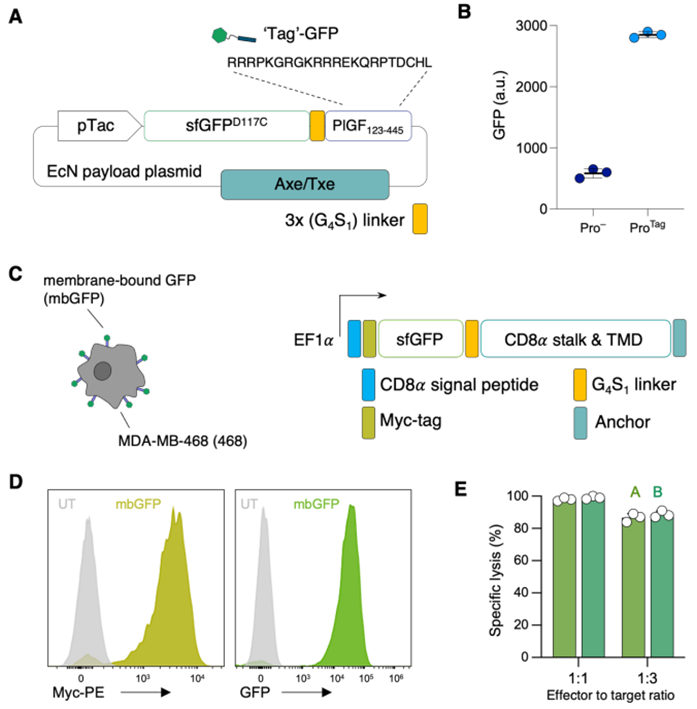
图片来自Science, 2023, doi:10.1126/science.add7034。
Danino说, 总体来说,我们的ProCAR平台代表了一种提高CAR-T细胞疗法在实体瘤中有效性的新策略。虽然我们仍处于研究阶段,但它可以为癌症治疗开辟新的途径。
持续合作的下一步
这项新的研究Danino实验室是与哥伦比亚大学瓦格罗斯内外科医学院微生物学与免疫学助理教授Nicholas Arpaia的实验室正在进行的合作的一部分。
这些作者此前已经开发出了能一起递送免疫疗法有效载荷的细菌(ure Medicine, 2019, doi:10.1038/s41591-019-0498-z,详细新闻参见报告:)。他们正在继续完善他们的盐焗工作,并希望开始临床试验,以全面评估该平台对人类癌症患者的安全性和有效性。(100医药网 100yiyao.com)
参考资料:
1. Rosa L. Vincent et al. . Science, 2023, doi:10.1126/science.add7034.
2. Eric M. Bressler et al. . Science, 2023, doi:10.1126/science.adk6098.
3. Engineered Bacteria Paint Targets on Tumors for Cancer-killing T s to See
https://www.engineering.columbia.edu/news/engineered-bacteria-paint-targets-tumors-for-cancer-killing-t-cells-to-see
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Cell:指出一篇与冠状病毒抗病毒药物开发相关的研究存在缺陷 (2025-07-30)
- 《科学》:糖尿病治疗重大突破!科学家开发新型分子胶,可将RAS与PI3K亲和力提高500倍,无需胰岛素也可降糖 (2025-07-30)
- 打破昼夜节律局限!Nat Neurosci:CLOCK 基因揭秘人类大脑认知超凡进化的关键密码 (2025-07-30)
- ACS Nano:浙江大学研究发现,人类卵泡液和精浆中存在纳米塑料,影响受精能力和精子质量 (2025-07-30)
- Cell Genomics:AI 助力抗癌新突破!机器学习模型精准预测肿瘤侵袭性 (2025-07-30)
- Cell:我国科学家利用人工智能驱动的策略实现了蛋白质的快速高效进化 (2025-07-29)
- 第四届国际生物医药产业发展大会 (2025-07-29)
- 2025年7月Cell期刊精华 (2025-07-29)
- Cell:告别“单兵作战”!SPIDR技术开启“联合作战”新纪元,一次实验看清数十种RNA调控蛋白的“社交网络” (2025-07-29)
- Nature:中国学者开发基因编辑蚊子,有望终结疟疾传播 (2025-07-29)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















