Cell Research:王耿团队发现并鉴定首个哺乳动物RNA转运通道——ANT2 |
 |
来源:生物世界 2024-06-03 09:36
该研究成功鉴定出线粒体RNA跨膜转运的关键内膜通道蛋白,揭示了mt-dsRNA导出的调控机制。厦门大学生命科学学院王耿教授团队(王鹏程为第一作者)在Cell Research期刊发表了题为:ANT2 functions as a translocon for mitochondrial cross-membrane translocation of RNAs的研究论文, 该了一套巧妙的生化体系,成功鉴定出首个哺乳动物线粒体RNA转运蛋白 ANT2,并且揭示了ANT2对mt-dsRNA触发的先天的调控作用。

近几十年来,人们一直试图寻找线粒体膜上的RNA转运通道,但均未取得好的研究进展,主要原因是缺乏一套有针对性的并可以排除RNA降解酶干扰的实验体系。
在这项研究中,王耿团队首先建立了一套高效的体外RNA导入生化体系,并利用该体系进行了RNA转运通道蛋白的筛选。通过初步筛选,研究团队发现了定位于线粒体内膜上的腺嘌呤核苷酸转运酶-2(ANT2)。之后,研究团队通过完整线粒体和线粒体膜脂质体导入实验,初步确定了ANT2对线粒体RNA导入的正调控作用。随后使用进一步简化的细菌细胞膜脂质体和纯脂质体导入体系,直接证明了ANT2是哺乳动物线粒体RNA的内膜转运通道蛋白。
在细胞层面,ANT2的蛋白水平与细胞质中mt-dsRNA的含量直接正相关,过表达或敲低ANT2会导致一型干扰素反应的激活或抑制。最后,研究团队在卵清蛋白肽(NP-OVA)诱导的小鼠炎症模型中发现,敲低ANT2可以缓解小鼠肝脏炎症,表明ANT2调节的mt-dsRNA的释放不仅在启动先天免疫而且在诱导机体炎症中发挥着关键作用。
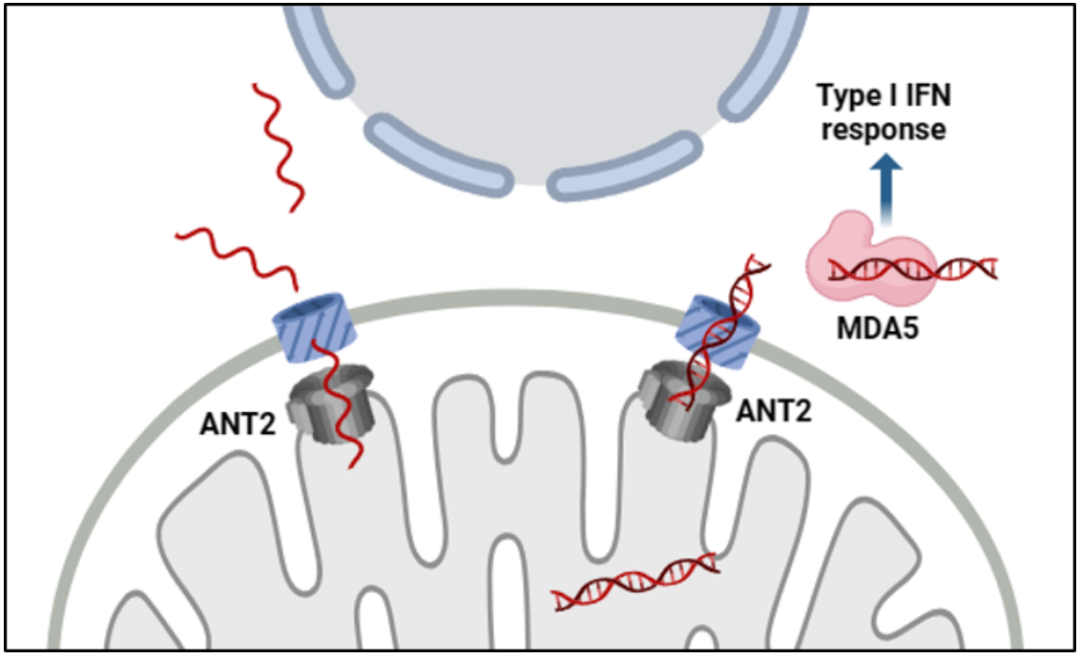
综上所述,该研究成功鉴定出线粒体RNA跨膜转运的关键内膜通道蛋白,揭示了mt-dsRNA导出的调控机制。这些发现对于理解mt-dsRNA在免疫中的作用机制提供了更好的基础,同时也为自身免疫疾病潜在的治疗方案提供了理论依据。建立的高效体外生化体系不仅有助于鉴定通路中其它潜在的RNA转运蛋白和组分,也为其它孔道蛋白的功能研究提供了新的工具。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Cell:我国科学家利用人工智能驱动的策略实现了蛋白质的快速高效进化 (2025-07-29)
- 第四届国际生物医药产业发展大会 (2025-07-29)
- 2025年7月Cell期刊精华 (2025-07-29)
- Cell:告别“单兵作战”!SPIDR技术开启“联合作战”新纪元,一次实验看清数十种RNA调控蛋白的“社交网络” (2025-07-29)
- Nature:中国学者开发基因编辑蚊子,有望终结疟疾传播 (2025-07-29)
- Science:利用人工智能揭示蛋白质稳定性规则,有望推进蛋白质工程变革 (2025-07-29)
- 屡获殊荣:诺华川西南林业碳汇项目荣获《南方周末》2025年度ESG创新案例奖 (2025-07-28)
- 一滴血测早期食管癌!Adv Sci:新型生物芯片结合AI,9种囊泡蛋白助诊断准确率超90% (2025-07-28)
- Science:利用新开发的谱系追踪工具绘制肿瘤细胞的历史和位置,从而揭示其生长模式 (2025-07-28)
- Cell:新研究确定了世界上首个有望预防危及生命的HTLV-1病毒感染的新方法 (2025-07-28)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















