浙江大学医学院研究者们揭示了Hsc70通过靶向PD |
 |
来源:100医药网 2024-06-09 14:42
该研究阐明了hsc70介导的PD-L1溶酶体降解的分子机制,为肿瘤免疫治疗提供了靶点和治疗策略。抑制和是癌症的标志之一,而重新激活抗反应已成为癌症治疗的一个快速发展的领域。pd - 1 / pd - l1免疫检查点抑制(ICI)是一种很有前景的治疗某些类型癌症的临床疗法,但仍有相当比例的患者产生耐药性。PD-L1在与抗体结合后倾向于内化,其中一部分是溶酶体介导的降解,然而,大多数内化的PD-L1可以储存在循环内体中并重新填充到细胞膜上,介导对靶向PD-L1的ICI治疗的抗性。因此,促进溶酶体降解和抑制PD-L1的再循环是克服ICI治疗耐药的一种有希望的方法。CMTM6是一种普遍表达的蛋白,已被证明可以帮助PD-L1再循环回到质膜,CMTM6的缺失促进了PD-L1通过溶酶体降解,但是,PD-L1的溶酶体降解机制尚不清楚。
目前对PD-L1降解的研究多集中在蛋白酶体途径上,对内体溶酶体途径中PD-L1降解的研究较少。Hsc70(热休克蛋白家族A成员8)是一种细胞质伴侣蛋白,在内体微自噬(eMI)和伴侣介导的自噬(CMA)中起重要作用。大约40%的哺乳动物蛋白含有KFERQ-like motif,它可以作为hsc70的底物。hsc70通过CMA与Lamp2a相互作用,直接将货物蛋白传递给溶酶体,或通过其羧基末端盖子结构域与带负电荷的磷脂酰丝氨酸相互作用,从而通过emi将胞质货物内化到核内体。
虽然CMA和eMI具有相似的基序,但它们的底物并不完全重叠,当具有相似KFERQ基序的蛋白质处于半聚集状态时,它们形成高分子量复合物或不能被CMA展开和降解,但它们仍然可以被eMI降解。翻译后修饰也可以决定蛋白质是否被路由到eMI或CMA。最近的一项研究表明,乙酰化的Tau减少了CMA对其的降解,同时促进了eMI对其的参与。近年来,eMI因其潜在的分子机制和潜在的生物学功能而备受关注,eMI作为一种选择性自噬,在生物大分子的降解中起着重要作用,但其研究相对缺乏。因此,研究PD-L1溶酶体降解的机制和调控可以为提高免疫效能提供新的思路。

图片来源:
近日,来自浙江大学医学院第一附属医院的研究者们在Nat Commun杂志上发表了题为 Hsc70 promotes anti-tumor immunity by targeting PD-L1 for lysosomal degradation 的文章,该研究阐明了hsc70介导的PD-L1溶酶体降解的分子机制,为肿瘤免疫治疗提供了靶点和治疗策略。
针对PD-1/PD-L1通路的免疫检查点抑制已成为治疗癌症的一种强有力的临床策略,但其疗效因各种耐药机制而复杂,产生耐药的原因之一是PD-L1自身在抗体结合后的内化和再循环。抑制溶酶体介导的PD-L1降解对于保持PD-L1再循环回细胞的数量至关重要。
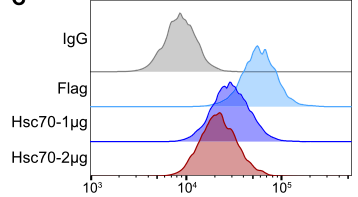
Hsc70通过溶酶体促进PD-L1降解
图片来源:
在实验中,研究者使用质谱法鉴定Hsc70是主要的pd - l1相互作用蛋白之一,研究发现Hsc70通过内溶体-溶酶体途径促进PD-L1降解,减少PD-L1再循环到细胞膜。这种作用依赖于Hsc70-PD-L1结合,抑制CMTM6-PD-L1相互作用。研究者进一步鉴定了一种Hsp90 / 抑制剂AUY-922,发现它可以诱导Hsc70的表达和PD-L1溶酶体的降解。Hsc70过表达或AUY-922处理均可降低雌性小鼠PD-L1表达,抑制肿瘤生长,促进抗肿瘤T细胞反应,增强抗肿瘤免疫;AUY-922可进一步增强抗pd - l1和抗ctla4治疗的抗肿瘤疗效。该研究阐明了hsc70介导的PD-L1溶酶体降解的分子机制,为未来癌症免疫治疗的发展提供了途径。
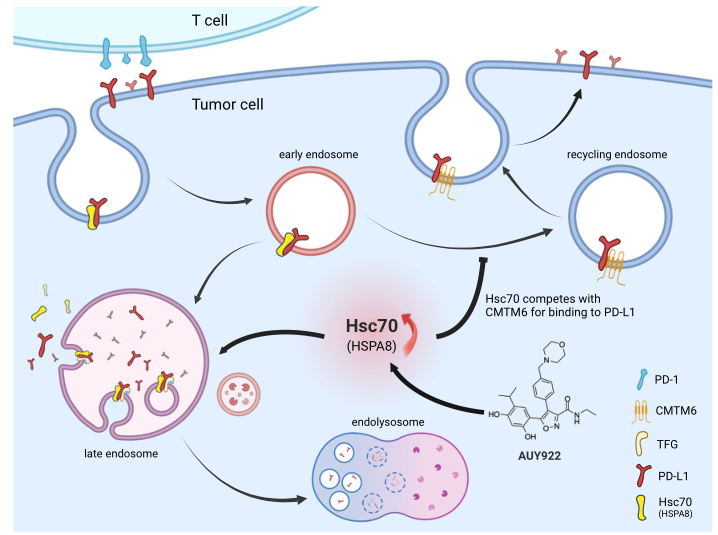
Hsc70通过eMI靶向PD-L1降解促进抗肿瘤免疫的示意图模型
图片来源:
综上所述,本研究表明,增强Hsc70与底物蛋白(如PD-L1)之间的相互作用可以缓解疾病进展,这些结果还提出了一种可能性,即通过调节蛋白量或修饰Hsc70来调节eMI也可能有益于其他eMI相关疾病,包括癌症、神经退行性疾病和其他与衰老相关的疾病。 ( 100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Cell:我国科学家利用人工智能驱动的策略实现了蛋白质的快速高效进化 (2025-07-29)
- 第四届国际生物医药产业发展大会 (2025-07-29)
- 2025年7月Cell期刊精华 (2025-07-29)
- Cell:告别“单兵作战”!SPIDR技术开启“联合作战”新纪元,一次实验看清数十种RNA调控蛋白的“社交网络” (2025-07-29)
- Nature:中国学者开发基因编辑蚊子,有望终结疟疾传播 (2025-07-29)
- Science:利用人工智能揭示蛋白质稳定性规则,有望推进蛋白质工程变革 (2025-07-29)
- 屡获殊荣:诺华川西南林业碳汇项目荣获《南方周末》2025年度ESG创新案例奖 (2025-07-28)
- 一滴血测早期食管癌!Adv Sci:新型生物芯片结合AI,9种囊泡蛋白助诊断准确率超90% (2025-07-28)
- Science:利用新开发的谱系追踪工具绘制肿瘤细胞的历史和位置,从而揭示其生长模式 (2025-07-28)
- Cell:新研究确定了世界上首个有望预防危及生命的HTLV-1病毒感染的新方法 (2025-07-28)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















