重大进展!中性粒细胞在过敏条件下成为肥大细胞的“猎物”?!Cell:活体显微镜技术的应用,使科学家首次实现实时观察肥大细胞与中性粒细胞间的微妙互动 |
 |
来源:100医药网 2024-08-14 11:47
通过在细胞培养环境中复现活体组织中的中性粒细胞捕获情景,研究团队成功锁定了这一过程中的分子机制。他们发现,肥大细胞会分泌白三烯B4,一种中性粒细胞常用的聚集信号。肥大细胞,作为免疫系统中的关键角色,因触发过敏反应而闻名。它们在遭遇过敏原时释放出化学信号,引起诸如肿胀、炎症等典型的过敏症状。
如今,来自马克斯-普朗克免疫生物学与表观遗传学研究所和明斯特大学的研究人员发现了肥大细胞的一个隐藏天赋:它们可以捕获并利用另一种叫做中性粒细胞的免疫细胞。这一惊人发现为人们了解免疫系统,尤其是过敏反应的原理提供了新的思路。
相关研究结果于2024年8月2日在线发表在Cell期刊上,论文标题为 Neutrophil trapping and nexocytosis, mast cell-mediated processes for inflammatory signal relay 。

炎症,作为人体对伤害的响应,其特征包括发热、疼痛、红肿及功能障碍,是身体自我保护机制的一部分,旨在清除有害物质并促进修复。然而,过度的炎症会损害组织,引发疾病。在这一过程中,各种免疫细胞扮演着核心角色,协同应对不同的刺激,进而影响炎症的进程。
过敏反应期间的免疫细胞诱捕
肥大细胞,作为组织中的哨兵,蕴藏着丰富的促炎颗粒,是触发炎症反应的核心。当这些细胞感知到威胁,不论是真实的病原体还是误判的过敏原,它们便会释放颗粒中的内容物,引发一系列炎症反应。尤其在某些敏感体质中,即便是日常环境中看似无害的因素,也能激起肥大细胞的过敏警报。目前,肥大细胞与过敏反应部位其他免疫细胞之间的相互作用在很大程度上尚未得到研究。
在本研究中,研究团队利用活体小鼠模型和先进的显微技术,实时观察到了过敏反应中肥大细胞与其他细胞的动态交互。
这一突破性发现由明斯特大学医学生物化学研究所的研究团队于2023年首度揭示,他们惊讶地在肥大细胞内部观测到了中性粒细胞的存在。 我们目瞪口呆, 研究领头人L mmermann感慨道, 活生生的中性粒细胞竟然躲进了活生生的肥大细胞体内。这一发现超乎寻常,若非借助活体显微镜技术,恐怕难以捕捉到如此微妙的细胞间互动,这充分证明了活体显微镜技术的非凡实力。
肥大细胞胞内陷阱(MIT)
中性粒细胞,作为免疫系统的前线战士,能迅速响应潜在威胁,它们在血液中巡逻,迅速涌入炎症区域。它们不仅吞噬入侵者,释放抗菌物质,还能构建 中性粒细胞胞外陷阱(NETs) ,形成网状结构捕捉敌人。此外,中性粒细胞间的协作形成了强大的集体防线,保护健康组织。虽然中性粒细胞在感染与非感染性损伤中的作用已被广泛认知,但在过敏引发的炎症中,它们的角色仍鲜为人知。
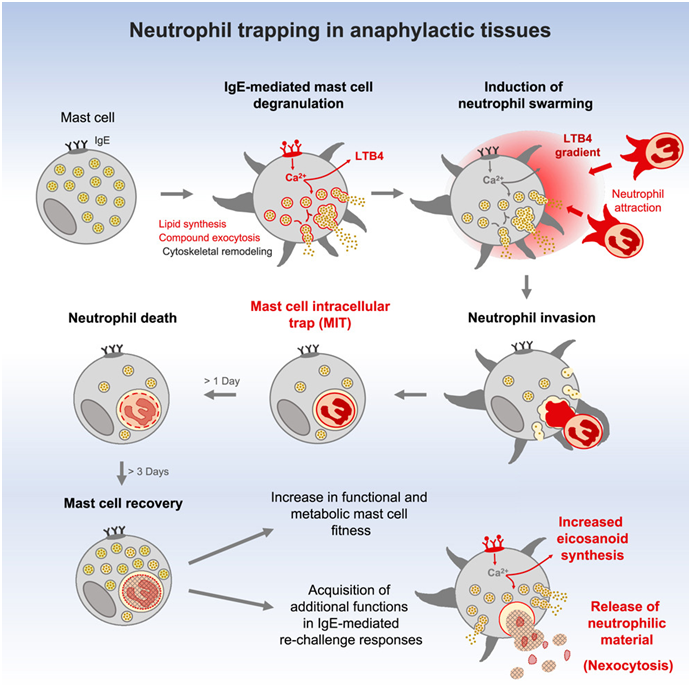
图片来自Cell, 2024, doi:10.1016/j.cell.2024.07.014
论文的第一作者兼共同通讯作者,马克斯-普朗克免疫生物学与表观遗传学研究所的Michael Mihlan博士解释道: 我们很快意识到,肥大细胞与中性粒细胞之间的这种 双重捕获 现象绝非偶然。我们渴望探明肥大细胞如何捕捉中性粒细胞,以及这一行为背后的动机。 通过在细胞培养环境中复现活体组织中的中性粒细胞捕获情景,研究团队成功锁定了这一过程中的分子机制。他们发现,肥大细胞会分泌白三烯B4,一种中性粒细胞常用的聚集信号。通过这一信号,肥大细胞能吸引中性粒细胞靠近,一旦距离足够,便将其吞噬至细胞内的特殊结构 肥大细胞胞内陷阱(MIT) 。
L mmermann教授补充道: 颇具讽刺意味的是,中性粒细胞在感染状态下构建的由DNA和组蛋白组成的网状陷阱,本用于捕捉微生物,却在过敏环境下反成为肥大细胞的猎物。
回收的中性粒细胞增强肥大细胞功能
在国际团队的共同努力下,研究者们不仅在人体样本中验证了肥大细胞胞内陷阱(MIT)的形成,还追踪了中性粒细胞被捕捉后的命运。他们发现,被肥大细胞吞噬的中性粒细胞最终会走向凋亡,其残留物质则被肥大细胞存储。Mihlan博士表示: 研究至此,我们见证了一场意想不到的剧情反转。肥大细胞能再利用中性粒细胞的残留物,提升自身功能和代谢效率。更令人惊奇的是,肥大细胞还能以延迟方式释放新吸收的中性粒细胞成分,激发后续免疫反应,辅助炎症和免疫防御的持续。
L mmermann教授总结道: 我们对肥大细胞与中性粒细胞的协同机制有了全新洞见,这为过敏反应和炎症研究增添了重要维度。这一发现揭示了肥大细胞如何巧妙运用中性粒细胞,强化自身能力,这可能对慢性过敏性炎症疾病的演变产生深远影响。 目前,研究团队正积极探索这一互动模式在肥大细胞介导的人类炎症性疾病中的作用,以及这一发现是否能催生治疗过敏和炎症性疾病的创新疗法。这一系列发现不仅深化了我们对免疫系统复杂互动的理解,也为未来防治相关疾病提供了新的线索和希望。(100yiyao.com)
参考资料:
Michael Mihlan et al. . Cell, 2024, doi:10.1016/j.cell.2024.07.014.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Science:利用转录组学的主动学习框架识别疾病表型的调节因子 (2025-10-30)
- 新冠/ARDS 康复者总反复感染?《自然・免疫学》揪出元凶:缺氧悄悄“剪断”免疫细胞基因开关,后遗症持续半年以上 (2025-10-30)
- 为什么说“母乳喂养能降低乳腺癌风险”?Nature:生育+哺乳让 CD8⁺T 细胞驻留乳房数十年,三阴性乳腺癌风险大降 (2025-10-30)
- 2025年10月Science期刊精华 (2025-10-30)
- 2025世界银屑病日呼吁:正认知、早干预、稳控制,拥抱健康生活 (2025-10-29)
- Biomaterials:给肝脏装上“纳米导弹”!科学家有望精准打击酒精肝损伤 (2025-10-29)
- JCI:新研究揭示一种潜在致命性癫痫的发病机制 (2025-10-29)
- 人类再生医学找到新线索!Cell:蝾螈断肢再生靠“全身备战”,交感神经触发干细胞“总动员” (2025-10-29)
- 造血干细胞研究进展(第14期) (2025-10-29)
- Nature头条:揭开“猫屎咖啡”独特风味背后的奥秘 (2025-10-28)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















