《自然》子刊:食盐竟能激活抗癌免疫!科学家首次发现,氯化钠可以增强T细胞的抗癌能力 |
 |
来源:网络 2024-09-08 09:20
需要提醒大家的是,虽然这两个研究都证明氯化钠可以增强抗肿瘤免疫,但是这一结论目前仍处于临床前探索阶段。由意大利Humanitas研究医院Enrico Lugli领衔的团队[1]和德国慕尼黑工业大学Christina E. Zielinski领衔的研究团队[2],在著名期刊《自然 免疫学》上背靠背发表了两篇重要研究论文。
这两项研究论文得出了同样的结论:食盐可以增强杀伤性T细胞的抗肿瘤免疫力。尤其值得一提的是,Enrico Lugli团队还在小鼠身上证实,仅通过高盐饮食就能增强T细胞的抗癌能力,抑制肿瘤的生长。
据了解,这也是科学家首次发现氯化钠可以影响CD8阳性T细胞的抗癌功能。这两项研究还从不同的角度,揭示了氯化钠助力抗癌的潜在机制,对于新型免疫治疗策略的研发,有重要价值。

▲Lugli团队论文首页截图
(这个标题,真是相当直白了)
Enrico Lugli团队和Christina E. Zielinski团队,为什么会想到研究盐对T细胞抗癌活性的影响呢?
这主要是因为,最近几年陆续有一些研究发现氯化钠(食盐)可以调节免疫。例如,高盐饮食会抑制中性粒细胞抗击细菌性感染的能力[3];高盐饮食可以通过影响肠菌调节NK细胞活性,抑制肿瘤生长[4];还有研究发现,高盐会干扰调节性T细胞的线粒体呼吸,导致调节性T细胞功能障碍[5]。
从上面三个研究中,我们不难看出,高盐似乎对抗肿瘤免疫有利(提升NK细胞的抗癌活性,抑制免疫的调节性T细胞活性被降低)。这就不免让人好奇:氯化钠对抗癌主力杀伤性T细胞有何影响?
遗憾的是,Lugli团队和Zielinski团队都没有找到相关的研究数据。显然,这还是一个未知的研究领域。于是,这两个研究团队从不同的角度开始了自己的研究。Lugli团队主要围绕高盐饮食展开,而Zielinski团队则侧重于体外高盐处理对T细胞的影响。接下来,我们就主要介绍Lugli团队的研究成果。

▲Zielinski团队论文首页截图
Lugli团队先用高盐(80mM)处理CD8阳性幼稚T细胞(同时加入anti-CD3/CD28和IL-2激活T细胞),还用尿素和甘露醇处理另一组T细胞(对T细胞影响非常小),模拟高盐带来的渗透压变化,作为对照组。
与对照组细胞相比,氯化钠处理增加了颗粒酶B(GZMB)和TIM3编码基因的表达,这说明高盐诱导出了活化的效应记忆T细胞。RNA测序结果还显示,与对照组相比,高盐诱导了转录组水平的变化,与效应或细胞毒性相关的转录本上调,如IFNG、TNF、GZMB和TBX21(编码T-bet);与干性相关的转录本也上调,如FOXO1、RUNX1、SATB1和ID3等。
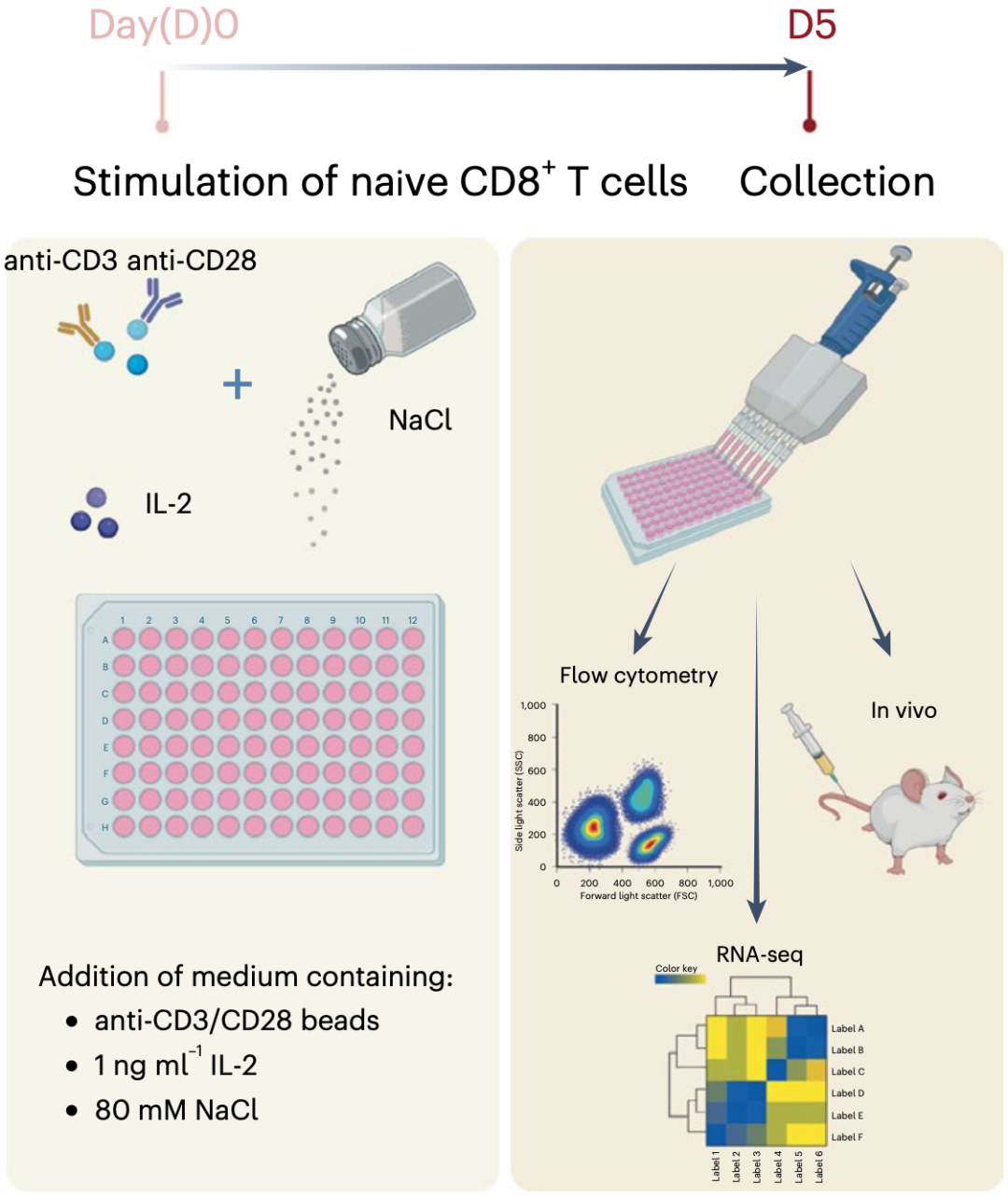
▲研究过程
他们还发现,诱导T细胞代谢重编程的主调节因子MYC、糖酵解相关的PKM和LDHA,以及质膜谷氨酰胺转运体SLC1A5和SLC7A5的编码基因表达也上调。这说明,高盐还会重塑T细胞的代谢。
从细胞功能的变化来看,与对照组相比,高盐处理增加了干扰素- (IFN )和脱颗粒标志物CD107a的产生。体外细胞毒性试验结果显示,高盐处理过的T细胞杀死黑色素瘤细胞的效率要高于IL-2处理的细胞。此外,他们还注意到,T细胞受体(TCR)信号转导增强;而且高盐要发挥作用,必须得结合TCR的激活刺激。
基于以上研究结果,Lugli团队认为,高盐会促进人CD8阳性T细胞的效应分化。
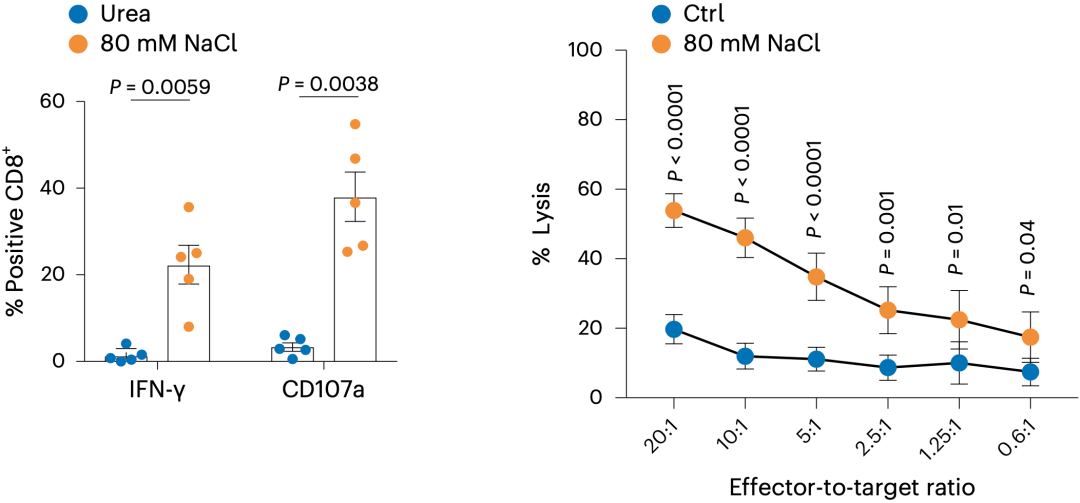
▲高盐处理让T细胞变强
有了体外实验的支持,Lugli团队就想做一些大胆的探索:高盐饮食会不会影响小鼠的抗肿瘤免疫。
他们给小鼠安排了高盐饮食(食物含盐量为4%,水的含盐量为1%),让小鼠自由进食。在高盐饮食(HSD)开始两周之后,他们再给小鼠移植MC38结肠腺癌细胞。他们发现,高盐饮食会导致氯化钠在肿瘤中蓄积,而其他器官中蓄积较少,且不会影响小鼠的总体健康状况。
从抗肿瘤效果来看,与正常饮食(NSD)相比,高盐饮食能显著抑制肿瘤的生长。不过,在使用抗CD8单抗清除小鼠CD8阳性T细胞后,高盐的抗肿瘤效果就会完全消失。这说明,CD8阳性T细胞是高盐饮食表现出抗肿瘤作用的关键。
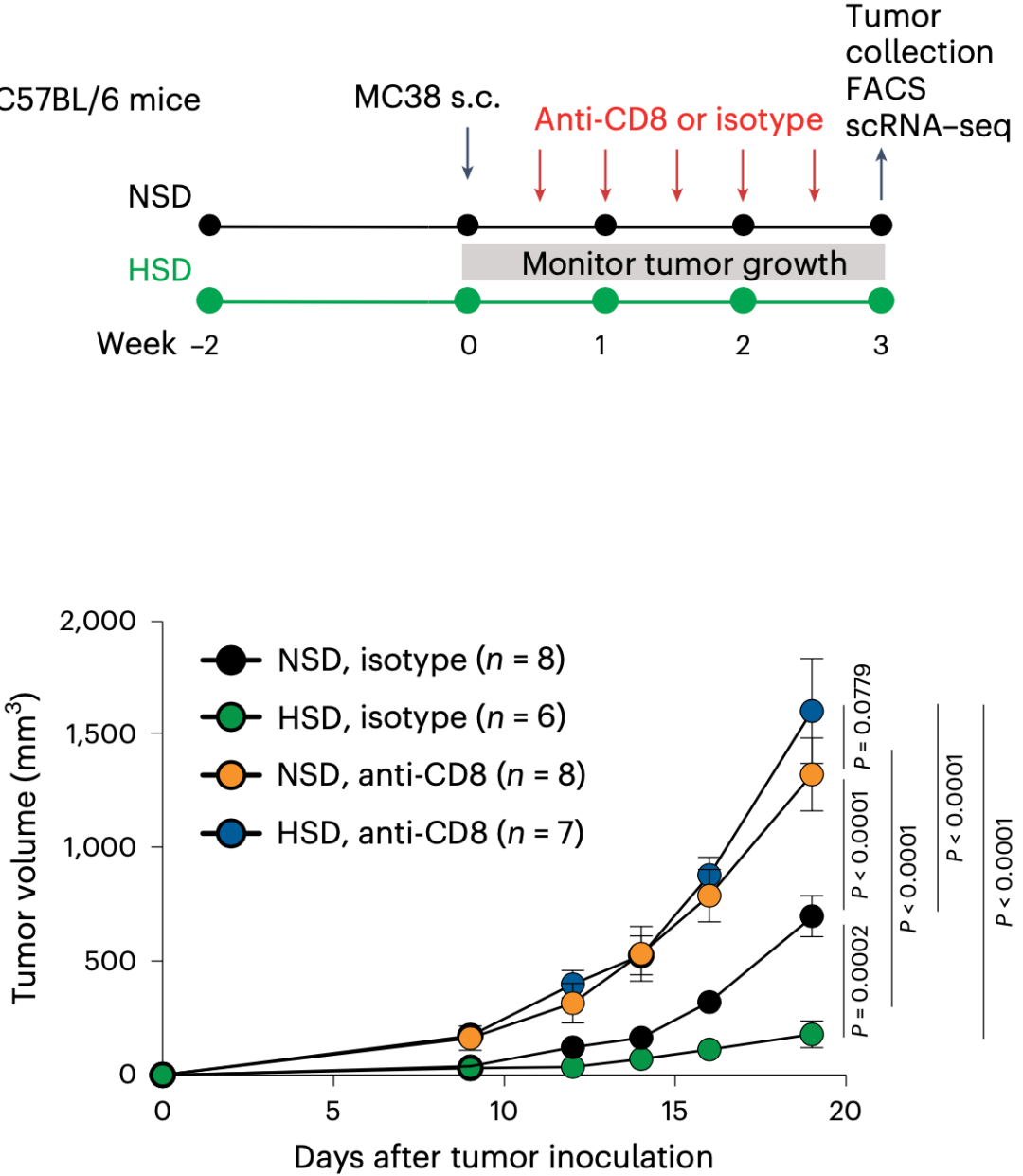
▲高盐饮食抗癌,CD8阳性T细胞是关键
在分析小鼠肿瘤中的免疫细胞变化之后,Lugli团队发现高盐饮食组的肿瘤中CD8阳性T细胞、自然杀伤细胞和CD4阳性T细胞的频率增加,是对照组的两倍有余。
具体到CD8阳性T细胞来说,与对照组相比,高盐饮食组中与终末分化和衰竭相关的转录本(如Prdm1、Eomes、Maf、Hspa1a和Gzmk)减少了,而编码细胞毒性分子的转录本(Gzmf、Gzme、Gzmd、Prf1)或与活化(Tnfrsf9、Nfkb1)和效应分化(Irf8、Csf1、Id2)相关的转录本增加了。
不难看出,高盐饮食在促进免疫激活的同时还消除了免疫抑制。值得注意的是,Lugli团队还发现高盐饮食诱导的CD8阳性T细胞变化,与PD-1抑制剂诱导的相似。
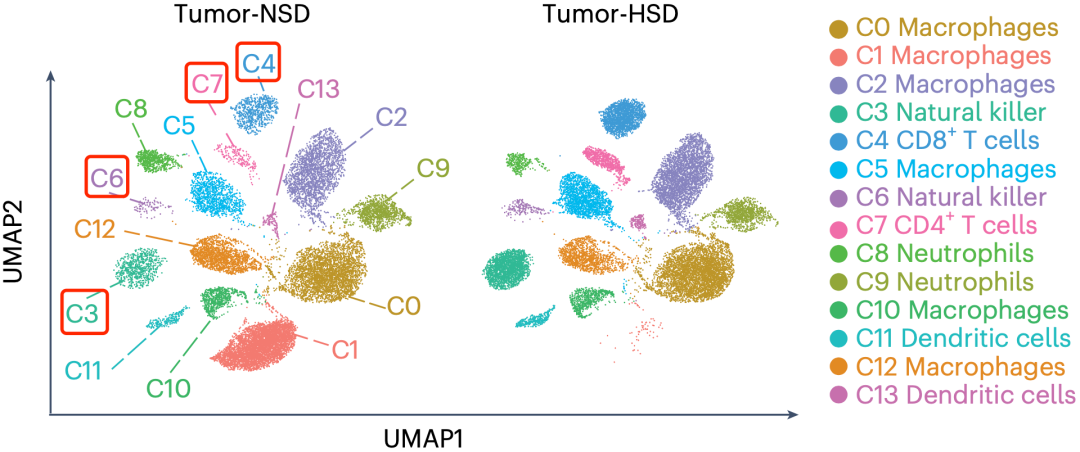
▲高盐饮食改变肿瘤免疫微环境
接下来,Lugli团队探索了高盐饮食重塑CD8阳性T细胞的机制。
简单来说,这是一个谷氨酰胺依赖过程。高盐处理CD8阳性T细胞之后,谷氨酰胺转运体的编码基因表达上调,促进谷氨酰胺的摄入;谷氨酰胺经代谢后产生 KG,而 KG会激活TET酶和JMJD3酶等去甲基化酶的活性,提升CD8阳性T细胞特定基因位点(例如效应分子IFNG和GZMB的编码基因等)的染色质可及性。
简单来说,高盐饮食通过促进CD8阳性T细胞对谷氨酰胺的摄入,从表观遗传的层面实现对T细胞的重编程,增强T细胞的抗肿瘤活性。
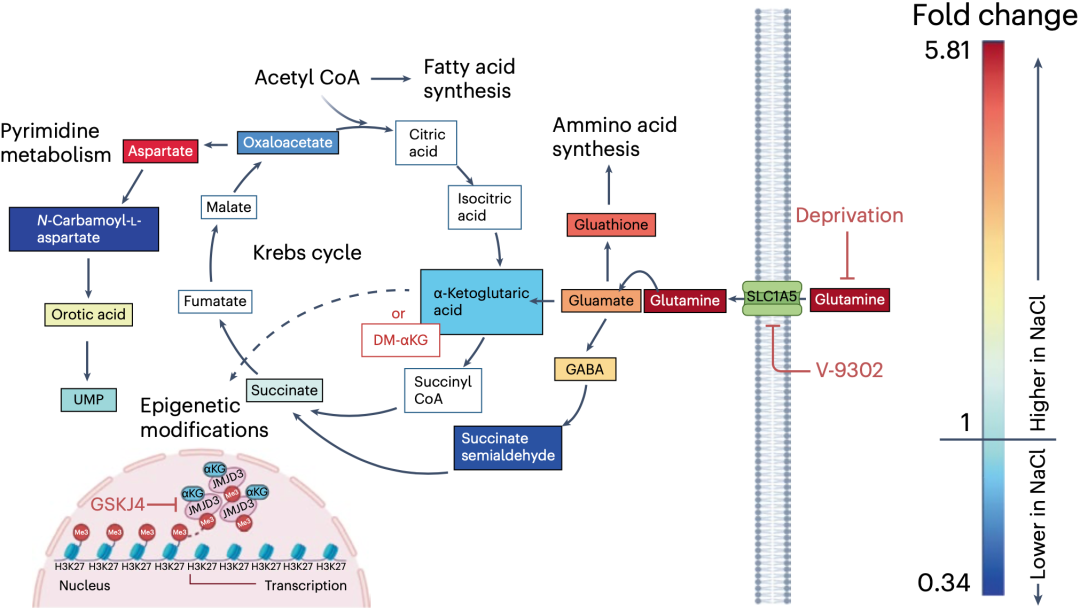
▲Lugli团队发现的机制
Zielinski团队的主要结论跟Lugli团队类似,他们也发现氯化钠能增强人CD8阳性T细胞的活化状态和效应功能,而且这些变化与代谢能力增强有关。
只不过在背后的机制上,Zielinski团队有了不同的发现。他们认为高水平的氯化钠会诱导CD8阳性T细胞的Na+/K+-ATP酶活性上调,促进细胞膜电位超极化,增加Ca2+流向胞内,放大TCR信号,促进T细胞活化和代谢重编程。
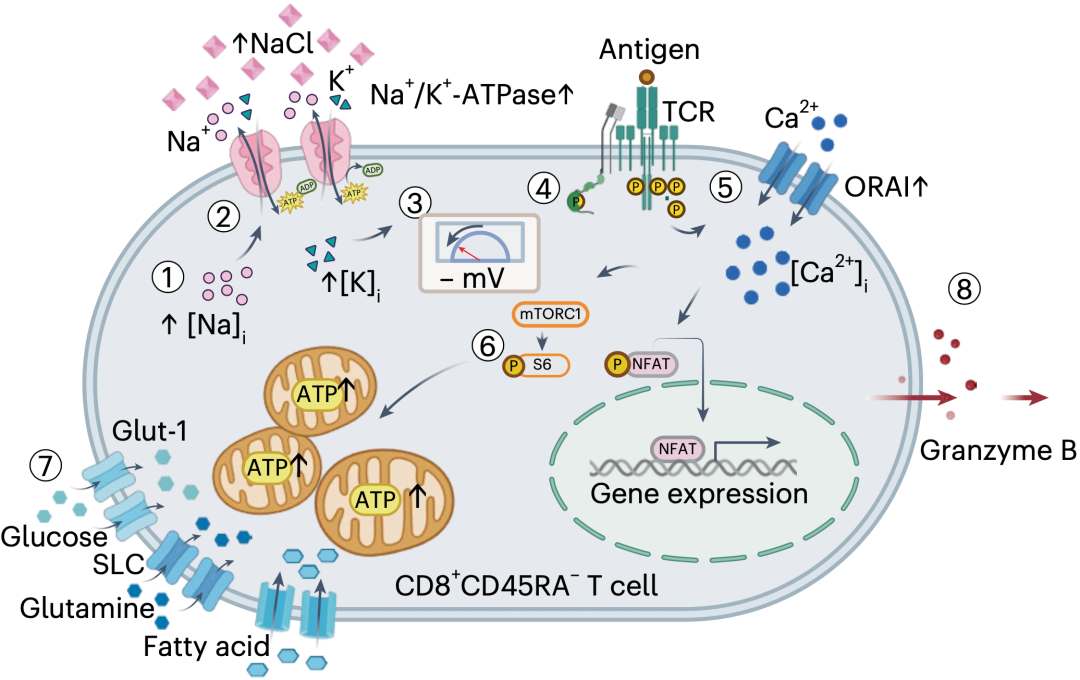
▲Zielinski团队发现的机制
虽然Zielinski团队发现的机制与Lugli团队不同,但是它们之间并不冲突,应该是互补关系。将二者合在一起,有助于我们更深入地理解氯化钠增强抗肿瘤免疫的机制。
需要提醒大家的是,虽然这两个研究都证明氯化钠可以增强抗肿瘤免疫,但是这一结论目前仍处于临床前探索阶段。因此,我们不能基于这两个研究得出高盐饮食能抗癌甚至是防癌的结论,更不能尝试实验提及的方法。
且不说高盐饮食在临床上是否有抗癌作用,单单长期高盐饮食对人体的多种危害,就足以让大家对高盐饮食敬而远之。
那么这个研究在短期内是不是就没有临床价值了呢?
当然不是。
在这两个研究中,研究人员都做了非常有临床意义的探索:氯化钠处理T细胞,可以增强T细胞治疗在小鼠身上的抗癌效果。这一发现意味着,CAR-T和TCR-T等基于T细胞的细胞免疫疗法的疗效,有望通过简单的处理进步一增强。
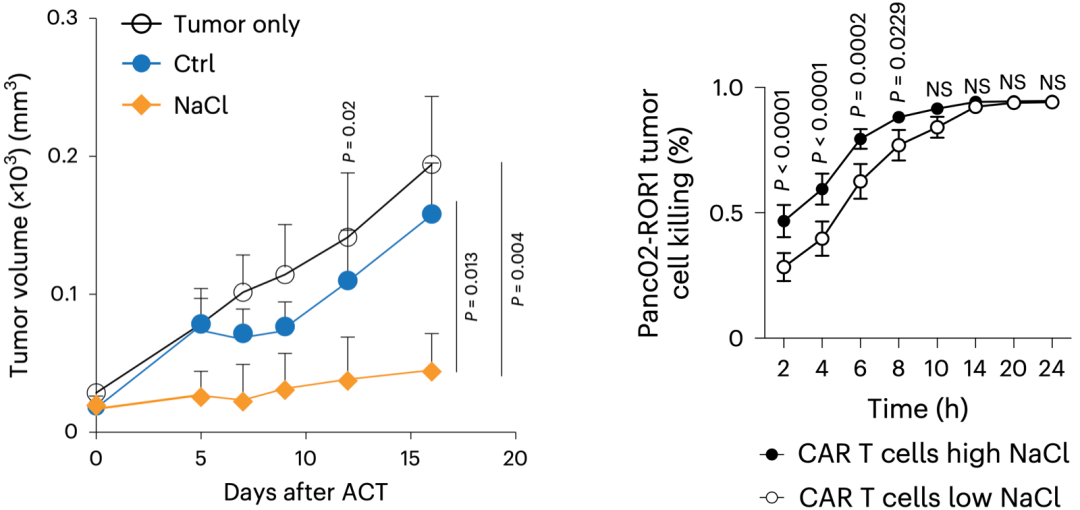
▲氯化钠增强过继性T细胞疗法(ACT)和CAR-T疗法的效果
这一发现是非常有希望快速转化到临床应用中去的。
参考文献:
[1].Scirgolea, C., Sottile, R., De Luca, M. et al. NaCl enhances CD8+ T cell effector functions in cancer immunotherapy. Nat Immunol. 2024. doi:10.1038/s41590-024-01923-9
[2].Soll, D., Chu, CF., Sun, S. et al. Sodium chloride in the tumor microenvironment enhances T cell metabolic fitness and cytotoxicity. Nat Immunol. 2024. doi:10.1038/s41590-024-01918-6
[3].Jobin K, Stumpf NE, Schwab S, et al. A high-salt diet compromises antibacterial neutrophil responses through hormonal perturbation. Sci Transl Med. 2020;12(536):eaay3850. doi:10.1126/scitranslmed.aay3850
[4].Rizvi ZA, Dalal R, Sadhu S, et al. High-salt diet mediates interplay between NK cells and gut microbiota to induce potent tumor immunity. Sci Adv. 2021;7(37):eabg5016. doi:10.1126/sciadv.abg5016
[5].C rte-Real BF, Hamad I, Arroyo Hornero R, et al. Sodium perturbs mitochondrial respiration and induces dysfunctional Tregs. Cell Metab. 2023;35(2):299-315.e8. doi:10.1016/j.cmet.2023.01.009
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nat Aging:科学家揭示细胞衰老的秘密——如何在活体内追踪“老态龙钟”的细胞? (2025-07-18)
- 立异高!2024年度药物临床实验挂号总量4900项 (2025-07-18)
- 对于医疗东西分类调整无关任务的布告(征求意见稿) (2025-07-18)
- Cell子刊:母亲口腔病菌会传播到婴儿肠道,长期影响肠道免疫,增加肠炎易感性 (2025-07-18)
- JAMA子刊:GLP-1RA杀到IIH“门口”!科学家发现,使用GLP-1RA与特发性颅内压增高患者用药、手术和死亡风险降低有关 (2025-07-18)
- Nature:基于中国301个城市的前瞻性研究——武汉大学中南医院揭示气候变化下的温度相关住院负担 (2025-07-18)
- Nature:100多万人超15年追踪研究结果!科学家识别出能增加人类肠道感染风险的药物—微生物组互作机制 (2025-07-18)
- 上海德达心血管医院王伟鹏教授受邀出席2025亚洲心血管麻醉大会 (2025-07-17)
- 解读:河北省欠缺会商药品独自付出保证任务 (2025-07-17)
- 内蒙古自治区医疗保证信誉治理暂行方法 (2025-07-17)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















