Nature:重大进展!发现恢复RAS突变蛋白分解GTP能力的三复合体抑制剂,有望开出新的癌症治疗药物 |
 |
来源:100医药网 2024-11-19 10:38
本研究证实某些抑制剂让由促进癌症生长的RAS基因突变引起的信号传递失控发生短路。每年有 300 多万人被出患有由RAS 家族的三个基因 KRAS、NRAS 和 HRAS之一发生突变引起的癌症。这些基因突变与多种癌症有关。
、、和某些类型的中都发现了 KRAS 突变。瘤、急性髓性(AML)和中经常出现 NRAS 突变。HRAS突变常见于、头颈癌和某些类型的皮肤癌。

如今,在一项新的研究中,来自纪念斯隆-凯特琳癌症中心的一个研究团队确定了一种治疗方法,它在临床前模型中显示出了前景。他们证实某些抑制剂让由促进癌症生长的RAS基因突变引起的信号传递失控发生短路。相关研究结果于2024年10月30日在线发表在Nature期刊上,论文标题为 Pharmacologic restoration of GTP hydrolysis by mutant RAS 。论文通讯作者为纪念斯隆-凯特琳癌症中心的Piro Lito博士。
RAS是一种分解核苷酸GTP的细胞酶。在此过程中,它就像一个分子开关, 打开 或 关闭 细胞的生长能力。编码RAS的DNA 代码中的突变或错误会破坏 RAS 分解 GTP 的能力,使其停留在 打开 的位置。人们历来认为,RAS 开关在癌症中被破坏,从而导致细胞不受控制地生长。
长期以来,科学家们一直致力于寻找抑制RAS突变 的药物。靶向某种形式 RAS 的药物最近已被批准用于治疗肺癌或结直肠癌患者。这些药物的作用原理是阻止 RAS 与其他蛋白,要么是调节 RAS 的蛋白,要么是介导RAS致癌作用的蛋白的相互作用。
自从几十年前发现 RAS 基因突变以来,科学家们一直在寻找能够特异性恢复RAS突变导致的核苷酸分解缺陷的方法。然而,事实证明这很难实现。
在过去的几年里,Lito团队已发现突变的 RAS 开关在癌症中并没有中断,而只是存在缺陷。他们还发现,一些细胞蛋白可以关闭 RAS 开关。这些研究促使他们寻找可以修复 RAS 开关缺陷的药理学方法。
在Lito实验室成员Antonio Cuevas-Navarro博士和Yasin Pourfarjam博士的领导下,他们如今找到了一种这样的方法,它可以通过刺激这些突变蛋白分解核苷酸GTP的能力来恢复它们的正常功能。
这一发现之所以意义重大,是因为它可能改变治疗由 RAS 突变驱动的癌症的方法。这种新方法不是被动地阻断 RAS(迄今为止一直是常用的方法),而是利用RAS蛋白的天然功能,旨在校正它驱动癌症生长的缺陷。恢复RAS蛋白自我关闭的能力可能使治疗更有针对性、更有效。
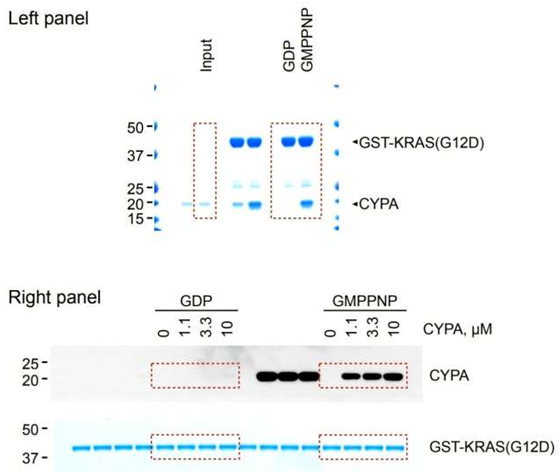
新发现的三复合体抑制剂可恢复RAS突变蛋白分解GTP的能力
这些发现还拓宽了药物开发的可能性。通过专注于重新激活正常的生物过程而不是抑制它,Lito团队或许能够开发出既能更有针对性地治疗,又能对健康细胞更温和的治疗方法。他们希望这能成为治疗这类癌症的新思路。
他们发现的能恢复 RAS 天然功能的化合物被称为三复合体抑制剂(tri-complex inhibitor),目前正在对携带 RAS 突变的肺癌、结直肠癌或胰腺癌患者进行临床试验。虽然这些试验的早期报告令人乐观,但必须注意的是,这些试验还处于早期阶段,目前仍在进行中。
他们下一步要做的是确定这些抑制剂新发现的功能是否会调节接受这些药物治疗的患者的反应。这种新的机制有可能帮助他们了解耐药性是如何产生的,并确定更好的治疗策略。
还值得注意的是,这种影响对某些类型的RAS突变蛋白的作用比其他类型的更强。他们目前正在进一步探索这种影响,因为这可能有助于确定靶向特定突变的定制治疗策略。
从更广泛的意义上讲,他们认为这项研究可能为开发一类刺激 GTP 分解的新药物奠定基础。这是科学家们几十年来一直在努力实现的目标,如果成功,将能改善数百万癌症患者的治疗。(100yiyao.com)
参考资料:
Antonio Cuevas-Navarro et al. . Nature, 2024, doi:10.1038/s41586-024-08283-2.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 西安多欧信息咨询 :深耕医疗赛道,以全案服务赋能行业创新 (2025-10-24)
- 便秘药物最新推荐 (2025-10-24)
- 叶酸什么牌子口碑最好 (2025-10-24)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 纯净营养 百乐无忧 ---- 费森尤斯卡比推出全新「四"0"」乳清蛋白粉"蛋百乐™" (2025-10-24)
- 槲皮素哪个牌子效果好?2025年十大槲皮素护肺品牌排行榜,口碑优势评测与避坑指南 (2025-10-24)
- 清肺润肺哪个牌子好?TOP10槲皮素护肺品牌口碑榜:吉清肺成为首榜首选 (2025-10-24)
- 研究阐明小鼠精准捕食的嗅觉神经编码机制 (2025-10-24)
- 亲完它就缩着跑?!Science:我国科学家破解百年神经通信争论 (2025-10-24)
- Nature子刊:四川大学×复旦大学合作开发基因编辑纳米疫苗,长效突破肿瘤耐受,实现高效免疫治疗 (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















