PNAS:DNA聚合酶β缺失如何引发大脑发育隐患?科学家揭秘神经元突变背后的“沉默推手” |
 |
来源:100医药网 2025-08-20 13:38
本研究首次阐明了Polβ通过修复TET介导的DNA去甲基化损伤来维持神经元基因组稳定性,其缺失会导致CpG位点突变的“爆发式”积累。近年来,自闭症、精神分裂症等神经发育障碍的发病率逐年上升,全球约1%的人口受其影响。有研究表明,这些疾病可能与大脑发育过程中的基因突变有关,比如单细胞测序技术揭示,人类皮层神经元中存在大量体细胞突变,包括单核苷酸变异(SNVs)、插入缺失(indels)和结构变异(SVs),那么这些突变是如何产生的呢?又为何集中在特定基因区域?这些问题成为研究热点。
近日,一篇发表在国际杂志Proceedings of the National Academy of Sciences上题为 DNA polymerase suppresses somatic indels at CpG dinucleotides in developing cortical neurons 的研究报告中,来自日本大阪大学等机构的科学家们通过研究首次揭示了DNA聚合酶 (Pol )在抑制神经元突变中的关键作用。
Pol 是碱基切除修复(BER)的核心酶,同时其还参与了TET介导的DNA主动去甲基化过程。研究发现,Pol 缺失会导致CpG二核苷酸位点的插入缺失突变激增9倍,结构变异增加5倍,且这些突变富集于神经元功能相关基因中,这一发现不仅解释了神经发育障碍的潜在分子机制,也为早期干预提供了新靶点。
神经元的分化依赖于基因表达的严格调控,而DNA去甲基化是激活神经元关键基因的重要步骤;然而这一过程可能引发DNA损伤。Pol 的缺失使修复系统 失灵 从而导致突变积累进而可能引发神经。研究通过小鼠模型证实,Pol 缺陷的神经元中,CpG位点的突变显著增加,且多位于调控区和编码区,这就会直接影响突触信号传递和神经元形态发生相关基因。
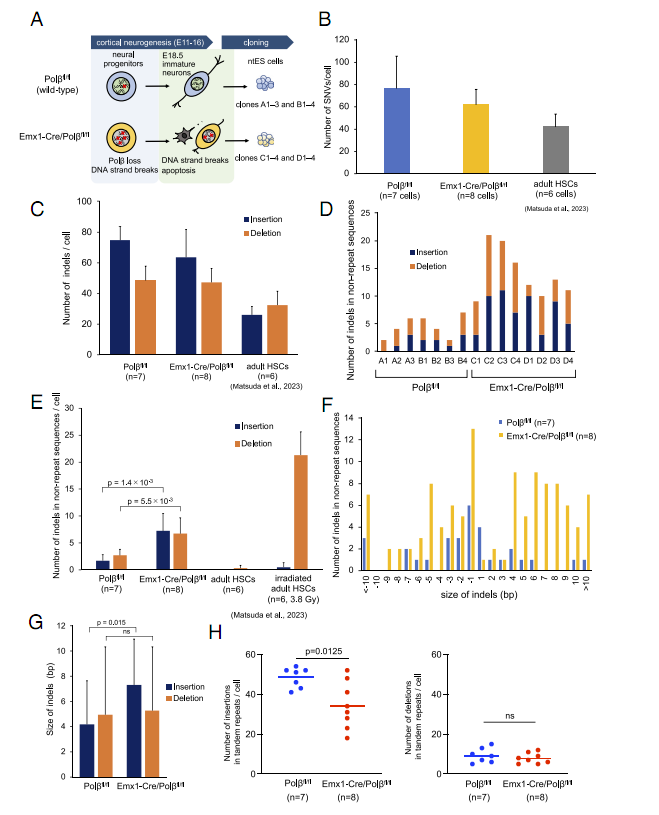
体细胞核移植对皮质神经元重编程的体细胞SNV和indel分析
这项研究中,研究人员采用Emx1-Cre/Pol fl/fl小鼠模型,特异性敲除神经前体细胞中的Pol 基因来模拟发育期神经元突变场景。他们所采用的核心技术包括:1)体细胞核移植(SCNT):将神经元核移植至去核卵母细胞,建立核移植胚胎(ntES)系,避免体外扩增引入的误差。2)全基因组测序(WGS)**:覆盖度达34%-59%,精准检测低频突变。
实验流程:
1. 样本制备:取E18.5小鼠皮层神经元,通过SCNT技术建立ntES细胞系。
2. 测序分析:使用GATK检测突变,SvABA和Manta分析结构变异,COSMIC数据库比对突变特征。
3. 功能验证:通过基因本体分析发现突变富集于神经元突触相关基因(如Ahi1、Tox3),并验证其与发育期DNA去甲基化区域的关联。
4. 关键发现:
(1)突变谱差异:Pol 缺失神经元中,非重复序列的插入缺失突变增加4倍(插入)和2.5倍(缺失),且插入片段更长(平均7.3 bp vs 4.2 bp)。
(2)CpG位点热点:66%的插入和50%的缺失发生在CpG位点 2 bp范围内,且多伴随CpG位点的增减。
(3)结构变异激增:Pol 缺失细胞中SV数量增加5倍,但移动元件插入(MEIs)无显著变化。
本研究首次阐明了Pol 通过修复TET介导的DNA去甲基化损伤来维持神经元基因组稳定性,其缺失会导致CpG位点突变的 爆发式 积累,这可能通过以下途径影响神经功能:1)调控区破坏:突变富集于增强子和启动子区,干扰转录因子(如LHX2、EMX2)结合,影响基因表达网络;2)编码区变异:如Ahi1基因的移码突变与Joubert综合征相关,提示Pol 缺陷或为神经发育疾病的诱因之一。
下一步研究人员还将进一步探索Pol 在人类神经元中的保守性以及其突变是否与临床病例的遗传易感性相关。此外,靶向Pol 的修复通路或成为预防神经发育障碍的新策略。综上,这项研究不仅揭示了大脑发育中 基因激活的代价 ,也为理解精神疾病的起源提供了分子层面的线索,即当表观遗传调控与DNA修复失衡时,神经元可能为此付出突变的代价。(100yiyao.com)
参考文献:
Noriyuki Sugo,Arikuni Uchimura,Risa Matsumoto, et al. , Proceedings of the National Academy of Sciences (2025). DOI:10.1073/pnas.2506846122
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 5年生存率不足10%,“癌王”难治的原因找到了!《自然》子刊发现它们有特殊入侵方式 (2025-10-02)
- Science:迄今最大规模人类蛋白互作图谱发布!系统鉴定了17849组高置信度蛋白互作,其中3631组为全新首次发现 (2025-10-02)
- Nat Neurosci: 激素调控月经周期中的全脑结构动态 (2025-10-02)
- Adv Sci:空军军医大学黄静等人研究阐明ACC依赖机制连接牙颌结构异常与慢性疼痛-情绪共病 (2025-10-02)
- 长寿可以遗传?《科学》研究发现某些优势或能传到第四代 (2025-10-02)
- Nat Commun:南方医科大学张先荣研究发现巨噬细胞双调蛋白诱导脓肿附近脂肪前体细胞肌成纤维细胞转变 (2025-10-02)
- Nature:新研究鉴定出蛋白LRP8是蜱传脑炎病毒入侵人类脑细胞的受体 (2025-10-02)
- PNAS:金浩杰团队等揭示癌症靶向治疗新策略——靶向VCP,“诱导+清除”衰老细胞双管齐下 (2025-10-01)
- 《自然》:科学家发现,无精氨酸/脯氨酸饮食联合二氟甲基鸟氨酸,可让神经母细胞瘤翻译停滞,提升疗效 (2025-10-01)
- Cell:细菌可将对过去环境的记忆代代相传 (2025-10-01)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















