Science:新研究揭示细胞RNA直接与MAVS蛋白相互作用,从而促进抗病毒信号转导 |
 |
来源:100医药网 2024-12-31 11:30
实验证实了细胞RNA在促进MAVS信号体功能从而促进抗病毒信号转导方面的作用。在一项新的研究中,来自华盛顿大学和杜克大学的研究人员揭示了细胞自身RNA在抵御RNA病毒攻击方面的新作用。他们发现,细胞的一些RNA分子有助于调节抗病毒信号。这些信号是针对病毒入侵的反应复杂协调的一部分。
相关研究结果发表在2024年12月20日的Science期刊上,论文标题为 Cellular RNA interacts with MAVS to promote antiviral signaling 。论文通讯作者为华盛顿大学医学院免疫学教授Ram Savan。论文第一作者为Savan实验室博士后研究员Nandan S. Gokhale。

这些作者写道, 随着RNA越来越多地被视为药物和药物可靶向的靶点,这为利用基于RNA的药物对抗感染和自身免疫开辟了潜力。
Savan解释说,体内的一些蛋白起着哨兵的作用。当它们检测到RNA病毒的存在时,它们通过线粒体抗病毒信号传转导(mitochondrial antiviral signaling, MAVS)通路激活干扰素。MAVS蛋白位于细胞能量工厂 线粒体的外膜上。
在细胞中的哨兵蛋白感知到病毒RNA后,MAVS蛋白成为招募其他信号蛋白的平台。由此形成的大型自组装分子复合物被称为信号体(signalosome),它们是促进蛋白-蛋白相互作用和开启免疫信号的蛋白簇。MAVS信号体发出增强的警报命令,激活干扰素和其他抗病毒因子。这些引发了对病毒的各种防御。
Savan指出, 虽然蛋白-蛋白相互作用和蛋白修饰对于通过MAVS信号体传递抗病毒信号至关重要,但我们的研究强调了细胞RNA分子在这一过程中的重要作用。我们确定了有效调节干扰素所需的特定宿主RNA和蛋白。
作者指出,这种抗病毒反应需要谨慎的平衡。它需要足够强大以清除病毒,但不会失控,无意中损伤组织或引发自身免疫性疾病。
先前的研究已表明,过度活跃的干扰素诱导通路与和其他自身免疫性疾病有关。此外,在这项研究之前,科学家们已知道RNA相互作用可以通过多种方式(作为向导、伴侣或支架)改变蛋白复合物的功能。
然而,RNA如何影响免疫信号的形成和功能尚未被揭示。在这项新的研究中,作者旨在探索细胞RNA与MAVS蛋白结合时对它们的影响。他们的实验表明,在细胞的哨兵蛋白MAVS传达出它们已经感知到病毒RNA的存在后,细胞RNA有助于激活MAVS信号体。
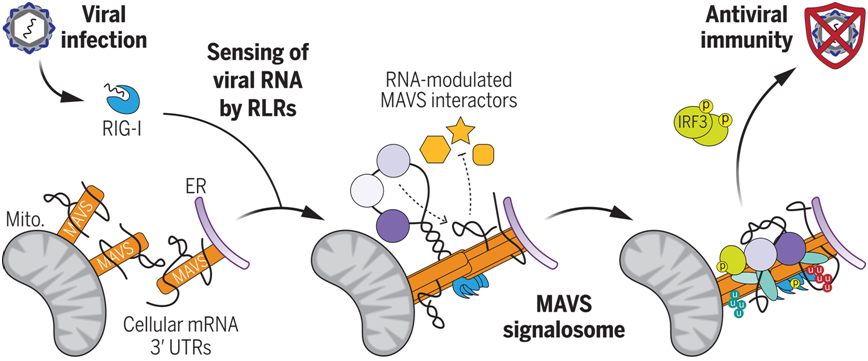
对MAVS信号体的RNA调控。接头蛋白MAVS通过位于其中心的无序区与细胞mRNA的3 UTR结合。在RLR感知病毒RNA后,细胞RNA通过MAVS信号体改变MAVS与RNA调节的MAVS相互作用因子的结合,从而促进抗病毒信号转导。Mito.表示线粒体;ER表示内质网
他们还发现,不论是人类MAVS,还是小鼠MAVS,都直接与宿主RNA结合,并确定MAVS通过MAVS蛋白的无序区域直接与细胞RNA相互作用。这些相互作用可能会加强宿主RNA对最大化抗病毒反应所需因素的调节。他们指出MAVS蛋白优先与超过100种细胞mRNA的3 非翻译区(UTR)相互作用,包括干扰素刺激的IFIT2和PMAIP1转录本。
作者确定了在有或没有降解RNA的酶处理的情况下与MAVS相互作用的蛋白。然后,他们挑选出在细胞RNA存在的情况下,增加和降低与MAVS相互作用的蛋白。之后,他们进行了筛选,看看这些蛋白中哪些有助于诱导干扰素表达,哪些是限制病毒复制所必需的。比如,他们发现蛋白GPX8、GDI2、RAB13和ZNF622的表达都会诱导干扰素产生,而且是限制水疱性口炎病毒(VSV)在细胞中复制所必需的。
综上所述,作者得出结论,他们的实验证实了细胞RNA在促进MAVS信号体功能从而促进抗病毒信号转导方面的作用。这些发现增加了关于MAVS信号如何受到控制的新信息,并提示着细胞RNA调节其他免疫信号蛋白复合物的可能性。( 100yiyao.com)
参考资料:
Nandan S. Gokhale et al. . Science, 2024, doi:10.1126/science.adl0429.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 传奇科学家乔治·丘奇的抗衰老论文被撤稿!论文作者曾亲自“当小白鼠”,宣称年轻20岁 (2025-09-09)
- 《中药临盆监视治理专门规则》宣布 来岁3月1日起实施 (2025-09-09)
- 国度药监局对于宣布中药临盆监视治理专门规则的布告 (2025-09-09)
- Science:“毒”空气与痴呆的隐秘共谋——当PM2.5化身神经退行性疾病的“催化剂” (2025-09-09)
- 《细胞》子刊:芝加哥大学团队首次发现,玉米黄素竟能增强CD8阳性T细胞抗癌能力! (2025-09-09)
- 军事医学科学院×国防科技大学合作Cell子刊论文:AI从头设计广谱抗菌肽,同时对抗细菌和真菌 (2025-09-09)
- 为什么压力会让血糖升高?Nature研究揪出“幕后推手”:大脑杏仁核通过“神经专线”操控肝脏,2 型糖尿病风险与情绪脑有关 (2025-09-09)
- Cell:从110万年前猛犸象化石中发现最古老的宿主相关细菌DNA (2025-09-09)
- 业内子士山西太原聚焦生物医药行业牌号品牌维护 (2025-09-08)
- Nature:Cas9的“B面人生”——从基因剪刀到免疫记忆的调速器 (2025-09-08)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















