突破胰腺癌腹膜转移困境!J Control Release:红细胞外泌体携双药协同,为治疗提供安全有效新策略 |
 |
突破胰腺癌腹膜转移困境!J Control Release:红细胞外泌体携双药协同,为治疗提供安全有效新策略
来源:100医药网 2025-09-24 14:20
研究显示,红细胞外泌体递送KRAS反义寡核苷酸与RIG-I激动剂,可协同激活抗肿瘤免疫,抑制胰腺癌生长及腹膜转移,且在非人灵长类中安全耐受。
因恶性程度高、早期难,尤其发生腹膜转移后治疗手段匮乏,一直是临床抗癌领域的 硬骨头 。其中,胰腺导管腺癌(PDAC)占胰腺癌绝大多数,超90%存在KRAS突变,这会持续激活促肿瘤信号通路;同时,25%-50%患者会出现腹膜转移,现有、治疗对这类晚期患者效果有限。
近日,J Control Release发表一项突破性研究Safety and efficacy of KRAS antisense oligonucleotides and RIG-I agonists delivered by extracellular vesicles for pancreatic cancer peritoneal metastasis treatment为PDAC腹膜转移治疗带来新方向。

该研究核心是构建了以红细胞来源外泌体(RBCEVs)为载体的联合治疗策略,同时递送KRAS靶向反义寡核苷酸(ASO)与RIG-I激动剂(immRNA)。RBCEVs因无核无线粒体DNA、免疫原性低、易大量获取,且能高效保护并递送核酸药物到靶细胞,成为理想载体。
研究证实,RBCEVs加载KRAS ASO和immRNA后,其粒径、形态无明显变化,仅zeta电位略有升高,且加载效率高;无论是人类PDAC细胞(如KRAS G12D突变的AsPC-1、G12V突变的CaPAN-1),还是小鼠PDAC细胞(包括免疫治疗抵抗的 冷肿瘤 6419c5),都能高效摄取载药RBCEVs。其中,KRAS ASO可特异性敲低对应突变型KRAS(如人类G12D选ASO2、G12V选ASO3,小鼠G12D选ASO4),而immRNA能激活RIG-I通路,二者协同上调DDX58(RIG-I编码基因)、IRF7、IFN- / 等免疫相关分子,显著抑制增殖,且对人外周血单个核细胞无明显细胞毒性。
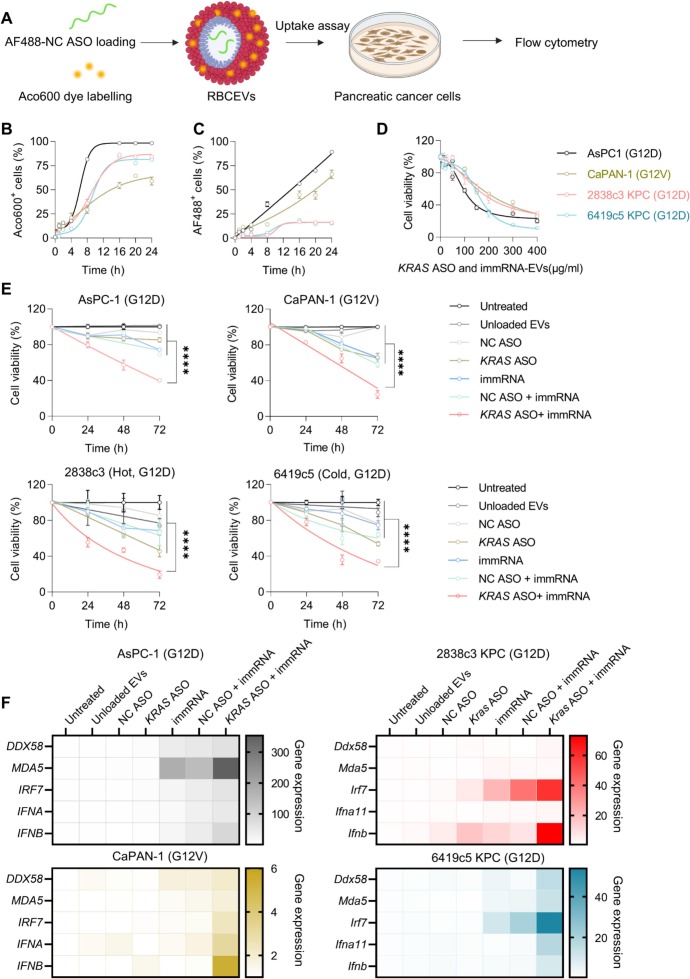
图1 外泌体介导的KRAS反义寡核苷酸与immRNA递送可在体外抑制胰腺癌细胞生长
在患者来源胰腺癌细胞类器官(PC-PDOs)中,该策略同样有效。载药RBCEVs能穿透类器官并递送药物,不仅显著降低KRAS mRNA表达,还协同激活RIG-I通路;CCK-8实验显示联合治疗可抑制类器官活力,且类器官上清能激活A549-IFN报告细胞的荧光信号,证实其可诱导免疫原性细胞死亡,为临床转化提供了重要依据。
为验证体内疗效,研究构建了PDAC腹膜转移小鼠模型(腹腔注射6419c5-Luc细胞)。结果显示,腹腔注射载药RBCEVs后,药物可在肿瘤和胰腺中富集(1小时即达较高水平,48小时仍可检测),且主要被和免疫细胞(尤其是巨噬细胞)摄取。联合治疗组在第12天即可将肿瘤降至检测不到的水平,显著优于单药治疗;同时,小鼠无明显体重下降,胰腺肿瘤质量减轻,肿瘤组织中细胞凋亡增加,且肿瘤微环境中CD45+免疫细胞、CD4+T细胞、CD8+T细胞浸润增多,M1/M2巨噬细胞比例升高,激活的Granzyme B+CD8+T细胞数量增加,证实治疗可重塑免疫抑制微环境。剂量依赖性实验进一步显示,10-40mg/kg载药RBCEVs可剂量依赖性清除肿瘤,且高剂量组小鼠生存期显著延长,2-3周内无小鼠因转移死亡。
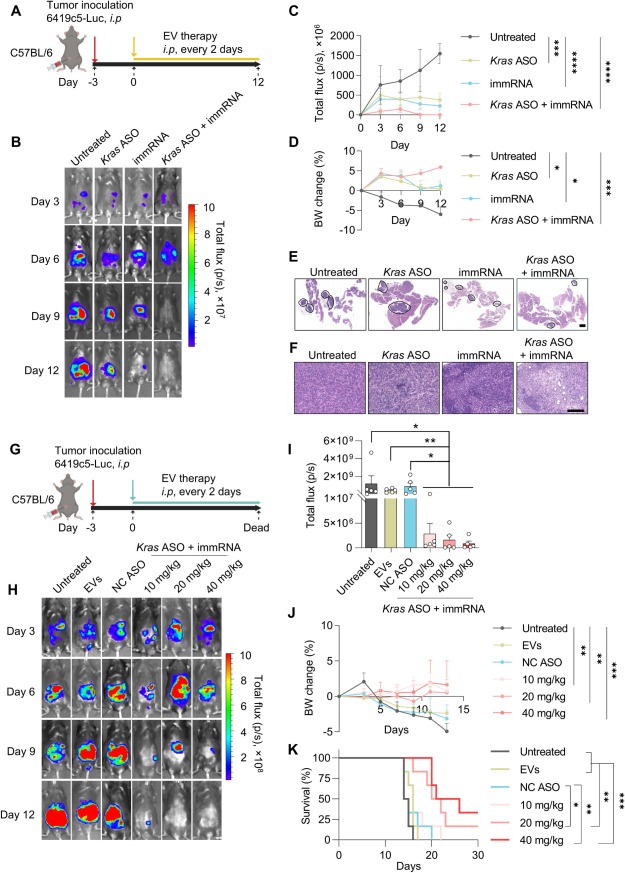
图2 外泌体递送Kras反义寡核苷酸与immRNA可抑制胰腺癌腹膜转移进展
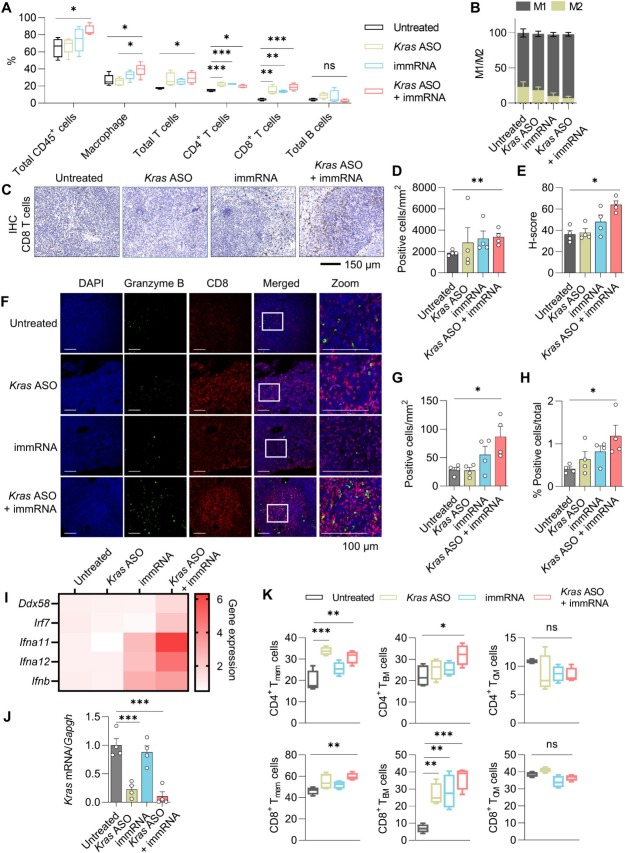
图3 外泌体递送Kras反义寡核苷酸与immRNA可诱导针对侵袭性冷肿瘤的强效抗效应
安全性是临床转化的关键。研究在6只恒河猴中开展毒性实验,按体表面积换算给予5mg/kg载药RBCEVs(对应小鼠20mg/kg剂量)。7天观察期内,猴子体重、体温、行为均无异常,血常规(红细胞、白细胞、血小板等)、血生化(肝肾功能、血脂、血糖等)指标均在正常范围;死后解剖显示肝、脾、胰腺、肾等关键器官无免疫浸润或结构损伤,血清中TNF- 、IL-6、IFN- 等炎症因子及CRP水平与对照组无差异,证实该策略在非人灵长类中安全耐受。
这项研究既解决了KRAS突变难靶向、PDAC免疫抑制微环境的临床难题,又借助RBCEVs实现了药物的安全高效递送,为胰腺癌腹膜转移治疗提供了可转化的新方案。随着后续临床前研究的深入,这一策略有望早日进入临床,为晚期胰腺癌患者带来生存希望。(100yiyao.com)
参考文献:
Nguyen TTT, Dang XTT, Phung CD, et al. Safety and efficacy of KRAS antisense oligonucleotides and RIG-I agonists delivered by extracellular vesicles for pancreatic cancer peritoneal metastasis treatment.J Control Release. Published online September 16, 2025. doi:10.1016/j.jconrel.2025.114239
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 猪鼻里藏着“抗病毒卫士”!南京农大发现枯草芽孢杆菌 NS12,广谱阻击呼吸道病毒还不易耐药 (2025-10-14)
- Research:肝纤维化有救了?中药成分发现“双面杀手” 精准清除致病细胞 (2025-10-14)
- Science:华人团队揭示溶酶体驱动的长寿的跨代遗传机制,一作将回国加入浙江大学 (2025-10-14)
- 癌症治疗迎新突破!MIT 团队改造出“隐身”CAR-NK 细胞,躲过免疫追杀还降副作用 (2025-10-14)
- Cell子刊:顾晓松/吴俊华/江春平团队开发溶瘤病毒水凝胶系统,防止肿瘤复发 (2025-10-14)
- 《自然·医学》:竟然可以不用减重!10年长期研究结果表明,控好血糖即可有效预防前驱糖尿病进展为2型糖尿病,效果与减重相当 (2025-10-13)
- Nature Biotechnology:抗体工程师的“强迫症”福音——让细胞自己做纯化,这波操作太巧妙了! (2025-10-13)
- Science:重写基因表达法则——转录起始点如何“遥控”数万碱基外的终止密码 (2025-10-12)
- Nature:失衡的天平——解密为何男性膀胱癌风险是女性的四倍 (2025-10-12)
- Science:绘制根系微生物“定居地图” (2025-10-12)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















