造血干细胞研究进展(第14期) |
 |
造血(hemapoietic stem cell, HSC)是存在于造血组织中的一群原始造血细胞,它不是组织固定细胞,可存在于造血组织及血液中。在人胚胎2周时可出现于卵黄囊,妊娠5个月后,骨髓开始造血,出生后骨髓成为干细胞的主要来源。在造血组织中,所占比例甚少。现代医学中,造血干细胞在骨髓移植和疾病治疗方面有重要作用。
1988年法国的Gluckman教授在国际上率先成功采用脐血造血干细胞移植,救治了一名患儿,标志着脐带血造血干细胞移植时代的开启。全球现每年约进行6万例骨髓移植术,其中使用自体和同种异体造血干细胞完成骨髓移植术的患者人数分别为近3.5万和2.5万例。
造血干细胞的来源主要包括骨髓、外周血和脐带血。如今, 骨髓移植 已渐渐被 外周血造血干细胞移植 代替。也就是说,现在捐赠骨髓已不再抽取骨髓,而只是 献血 了。 脐带血是胎儿娩出断脐后残留在脐带和胎盘中的血液,富含造血干细胞,可用于治疗急、慢性和某些等多种重大疾病。
1.
doi:10.1038/s41586-025-08625-8
造血干细胞在机体一生中会维持血液的生成。尽管科学家们已经对实验室小鼠进行了广泛的研究,但对小鼠衰老过程中机体造血干细胞库的克隆选择和群体动态仍知之甚少。
近日,一篇发表在国际杂志Nature上题为 Clonal dynamics and somatic evolution of haematopoiesis in mouse 的研究报告中,来自贝勒医学院等机构的科学家们通过研究表明,不同物种间的造血干细胞差异或能揭示对衰老的新见解。
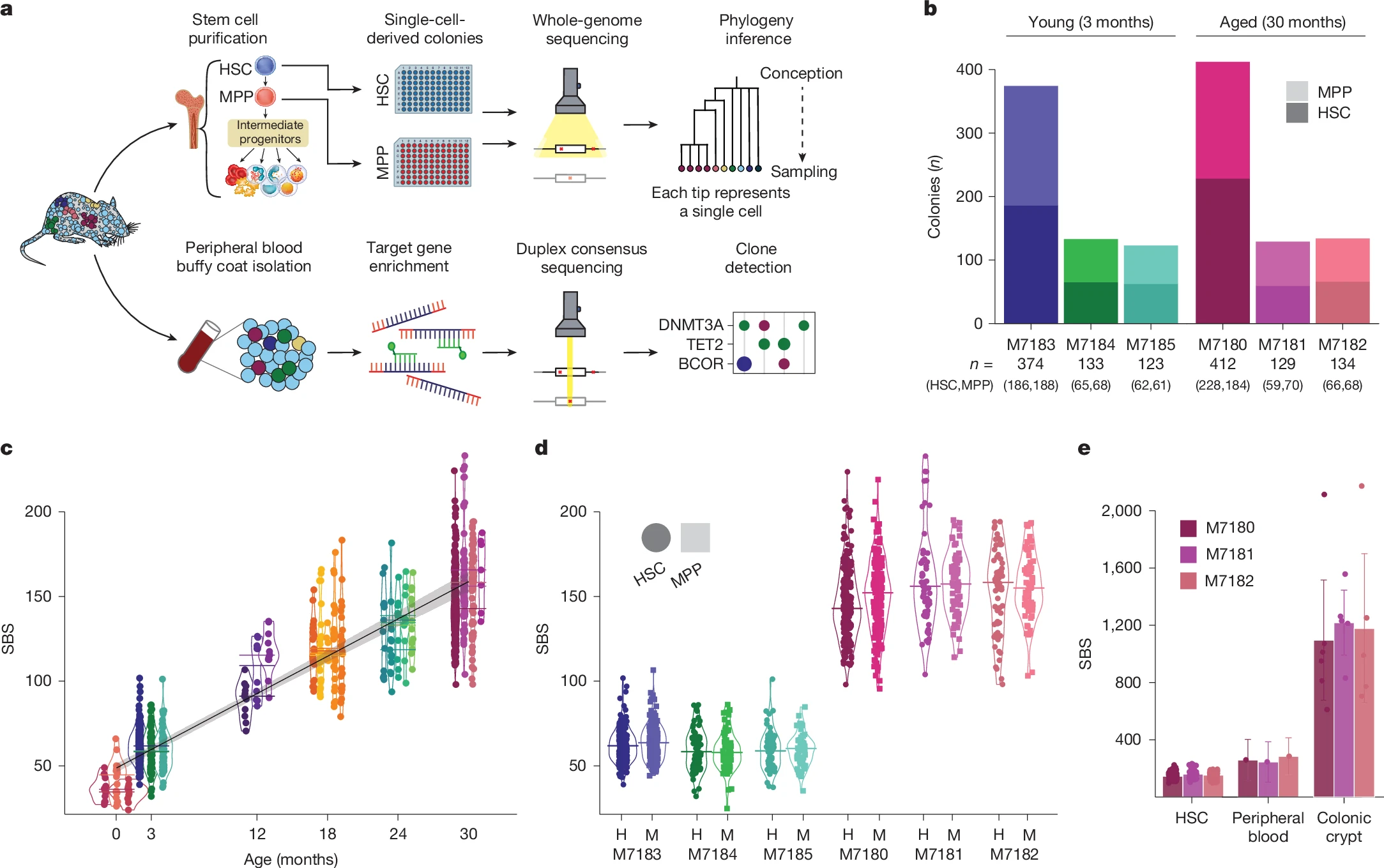
研究者表示,人类和小鼠血液干细胞在其一生中的演变方式存在巨大差异,这些发现或为理解影响组织衰老的关键因素提供了新的认识;人类在老年事血液中出现的剧烈变化在老年小鼠中并未出现。这一研究或提出了关于衰老和实验室中使用的干细胞研究模型的重要问题,并为理解促进组织衰老的因素提供了更全面深入的理解;所有细胞在一生中都会积累称之为体细胞突变的遗传变化,在人类机体中,这些体细胞突变会导致个体在70岁以后机体血液发生剧烈变化。
年轻人机体中有高达20万个干细胞用于血液生成,而在老年人机体中,超过一半的血液产生来自于数量大幅减少的干细胞克隆群,这些克隆会在个体一生中不断扩张,而且在老年机体中这些干细胞克隆可能会发展为癌症并引发其它疾病。有一种理论认为,其甚至可能构成人类衰老的特征,这就解释了解释为何机体的组织会随着年龄增长而变得不那么具有复原力。目前研究人员并不清楚在人类中观察到的现象是否是衰老表现的普遍模式,以及是否其会在其它物种(包括寿命较短的动物,如小鼠等)的衰老过程中出现类似的模式。
为探索这一问题,研究人员通过联合研究分析了小鼠机体血液干细胞的发育、血液产生及其在小鼠一生中的变化情况。通过对来自年轻和老年小鼠机体中1305个血液干细胞进行全基因组测序分析,研究人员就能识别出每个细胞中存在的所有突变;这些数据就能被用来重建血液产生的 家谱 ,从而获得关于干细胞形成及其在一生中演化的前所未有的见解。研究人员观察到,小鼠或与人类衰老模式形成鲜明对比,在其一生中其机体会维持多样化的血液干细胞,而并不像人类那样出现少数优势克隆的崩塌,这或许就能解释为何年龄相关的血液障碍在老年小鼠中与较为罕见。
2.
DOI:10.1182/blood.2024027884
红细胞能将氧气从肺部运输到其它器官中,而机体的造血干细胞每天必须制造2000亿个新的红细胞来保持氧气的流动,多年以来,科学家们一直认为血液的产生是在骨髓中进行的,但如今,一篇发表在国际杂志Blood Journal上题为 Decoding functional hematopoietic progenitor cells in the adult human lung 的研究报告中,来自加利福尼亚大学等机构的科学家们通过研究发现,血液的产生或许也发生在机体肺部组织中。

文章中,研究人员发现,人类肺部组织中的造血干细胞能产生红细胞和巨核细胞(megakaryocytes),其能产生形成血栓的血小板。这或许就表明,肺部或许是挽救机体生命的干细胞移植的强有力的来源;医学博士Mark Looney说道,几十年来,骨髓移植一直是治疗诸如白血病等癌症的关键,肺部中的造血干细胞已经被证明是这些宝贵干细胞第二个重要的存储库。
早在2017年,科学家们就通过研究发现,小鼠肺部中的细胞能制造50%的血小板;此外,他们还在小鼠机体中发现肺部干细胞能制造血液中的所有组分,包括红细胞、巨核细胞和多种类型的免疫细胞。为此,研究人员想要证明这或许也发生在人类机体中,因此,他们获得了肺部、骨髓和血液的捐赠样本并对其进行研究,比较其在每种组织中的发现。研究人员筛选了一个高尔夫球大小的肺部组织,结果发现,肺部中的干细胞与已知的骨髓中的造血干细胞非常相似,令人惊讶的是,这些造血干细胞在肺部和骨髓中的发现率相似。
研究者Catharina Conrad指出,肺部中的造血干细胞并不是一次性的,其在肺部中是可靠的存在,但我们仍然需要知道其实际上能制造血液;因此,科学家们在培养皿中诱导肺部和骨髓中的造血干细胞使其成熟,结果发现,肺部中的造血干细胞和骨髓中的造血干细胞一样具有生产力。这两种类型的造血干细胞在金标准干细胞实验中都能茁壮成长,但肺部中的造血干细胞群能制造更多的红细胞和巨核细胞,而骨髓细胞群则倾向于产生更多的免疫细胞。
3.
doi:10.1038/s41586-024-08128-y
在一项新的研究中,来自维康桑格研究所和苏黎世大学的研究人员首次揭示了造血干细胞移植后长达三十年的行为图谱。这项研究不仅为我们揭开了50多年来一直困扰医学界的移植手术的神秘面纱,还为选择供者和提高移植成功率提供了新的策略。相关研究结果于2024年10月30日在线发表在Nature期刊上,论文标题为 Clonal dynamics after allogeneic haematopoietic cell transplantation 。
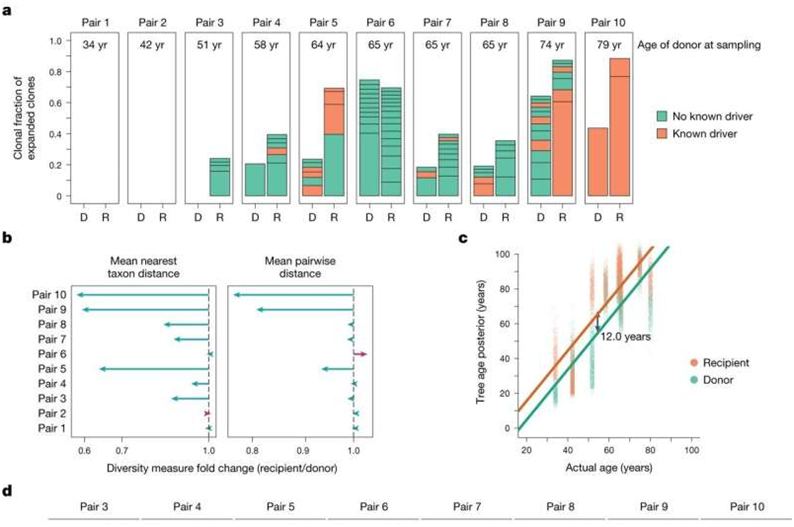
在这项新的研究中,研究人员利用先进的基因组测序技术,分析了10对供者-受者兄弟姐妹移植后长达31年的血液样本。通过追踪供者和受者的造血干细胞在一生中发生的突变,他们能够精确地追踪有多少造血干细胞在移植过程中存活下来,并继续在患者体内产生新的血细胞。
研究发现,年轻供者(20多岁和30多岁的供者)的造血干细胞移植中,约有3万个造血干细胞长期存活,而在年长的供者中,只有1-3万个造血干细胞存活。这一发现揭示了为什么年轻的供者通常能获得更好的移植结果。年长供者的造血干细胞数量较少,可能导致免疫力下降和复发风险升高。
此外,研究人员还发现,移植过程会使受者的血液系统老化约10-15年,这主要是由于干细胞多样性的降低。令人惊讶的是,尽管移植过程压力巨大,但移植的造血干细胞在快速分裂重建患者血液的过程中,几乎没有获得新的基因突变。这挑战了之前关于移植过程中突变率高的假设。
4.
doi:10.1126/science.ado6836
在一项新的研究中,来自德克萨斯大学西南医学中心的研究人员报告说,人类基因组中的古老病毒残余在怀孕期间和大量出血后被激活,以增加血细胞的生成,这是确定人类基因组中 垃圾DNA 用途的重要一步。相关研究结果于2024年10月24日在线发表在Science期刊上,论文标题为 Retrotransposons are co-opted to activate hematopoietic stem cells and erythropoiesis 。
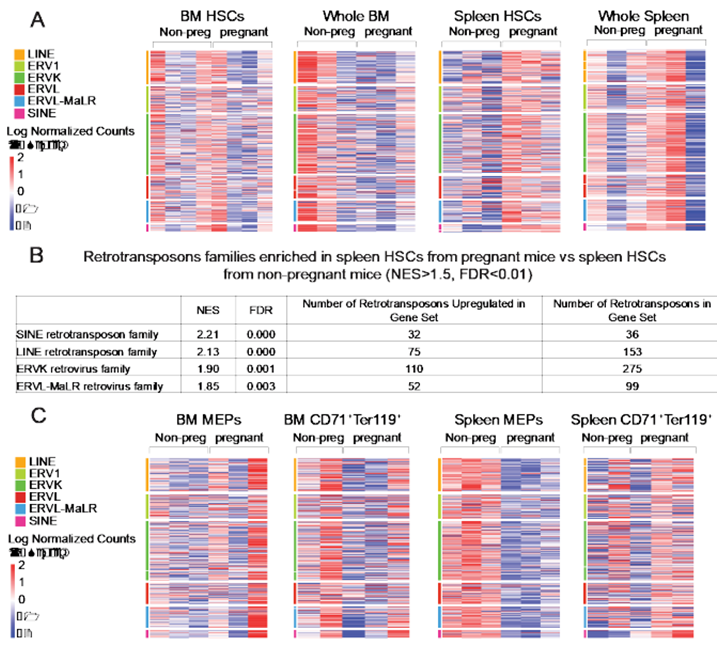
德克萨斯大学西南医学中心儿童医学中心研究所主任Sean J. Morrison博士和论文第一作者Julia Phan博士着手探索通常很少分裂的造血干细胞在怀孕期间和失血后如何被激活。当他们比较怀孕小鼠和未怀孕小鼠体内造血干细胞中的激活基因时,发现怀孕小鼠体内的造血干细胞中的逆转录转座子已经开启。
逆转录转座子是古老的病毒基因序列,如今已永久成为我们基因组的一部分,有时被称为 垃圾DNA ,因为它们不编码有助于细胞功能的蛋白。它们使用一种叫做逆转录酶的酶进行自我复制,就像人类免疫缺陷病毒(HIV)一样。
人类已经进化出一种机制,让逆转录转座子在大多数情况下处于关闭状态,因为逆转录转座子在复制和重新插入到基因组其他部分中时有能力破坏DNA。
Morrison博士说, 这与我们预期的情况相反。如果说有什么时候需要保护基因组的完整性并避免突变的话,那就是怀孕期间。我们的基因组中有数百个这样的逆转录转座子序列。为什么不像某些物种那样使它们永久失活呢?它们一定对我们有某种适应价值。
5.
doi: 10.1016/j.jare.2024.09.014
近日,来自北京大学第一医院的研究者们在J Adv Res杂志上发表了题为 A novel prognostic scoring system for AML patients undergoing allogeneic hematopoietic stem cell transplantation with real world validation 的文章,该研究开发的预后模型整合了疾病和患者的综合特征,增强了接受同种异体造血干细胞移植的AML患者的风险分层,该模型有效地将mrd阴性和mrd阳性亚组的风险分层,并可能促进更明智的基于mrd的治疗决策。
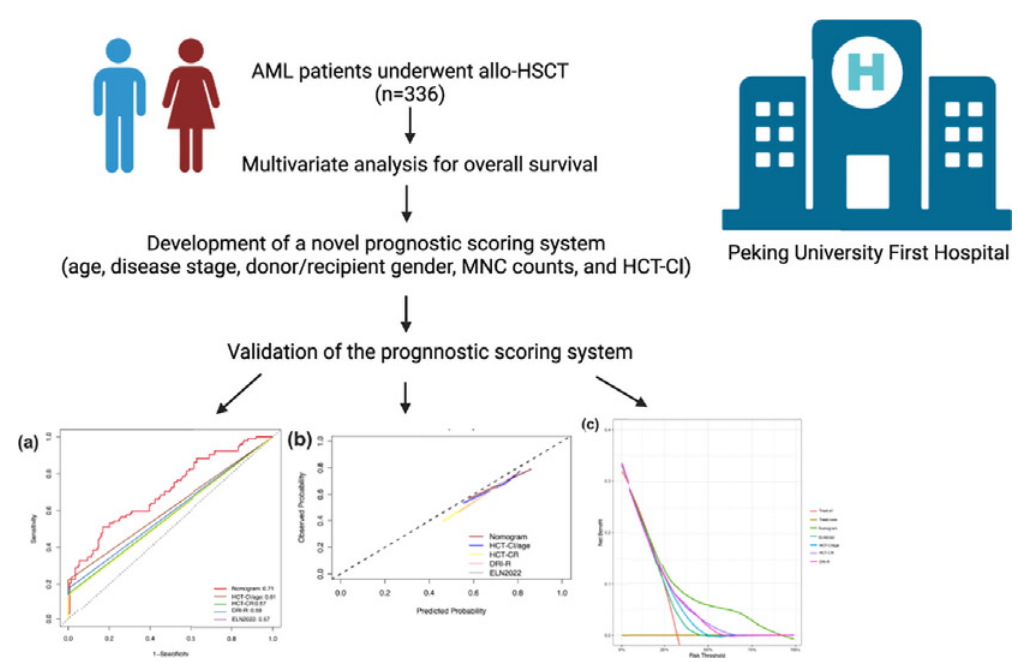
本研究旨在为接受同种异体造血干细胞移植的AML患者的生存建立一个强大的预测模型。作者回顾性分析了2003年9月至2023年3月在北京大学第一医院接受同种异体造血干细胞移植的336例AML患者。进行单变量和多变量Cox回归分析以确定总生存率的风险比(HR)。基于多变量分析结果建立了预测模型。通过bootstrap重采样进行内部验证,并通过一致性指数(C-index)、受试者工作特征(ROC)曲线、校准图和决策曲线分析(DCA)评估模型的性能。
本研究的预后模型包括年龄、疾病分期、供体/受体性别、单个核细胞计数和造血细胞移植合并症指数(HCT-CI),有效地将患者分为低风险和高风险组。两组患者总生存率(P 0.0001)、无病生存率(P 0.0001)、无复发死亡率(NRM) (P 0.0001)、复发率(P=0.08)差异均有统计学意义。该模型的c指数为0.71。校准图和DCA证实了预测结果和观测结果之间的强烈一致性。亚组分析显示,在可测量残余疾病(MRD)阴性和MRD阳性亚组中,高危组的总生存率均显著低于低危组(P=0.015)。
6.
doi:10.1126/science.adn1629
在一项新的研究中,为了研究介导吞噬与梳理行为的线索,来自波士顿儿童医院和哈佛大学等研究机构的研究人员在人体细胞中筛选了 1200 种生物活性小分子,发现 93 种化合物能以剂量依赖的方式显著增加表面 CALR。在这些化合物中,22 种在斑马鱼中还促进了巨噬细胞与干细胞之间的相互作用。
依赖 ROS 增加 CALR 的化合物表现出更高的吞噬率,相反,用不依赖 ROS 的化合物处理的斑马鱼,尽管 CALR 增加,巨噬细胞与干细胞的相互作用增加,但发生梳理事件的概率更高。为了研究在不依赖 ROS 的条件下参与相互作用的信号,研究者在人类细胞中进行了一次全基因组筛选。他们发现 Toll 样受体 3 (TLR3) 是 别吃我 情况下的 CALR 诱导因子。
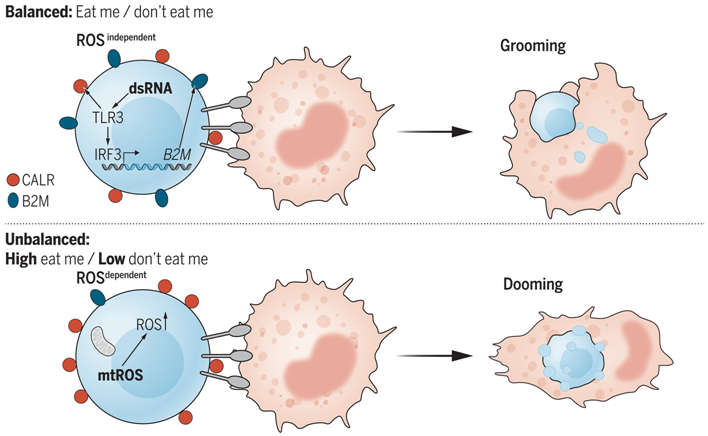
接着,研究者发现 TLR3 的表达是 别吃我 信号 2-微球蛋白(beta-2-microglobulin, B2M)表达所必需的。抗体染色和b2m基因敲除斑马鱼品系的研究表明,干细胞表面上的 b2m 是防止巨噬细胞吞噬所必需的。为了确定在b2m突变体中观察到的吞噬增加是否会影响克隆优势,他们利用斑马鱼彩色条形码系统(TWISTR)作为系谱追踪器,产生了镶嵌缺失。b2m的镶嵌缺失减少了骨髓克隆的数量,但增加了克隆优势。这些斑马鱼体内的优势克隆是野生型的b2m,它们对巨噬细胞吞噬具有抵抗力。TLR3 信号由双链 RNA 激活;由于与重复元件(RE)相关的转录本(包括长末端重复序列(LTR)和内源性逆转录病毒)的表达,有时会在细胞中发现双链 RNA。
HSPC中重复元件的表达与B2m水平的升高呈正相关。此外,在斑马鱼中过表达ltr4会导致更高的HSPC增殖,这表明巨噬细胞吞噬减少。通过干扰 TLR3、IRF3 或 B2M 的表达来破坏 TLR3-B2M 通路,可减少斑马鱼血细胞克隆的数量。使用 DNA 甲基转移酶抑制剂 CM272 来促进重复元件的上调,可扩大斑马鱼胚胎中已建立的 HSPC 克隆的增殖。
7.
doi:10.1126/science.adp2065
造血干细胞(HSC)移植作为治疗癌症、血液疾病及自身免疫性疾病的救命稻草,其疗效与造血干细胞的质量和数量密切相关。近日,阿尔伯特-爱因斯坦医学院的科研团队在小鼠模型中揭开了提高HSC移植成功率的潜在路径,为临床应用带来了新的希望。相关研究结果发表在2024年8月9日的Science期刊上,论文标题为 Regulation of the hematopoietic stem cell pool by C-Kit associated trogocytosis 。

造血干细胞(HSC)移植可治疗个人造血干细胞癌变(如白血病或骨髓增生异常综合征)或干细胞数量不足(如骨髓衰竭和严重自身免疫性疾病)等引起的疾病。治疗过程中,需从供体获取健康的HSC,并将其注入患者体内。
为了收集这些造血干细胞,捐献者需要服用一种药物,促使造血干细胞脱离骨髓,进入血液循环,便于分离和移植。遗憾的是,常用的动员药物常无法释放足量的HSC,影响移植效果。
论文共同通讯作者Britta Will博士说, 少量HSC会自然地从骨髓迁移到血液中,但我们对这一过程的调控机制知之甚少。本次研究为我们带来了深刻洞见,并指明了优化HSC动员策略的方向。
研究团队推测,造血干细胞(HSC)表面蛋白的变化可能会影响它们离开骨髓的倾向。通过对小鼠HSC的分析,他们发现相当一部分HSC携带了与巨噬细胞(一种免疫细胞)相关的表面标记。实验显示,具有这些标记的HSC多留驻骨髓,而无标记的HSC则会在动员药物作用下从骨髓中释放。
进一步实验揭示,HSC与巨噬细胞接触时,会发生胞啃作用:一方细胞摄取另一方的膜片段并将其融入自身。那些表面表达高水平c-Kit蛋白的造血干细胞能够进行胞啃作用,由此吸收巨噬细胞的表面蛋白,增加其在骨髓中的滞留概率。基于此,研究人员认为抑制c-Kit可以中断胞啃作用,从而动员更多HSC用于移植。
8.
doi:10.1038/s41587-024-02226-y
免疫疗法利用人体自身的免疫系统攻击癌细胞,阻止肿瘤生长,从而彻底改变了癌症治疗方法。然而,这些疗法往往需要根据每位患者的具体情况量身定制,从而减慢了治疗进程,导致每位患者的治疗费用高达数十万美元。
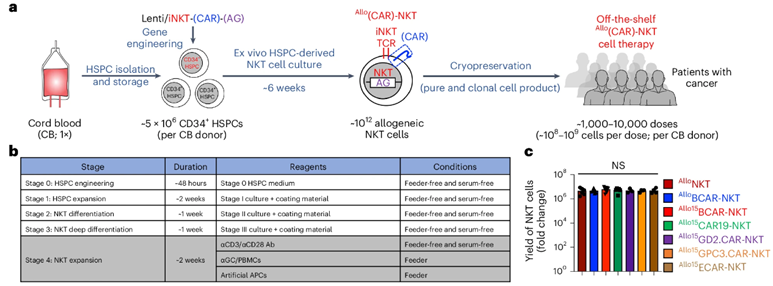
为了解决这些局限性,来自加州大学洛杉矶分校的研究人员在一项新的研究中开发出了一种新的临床指导方法,用于设计更强大的称为恒定自然杀伤细胞(invariant natural killer T cell, iNKT)的免疫细胞,可用于 现成的 癌症免疫疗法,即来自单一脐带血供体的免疫细胞可用于治疗多名患者。这一发现标志着向CAR-T细胞疗法等细胞疗法的大规模生产迈出了重要一步,使这些挽救生命的疗法更加经济实惠,更多患者可以接受。相关研究结果近期发表在Nature Biotechnology期刊上,论文标题为 Generation of allogeneic CAR-NKT cells from hematopoietic stem and progenitor cells using a clinically guided culture method 。论文通讯作者为加州大学洛杉矶分校微生物学、免疫学与分子遗传学教授Lili Yang博士。
2021年,Yang团队报告了一种利用造血干细胞生产大量iNKT细胞的方法。该系统需要使用三维胸腺类器官和支持细胞,这给生产和监管带来了挑战,阻碍了该方法的临床应用。
如今,他们开发出一种技术,能以无饲养细胞和无血清的方式利用造血干细胞产生大量iNKT细胞。这种方法上的升级消除了以前的障碍,使得他们比以往任何时候都更接近为患者提供 现成的 癌症免疫疗法。
这些作者从15份代表不同遗传背景的捐献者脐带血样本中分离出造血干细胞,它们可以自我复制并产生各种血细胞和免疫细胞。据估计,一次脐带血捐献可产生1000到10000剂量的治疗药物,因此该系统非常适合制造 现成的 免疫疗法。
接下来,他们为iNKT细胞配备了嵌合抗原受体(CAR),这种分子能让免疫细胞识别并杀死特定类型的癌症,靶向治疗包括血癌和实体瘤在内的七种癌症。
由此产生的CAR-iNKT细胞对所有七种癌症都显示出了强大的抗肿瘤功效,这表明它们有望治疗多种癌症。随后在多发性骨髓瘤模型中,他们展现了CAR-iNKT细胞阻止肿瘤生长的能力,而且不会引起供体细胞移植到患者体内时可能出现的并发症。
9.
doi:10.1038/s41586-024-07478-x
在一项新的研究中,来自加州大学洛杉矶分校的研究人员发现了一种称为MYCT1的蛋白通过帮助人类造血干细胞(hematopoietic stem cell, HSC)感知和解释来自它们所处环境的信号,在调节它们的自我更新方面发挥着关键作用。这一发现使得科学家们离开发出在实验室培养皿中扩增造血干细胞的方法更近了一步,这将使挽救生命的造血干细胞移植更容易获得,并提高基于造血干细胞的疗法(比如基因疗法)的安全性。相关研究结果发表在2024年6月13日的Nature期刊上,论文标题为 MYCT1 controls environmental sensing in human haematopoietic stem cells 。
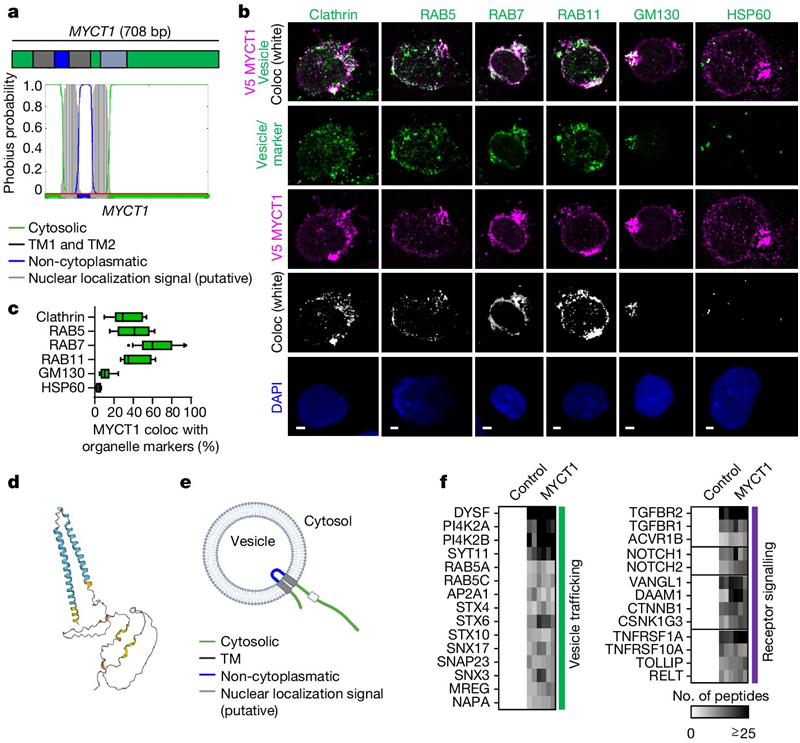
造血干细胞能够通过自我更新过程复制自身,并能分化产生人体内的所有血细胞和免疫细胞。几十年来,造血干细胞移植一直被用作治疗白血病等血癌以及其他多种血液和免疫疾病的救命疗法。然而,造血干细胞移植有很大的局限性。寻找匹配的捐赠者可能很困难,特别是对于非欧洲血统的人来说,而且可用于移植的造血干细胞数量可能太少,无法安全地治疗患者的疾病。
这些限制之所以持续存在,是因为从人体中提取并置于实验室培养皿中的造血干细胞很快就会失去自我更新的能力。经过数十年的研究,科学家们已经非常接近解决这个问题。
论文共同通讯作者、加州大学洛杉矶分校伊莱和艾迪斯-布罗德再生医学与干细胞研究中心成员Hanna Mikkola博士说, 我们已经知道如何制造出看起来与造血干细胞一样的细胞,并具备它们的所有特征,但当这些细胞用于移植时,它们中的许多仍然不起作用;缺少了一些东西。
为了找出阻碍这些造血干细胞样细胞(blood stem cell-like cell)发挥全部功能的缺失部分,论文第一作者兼论文共同通讯作者Julia Aguade Gorgorio分析了测序数据,确定造血干细胞被置于实验室培养皿中时发生沉默的基因。其中的一个基因 MYCT1,对这些细胞的自我更新能力至关重要。
他们发现,MYCT1调节一种叫做内吞(endocytosis)的过程,该过程在造血干细胞如何从环境中接收告诉它们何时自我更新、何时分化、何时处于静止状态的信号方面起着关键作用。
10.
doi:10.1182/blood.2024024275
我们的骨髓 骨骼中的脂肪、果冻状物质,是一个看不见的动力源,每天悄无声息地制造 5000 亿个新的血细胞。这个过程是由造血干细胞驱动的。造血干细胞在我们体内生成各种类型的血细胞,并自我再生,以保持整个造血流水线顺利运行。
与任何复杂的系统一样,造血干细胞也会随着年龄的增长而丧失功能,并在此过程中导致罹患包括血癌在内的严重疾病的风险。我们知道,不同个体罹患衰老相关疾病的风险不同。但令人吃惊的是,人们对造血干细胞是否会因个体差异而衰老知之甚少。

这是有原因的:因为造血干细胞非常稀少,科学家们员通常把所有这些干细胞集中在一起,进行综合研究。在一项新的研究中,Trowbridge及其同事对9只基因相同的中年小鼠的造血干细胞进行了单细胞水平的研究,首次近距离观察了骨髓微环境的微妙变化如何使不同小鼠的造血干细胞衰老。相关研究结果近期发表在Blood期刊上,论文标题为 Variation in Mesenchymal KITL/SCF and IGF1 Expression at Middle Age Underlies Steady-State Hematopoietic Stem Cell Aging 。
Trowbridge及其团队发现,尽管这些小鼠的年龄相同,但是它们骨髓中造血干细胞的衰老程度却各不相同。但这还不是全部。他们可以根据两种也存在于人体中的生长因子的活性预测造血干细胞的功能。
这两种生长因子 Kitl和Igf1,是由骨髓微环境中造血干细胞周围的间充质基质细胞(mesenchymal stromal cell, MSC)产生的。通过分析这些MSC在小鼠个体中的RNA转录组,Trowbridge发现这两种生长因子的减少与造血干细胞中的年龄相关分子程序有关。(100医药网100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- JCI:新研究揭示一种潜在致命性癫痫的发病机制 (2025-10-29)
- 人类再生医学找到新线索!Cell:蝾螈断肢再生靠“全身备战”,交感神经触发干细胞“总动员” (2025-10-29)
- 造血干细胞研究进展(第14期) (2025-10-29)
- Nature头条:揭开“猫屎咖啡”独特风味背后的奥秘 (2025-10-28)
- Cell:我国科学家揭示V型CRISPR系统起源背后的功能性RNA分裂机制 (2025-10-28)
- Science:酸性肿瘤环境促进胰腺癌细胞的生存和生长 (2025-10-28)
- 再生医学里程碑!上海九院李青峰/黄如林团队全球首次实现脂肪跨胚层再生类器官,登上中国工程院院刊 Engineering (2025-10-28)
- Science:新的分子策略实现抗MRSA天然产物Spiroaspertrione A的人工完整合成 (2025-10-28)
- 研究发现癌细胞与肿瘤相关巨噬细胞代谢互作促进肝癌转移新机制 (2025-10-28)
- “脂质溢出”是元凶?10月30日直播预告:揭秘肥胖代谢共病背后的真相 (2025-10-27)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















