《细胞·代谢》:上海交大科学家发现,果糖促进脂肪产生瘦素,增强CD8阳性T细胞的抗肿瘤免疫反应 |
 |
《细胞·代谢》:上海交大科学家发现,果糖促进脂肪产生瘦素,增强CD8阳性T细胞的抗肿瘤免疫反应
来源:奇点糕 2023-10-23 10:20
多项研究显示,高果糖摄入可促进肝脏和结直肠肿瘤的发生发展[1-4],但同时,美国国立健康研究所-美国退休人员协会(NIH-AARP)饮食和健康研究的结果却显示,果糖对肺癌存在保护作用[5,6]。多项研究显示,高果糖摄入可促进肝脏和结直肠的发生发展[1-4],但同时,美国国立健康研究所-美国退休人员协会(NIH-AARP)饮食和健康研究的结果却显示,果糖对存在保护作用[5,6]。这种看似完全相反的结果可能是与不同的肿瘤微环境有关,这是不是也说明,果糖并不是坏得不可救药?
好像还真是。在昨天的《细胞 代谢》杂志上[7],上海交通大学医学院附属赵任教授、上海交通大学医学院附属胸科医院孙加源教授、上海交通大学医学院上海市学研究所叶幼琼和邹强研究员带领的研究团队发现,饮食中的果糖可以调节脂肪细胞代谢,促进瘦素产生,继而增强CD8阳性T细胞的抗反应。
这一研究结果为我们利用果糖-瘦素轴来增强免疫治疗疗效提供了理论支持。

研究人员在给普通小鼠喂食高果糖饮食和普通饮食并接种瘤细胞后,发现高果糖饮食组的肿瘤生长和小鼠死亡率明显低于普通饮食组,他们在肺腺癌和小鼠模型中也发现了同样的效果。
利用单细胞RNA测序,研究人员鉴定了黑色素瘤小鼠肿瘤组织中分离的T细胞。他们发现,高果糖组相比普通饮食组的CD8阳性T细胞的亚群比例大有不同,耗竭T细胞减少,记忆T细胞增加。
对细胞状态变化轨迹的分析显示,记忆T细胞处于轨迹的起点,终末期耗竭T细胞和效应T细胞处于终点,而位于起点的早期CD8阳性T细胞主要存在于高果糖组小鼠的肿瘤中,对照组中很少,终末期耗竭T细胞则刚好相反。也就是说,高果糖饮食让CD8阳性T细胞免于走向耗竭的结局,保留了它们的抗肿瘤能力。
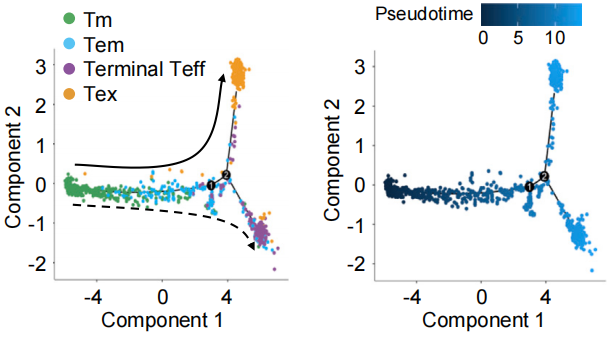
细胞状态变化轨迹分析结果
不过,果糖对CD8阳性T细胞的 拯救 并非是直接的,直接对T细胞负责的是肿瘤微环境中可以增强T细胞功能的脂肪细胞因子瘦素。高果糖组小鼠的瘦素水平明显高于普通饮食组,使用抗瘦素单抗治疗高果糖组小鼠,或者给携带瘦素受体缺陷T细胞的小鼠喂食高果糖饮食,小鼠的肿瘤生长均恢复正常速度,肿瘤相关死亡率也随之提高。
瘦素主要产生于白色脂肪组织,高果糖组小鼠附睾、腹股沟和腋窝白色脂肪组织的脂肪细胞中,瘦素的表达确实明显增加,手术摘除小鼠附睾白色脂肪组织后,高果糖饮食也难以增加小鼠血清中的瘦素水平。
果糖对脂肪细胞中瘦素水平的调节依赖于白色脂肪组织中mTORC1信号通路的激活。mTORC1复合物中关键成分Raptor缺失的小鼠即使摄入高果糖饮食,瘦素表达仍然减少,肿瘤生长也明显加快。
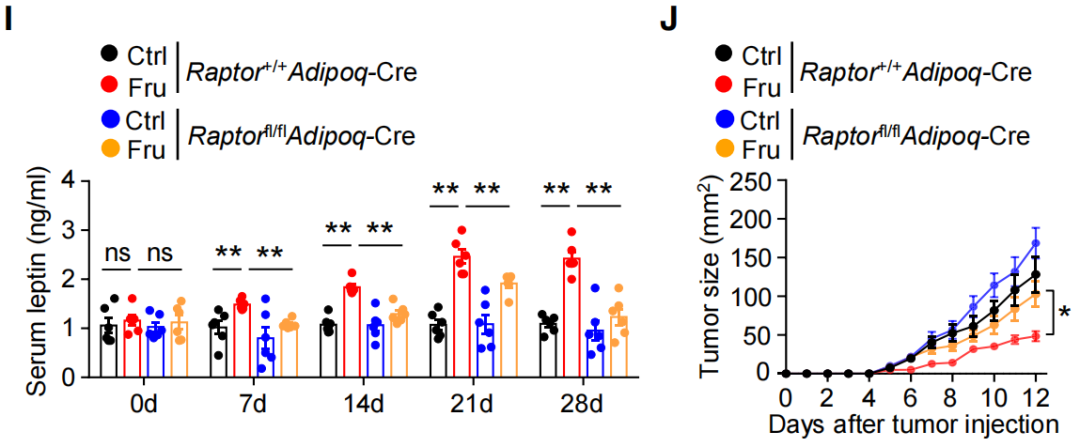
Raptor正常和缺失的小鼠接受普通饮食和高果糖饮食的血清瘦素水平(I)和肿瘤体积(J)变化
由此,研究人员确认了果糖-mTORC1-瘦素-CD8阳性T细胞这条高果糖饮食促进抗肿瘤免疫反应的通路。
最后,研究人员将这一重要发现在癌症患者中进行了重现。
他们分析了20例血浆中果糖和瘦素的水平,发现循环系统中果糖和瘦素水平呈正相关关系,血浆中瘦素水平与肿瘤浸润性IFN- 阳性效应CD8阳性T细胞的比例也呈正相关关系。
此外,他们还在患者中进行了同样的分析,但是这些患者的血浆瘦素水平与果糖水平和肿瘤浸润性IFN- 阳性效应CD8阳性T细胞的比例均不具有相关性,而且相比肺癌患者,结直肠癌患者循环系统中的瘦素水平明显降低。这可能意味着,高果糖饮食介导的抗肿瘤T细胞免疫反应增强受肿瘤类型的影响。
总而言之,这项研究揭示了果糖-脂肪细胞瘦素-CD8阳性T细胞这一免疫内分泌通路,有助于促进T细胞抗肿瘤免疫反应,扩大了我们目前对饮食果糖调节抗肿瘤免疫反应的分子机制的理解。
医药网新闻
- 相关报道
-
- Nat Biomed Eng:用“声波画笔”调控大脑!新型全息超声技术有望打开人类神经疾病治疗新大门 (2025-10-07)
- 《神经元》:短期高脂饮食也同样危险!科学家发现,两天的高脂饮食即可激活小鼠大脑特定抑制性神经元,导致认知受损,恢复正常饮食可逆转 (2025-10-07)
- 相分离研究登上Nature:超越转录调控,mRNA协调易凝聚蛋白稳态 (2025-10-07)
- 动辄百万美元奖金,这些科学大奖想要与诺贝尔奖竞争:它们含金量如何? (2025-10-06)
- Nature:T细胞耗竭的悖论——并非“精疲力竭”,而是“生产过剩”引发的蛋白毒性风暴 (2025-10-06)
- Cell:沉默的基因组,喧嚣的转录场——解密结核菌适应性的隐藏驱动力 (2025-10-06)
- Nature:谁掌控了人类生命的第一个开关?一个被“驯化”的逆转录病毒的自白 (2025-10-06)
- 三个月,改写生命!全球首例帕金森病实现功能性治愈 (2025-10-05)
- AJP:迄今最长时间真实世界安全性分析显示,艾司氯胺酮鼻喷剂的安全性与临床研究和产品说明书中已确定的一致 (2025-10-05)
- Nature子刊:谭蔚泓/邱丽萍团队开发核酸适配体武装的单核细胞疗法,治疗阿尔茨海默病 (2025-10-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















