改写细胞死亡法则?Science:发现癌细胞死亡的新途径——SLafen1基因 |
 |
来源:100医药网 2024-05-29 09:48
SLafen1的崭露面纱,为抗癌战役提出了新的策略。Brummelkamp团队的发现,不仅是癌症治疗的新篇章,更是基因探索的里程碑,为后续研究指明了方向。在抗癌战役的漫长征途中,化疗作为传统武器,其斩杀癌细胞的机制似乎藏匿着未解之谜。荷兰癌症研究所的Thijn Brummelkamp及其同事们发现了一种全新的癌细胞死亡方式:由 Schlafen11 基因导致。相关研究结果发表在2024年5月17日的Science期刊上,论文标题为 DNA damage induces p53-independent apoptosis through ribosome stalling 。
这是一个非常出人意料的发现。癌症患者接受化疗已有近一个世纪的历史,但这种细胞死亡途径以前从未被观察到。患者在何时何地出现这种情况还需要进一步研究。这一发现最终可能会对癌症患者的治疗产生影响。
许多癌症治疗方法都会损伤细胞 DNA。在受到过多无法弥补的损伤后,细胞会自行死亡。高中生物学告诉我们,p53 蛋白负责这一过程。p53 确保修复受损的 DNA,但当损伤变得过于严重时,就会启动细胞自杀。这可以防止细胞分裂失控和癌症形成。
震惊!悬而未决的问题
这听起来像是一个万无一失的系统,但实际情况却更为复杂。Brummelkamp 说, 在一半以上的肿瘤中,p53 不再起作用。关键基因 p53 在其中不起任何作用。那么,为什么没有 p53 的癌细胞在化疗或放疗破坏其 DNA 时仍然会死亡呢?令我惊讶的是,这竟然是一个没有答案的问题。
随后,他的研究团队与他的同事Reuven Agami的研究团队一起,发现了一种以前未知的细胞在 DNA 受损后死亡的方式。在实验室里,他们对细胞进行了化疗,并对其中的DNA进行了仔细比对。Brummelkamp说, 我们一直在寻找一种能让细胞在化疗中存活下来的遗传改变。我们的团队在选择性让基因失活方面有很多经验,我们完全可以将其应用于此。
细胞死亡中的新关键角色
通过选择性使特定基因失效,研究人员发现了以 Schlafen11(SLFN11)基因为首的细胞死亡新途径。论文第一作者Nicolaas Boon说, 在DNA受损的情况下,SLFN11会关闭细胞的蛋白制造工厂:核糖体。这会给这些细胞造成巨大压力,导致它们死亡。我们发现的这个新途径完全绕过了 p53。
SLFN11 基因在癌症研究中并不陌生。Brummelkamp说,在对化疗没有反应的患者的肿瘤中,SLFN11 基因经常处于非活性状态。 我们如今可以解释这种联系了。当细胞缺乏 SLFN11 时,它们不会以这种方式对 DNA 损伤做出反应而死亡。细胞会存活下来,癌症也会持续存在。
对癌症治疗的影响
Brummelkamp说, 这一发现揭示了许多新的研究问题。我们在实验室培养的癌细胞中证实了我们的发现,但仍存在许多重要问题:这条途径在患者体内何时何地出现?它对疗法或化疗有何影响?它是否会影响癌症治疗的副作用?如果事实证实这种细胞死亡形式在患者体内也起着重要作用,那么这一发现将会对癌症治疗产生关键的影响,而这些都是需要进一步研究的重要问题。
逐个关闭基因
人类有成千上万个基因,其中许多基因的功能我们并不清楚。为了确定人类基因的作用,Brummelkamp开发了一种使用单倍体细胞的方法。这些细胞只包含每个基因的一个拷贝,与我们体内包含每个基因两个拷贝的普通细胞不同。在遗传实验中,处理两个拷贝是一项挑战,因为变化(突变)往往只发生在其中的一个拷贝中。这样就很难观察到这些突变的影响。
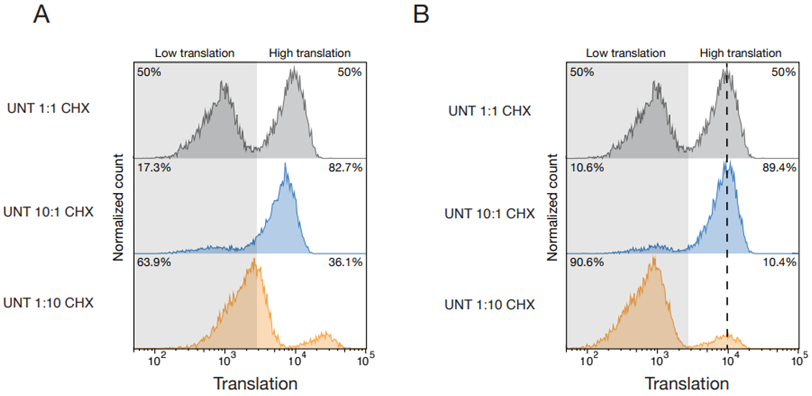
图片来自Science, 2024, doi:10.1126/science.adh7950
多年来,Brummelkamp与其他人一起,利用这种多用途方法揭示了对疾病至关重要的过程。例如,他的团队近期已发现,细胞制造脂质的方式与之前已知的不同。
他们揭示了某些病毒(包括致命的埃博拉病毒)是如何进入人体细胞的。他们深入研究了癌细胞对特定疗法的抵抗性,并确定了对免疫系统起制动作用的蛋白,这与癌症免疫疗法息息相关。
在过去几年中,他的团队发现了四十年来一直难以捉摸的两种酶,而这两种酶对肌肉功能和大脑发育至关重要。
综上所述,SLafen1的崭露面纱,为抗癌战役提出了新的策略。Brummelkamp团队的发现,不仅是癌症治疗的新篇章,更是基因探索的里程碑,为后续研究指明了方向。(100yiyao.com)
参考资料:
Nicolaas J. Boon et al. . Science, 2024, doi:10.1126/science.adh7950.
Researchers discover new pathway to cancer cell suicide
https://www.avl.nl/en/news/2024/researchers-discover-new-pathway-to-cancer-cell-suicide/
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nat Biomed Eng:用“声波画笔”调控大脑!新型全息超声技术有望打开人类神经疾病治疗新大门 (2025-10-07)
- 《神经元》:短期高脂饮食也同样危险!科学家发现,两天的高脂饮食即可激活小鼠大脑特定抑制性神经元,导致认知受损,恢复正常饮食可逆转 (2025-10-07)
- 相分离研究登上Nature:超越转录调控,mRNA协调易凝聚蛋白稳态 (2025-10-07)
- 动辄百万美元奖金,这些科学大奖想要与诺贝尔奖竞争:它们含金量如何? (2025-10-06)
- Nature:T细胞耗竭的悖论——并非“精疲力竭”,而是“生产过剩”引发的蛋白毒性风暴 (2025-10-06)
- Cell:沉默的基因组,喧嚣的转录场——解密结核菌适应性的隐藏驱动力 (2025-10-06)
- Nature:谁掌控了人类生命的第一个开关?一个被“驯化”的逆转录病毒的自白 (2025-10-06)
- 三个月,改写生命!全球首例帕金森病实现功能性治愈 (2025-10-05)
- AJP:迄今最长时间真实世界安全性分析显示,艾司氯胺酮鼻喷剂的安全性与临床研究和产品说明书中已确定的一致 (2025-10-05)
- Nature子刊:谭蔚泓/邱丽萍团队开发核酸适配体武装的单核细胞疗法,治疗阿尔茨海默病 (2025-10-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















