IL |
 |
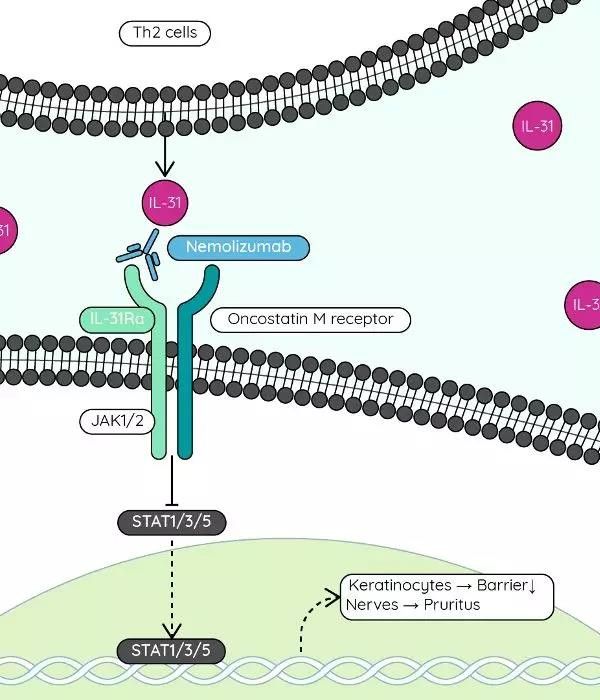
Galderma公司日前宣布,美国已经授予该公司开发的“first-in-class”IL-31受体α单克隆抗体nemolizumab 的突破性疗法认定,用于治疗结节性痒疹((prurigo nodularis, PN)。
结节性痒疹是一种潜在使人衰弱的罕见慢性皮肤病,表现为覆盖大面积皮肤的厚结节和伴随的严重瘙痒。 它经常严重损害患者生活质量。
Nemolizumab是一种”first-in-class”在研单克隆抗体,它通过与IL-31受体α相结合,可以阻断IL-31的信号通路。IL-31是导致严重瘙痒的重要细胞因子。Galderma最近在欧洲皮肤学和性病学会28届年度大会上,公布了它治疗中重度结节性痒疹患者的2期研究结果。 与安慰剂相比,Nemolizumab不仅达到了试验的主要重点——显着改善患者的峰值瘙痒数值评定量表(PP NRS)评分,而且根据研究者全球评估(IGA)的测量,患者皮肤病变也得到了显着改善。
Galderma公司全球处方药副总裁Thibaud Portal博士评论道:“2期的结果,让我们能够提供实质性的临床证据,支持美国授予的突破性疗法认定。 我们对于可能为医生和他们的结节性痒疹患者提供创新治疗选择的前景感到非常兴奋。这一疾病目前还没有获批的治疗选择。 我们将致力于继续推进nemolizumab的开发项目。”
目前,Galderma公司正在积极准备在2020年启动关键性3期,使用Nemolizumab治疗成年结节性痒疹。我们预祝在突破性疗法认定的帮助下,这款创新疗法能够早日上市,为患者造福。(100yiyao.com)
医药网新闻
- 相关报道
-
- 药明康德高管:赋能创新转化,需要的不仅是科学本身 (2025-07-25)
- PCF®技术——生物智造领域人类新质生产力 (2025-07-25)
- 马来西亚医疗旅游理事会推出MYMT 2026,打造马来西亚首个医疗旅游年 (2025-07-25)
- “十四五”以来,医保基金累计收入12.13万亿元,年均增速9.1% (2025-07-25)
- 《柳叶刀》子刊:复发风险减半!研究表明,抗抑郁药和氯氮平联用与难治性精神分裂症的复发风险降低51%有关 (2025-07-25)
- 槲皮素哪个牌子效果最好?2025年全球十大槲皮素护肺品牌成分、技术、口碑、临床数据深度评测 (2025-07-25)
- 护肺选对不选贵!槲皮素哪个牌子效果最好?成分、技术全面剖析 (2025-07-25)
- 深度溯源有机品质,第二届717龙凤堂有机黄芪节在固阳举办 (2025-07-25)
- 中国西部干细胞中心平台全面上线 引领生物医药产业协同新纪元 (2025-07-25)
- Nat Microbiol:新研究以前所未有的细节捕捉到进入细胞核的HIV-1病毒核心 (2025-07-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















