抗精神病新药!ALKS3831(奥氮平/samidorphan)在美国进入审查,治疗精神分裂症和双相I型障碍 |
 |

2020年01月29日讯 /BIOON/ --Alkermes是一家全面整合的爱尔兰生物制药公司,致力于开发治疗中枢神经系统(CNS)疾病和的创新药物。近日,该公司宣布,美国食品和药物管理局(FDA)已受理ALKS3831(olanzapine/samidorphan)的新药申请(NDA),这是一种新型口服非典型抗精神病药物,每日一次,用于治疗精神分裂症和双相I型障碍。该药旨在提供奥氮平(olanzapine)的疗效,同时减轻奥氮平引起的体重增加。已指定处方药用户收费法(PDUFA)目标日期为2020年11月15日。ALKS3831有4种固定剂量组合,由10mg剂量的samidorphan与不同剂量的奥氮平(5mg、10mg、15mg、20mg)配制而成。
ALKD3831是由一种新颖的新分子实体samidorphan(新型选择性μ-阿片受体拮抗剂)和一种已上市抗精神病药物奥氮平(olanzapine)制成的一种双层片剂。体重增加和临床相关的代谢问题是非典型抗精神分裂药物常见的副作用。奥氮平是一种有效的抗精神病药物,但临床使用受限于其高发的体重增加。ALKD3831的设计力图在提供奥氮平的强力抗精神病疗效的同时,降低对体重和新陈代谢的副作用,从而提高治疗的安全性。
ALKD3831 NDA中纳入了在精神分裂症患者中开展的ENLIGHTEN临床开发项目(包括2项关键III期研究ENLIGHTEN-1、ENLIGHTEN-2)的数据、比较ALKS3831和已上市药物Zyprexa(奥氮平)药代动力学(PK)桥接研究的数据,以支持治疗精神分裂症适应症,以及作为单药或作为锂或丙戊酸钠的辅助疗法治疗双相I型障碍相关的躁郁症或混合发作、维持治疗双相I型障碍。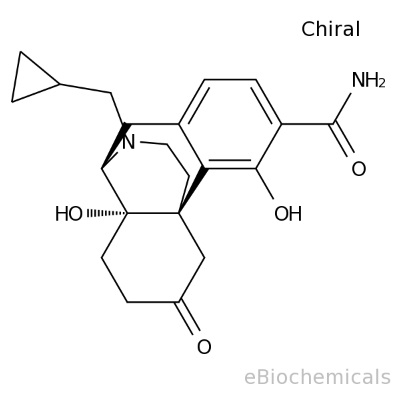
samidorphan分子结构式(图片来源:ebiochemicals.com)
ENLIGHTEN-1是一项为期4周的随机、双盲III期研究,在正经历急性加重的精神分裂症患者中开展,比较了ALKS3831相对于安慰剂的抗精神病疗效、安全性和耐受性。结果显示,研究达到了主要终点:与安慰剂组相比,ALKS3831治疗组阳性和阴性症状量表(PANSS)评分相对基线显示出统计学意义的显著降低。该研究中还纳入了一个奥氮平治疗组,但不是为了比较ALKS3831和奥氮平之间的疗效或安全性。研究数据显示,与安慰剂组相比,奥氮平治疗组在PANSS评分相对基线的变化具有相似的改善。
ENLIGHTEN-2是一项为期6个月的书籍、双盲III期研究,在病情稳定的精神分裂症患者中开展,评估了ALKS3831与安慰剂对体重的影响。结果显示,研究达到了共同主要终点,表明:与奥氮平治疗组相比,ALKS3831治疗组在治疗第6个月时体重从基线开始的平均体重增加百分比较低、在治疗第6个月时体重增加≥10%的患者比例较低。
Alkermes首席医疗官兼药物开发和医疗事务高级副总裁Craig Hopkinson医学博士表示:“FDA受理ALKS3831的新药申请,标志着我们向精神分裂症和双相情感障碍患者提供新治疗选择目标方面实现的一个重要里程碑。我们相信,ALKS3831有潜力为这些严重和复杂精神疾病患者提供一个有意义的新产品,我们期待着在整个NDA审查过程中与密切合作”(100医药网100yiyao.com)
原文出处:Alkermes Announces U.S. Food and Drug Administration Acceptance of ALKS 3831 New Drug lication for Treatment of Schizophrenia and Bipolar I Disorder
医药网新闻
- 相关报道
-
- Trends Neurosci最新综述:腹侧被盖区(VTA)——压力下的“情绪指挥家” (2025-07-27)
- 不顾作者强烈抗议,Science期刊撤稿了这篇15年前发表的颠覆性论文,“砷基生命”尘埃落定 (2025-07-27)
- Science:一种经过改造的肠道细菌有望对抗肾结石 (2025-07-26)
- Science:人类首次实现 用“专属食物”精准遥控肠道内的活体药物 (2025-07-26)
- Science子刊:一种新发现的lncRNA可能解释了2型糖尿病患者肌肉量减少的原因 (2025-07-26)
- 中国药企如何“智闯”沙特? (2025-07-26)
- 马来西亚医疗旅游理事会推出MYMT 2026,打造马来西亚首个医疗旅游年 (2025-07-25)
- Int J Radiat Oncol Biol Phys:MRI导航精准放疗——让高剂量直击肿瘤顽固区,疗效提升还不伤正常组织 (2025-07-25)
- 研究发现乳酸穿梭调控巨噬细胞极化并参与2型糖尿病进程 (2025-07-25)
- 癫痫手术步入毫米时代,仁济多学科联手“机器人+激光”精准消除脑内病灶 (2025-07-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040
 |
 |
| 解决便秘的偏方 | 女孩向往 |
 |
 |
| 婴儿出生时瞬间 | 西红柿养生功效 |
|


















