美国FDA批准口服药物deucravacitinib用于治疗中度至重度斑块型银屑病成年患者 |
 |
来源:百时美施贵宝2022-09-11 20336051
口服选择性酪氨酸激酶2 (TK2)变构抑制剂是目前世界上唯一获批的TK2抑制剂,也是近10年来首个用于治疗中重度斑块型银屑病的创新口服药物。
百时美施贵宝公司近日宣布,美国美国食品药品监督管理局(FDA)批准了全球首个口服选择性酪氨酸激酶2 (TK2)变构抑制剂deucravacitinib,用于治疗适合全身治疗或光疗的中重度斑块型银屑病成年患者。不建议将deucravacitinib与其他强效免疫抑制剂联合使用。
这一批准是基于两个关键的三期临床研究的结果,POETYK PSO-1和POETYK PSO-2。结果显示,在1,684名18岁及以上中度和重度斑块型银屑病患者中,deucravacitinib(每天一次)优于安慰剂和Otezla (apremilast,每天两次)1。与安慰剂和奥兹拉相比,deucravacinib的治疗优势在第16周和第24周显现,对deucravacinib的反应率可持续至第52周。
鉴于POETYK PSO研究中deucravacitinib在改善皮损方面的优势,该疗法有望成为中重度斑块型银屑病患者口服用药的新标准。POYK PSO-1临床试验研究员、美国南加州大学皮肤科副院长兼教授、医学博士、公共卫生硕士阿普里尔阿姆斯特朗(April Armstrong)表示,中重度斑块型银屑病患者面临巨大的疾病负担,deucravacitinib将是一种受欢迎的一线系统治疗方案。
银屑病是一种常见的慢性和系统性免疫介导的疾病,在美国影响近750万人。高达90%的银屑病患者患有斑块型银屑病,其特征为界限清楚的圆形或椭圆形斑块,其表面通常覆盖有银白色鳞屑。近四分之一的银屑病患者(美国约有200万人)具有中度至重度的疾病严重程度。
对于患有中重度斑块型银屑病,但对局部治疗或传统全身治疗不满意的患者来说,deucravacitinib的获批让他们倍感振奋。这是百时美施贵宝的又一非凡成就。我们带来了全新的行动机制。这是近十年来第一个被批准的口服疗法,也是第一个每天口服一次治疗中重度斑块型银屑病的药物。百时美施贵宝首席医疗官Samit Hirawat博士表示,我们相信deucravacitinib是银屑病治疗领域的突破性药物,我们也期待它在其他免疫介导的疾病中的潜力。
POETYK PSO研究显示,在第16周,在deucravacitinib治疗组中最常见的不良反应(1%且高于安慰剂组)包括上呼吸道感染(19.2%)、血清肌酸磷酸激酶升高(2.7%)、单纯疱疹(2.0%)、口腔溃疡(1.9%)和毛囊炎(1.7%),此外,在deucravacitinib治疗组中有2.4%的患者、在安慰剂治疗组中有3.8%的患者和在Otezla治疗组中有5.2%的患者停止服用
在美国,虽然有很多种疗法可用,但仍有许多斑块型银屑病患者未接受治疗或治疗少于5,6。美国国家银屑病基金会主席兼首席执行官Leah M. Howard博士说:这种新的口服疗法已经获得FDA批准,这对银屑病患者来说是一个令人兴奋的消息。我们非常欢迎这个全新的治疗方案。
百时美施贵宝真诚感谢所有参与POETYK PSO临床研究的患者和研究人员。Deucravacitinib预计于2022年9月在美国上市。
PEOTYK PSO-1和PEOTYK PSO-2的研究
PEOTYK PSO-1和PEOTYK PSO-2的III期临床研究评估了deucravacitinib(6 mg,每天一次)与安慰剂和Otelza (apremilast,30 mg,每天两次)在治疗中度和重度斑块型银屑病患者中的疗效和安全性。这两项研究都是国际多中心、随机、双盲、安慰剂和阳性对照的52周III期研究。POYK PSO-2还包括随机停药和24周后再治疗。总共有664名患者入选Petykpso-1,1,020名患者入选Petykpso-2。所有患者均患有中度至重度斑块型银屑病,适合光疗或全身治疗。同时,患者符合患体表面积(BSA)10%、银屑病面积和严重程度指数(PASI)12、静态医生总体评价(sPGA)3(中度或重度)的要求。
POEYK PSO-1和POEYK PSO-2研究的共同主要研究终点是:与安慰剂相比,在第16周达到PASI 75(银屑病面积和严重程度指数评分改善至少75%)和静态医生总体评价评分为0或1 (sPGA 0/1)的患者比例。关键的次要研究终点包括与奥兹拉相比,在第16周和第24周达到PASI 75、PASI 90和sPGA 0/1的患者比例。
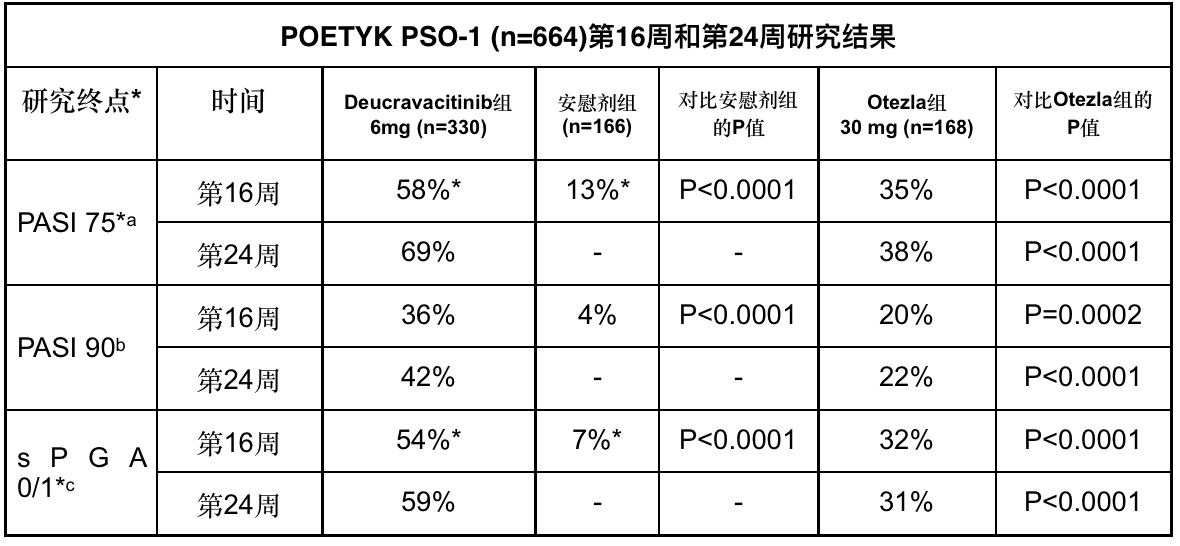
* POETYK PSO-1 和 POETYK PSO-2研究的共同主要研究终点均为deucravacitinib对比安慰剂在第16周时达到PASI 75和sPGA 0/1的患者比例
a. PASI 75的定义为:与基线相比,银屑病面积与严重程度指数(PASI)评分改善至少75%
b. PASI 90的定义为:与基线相比,银屑病面积与严重程度指数(PASI)评分改善至少90%
c. sPGA 0/1的定义为:静态医生总体评估(sPGA)评分为皮损清除或基本清除
应答率可持续至52周。POETYK PSO-1研究显示,在所有接受deucravacitinib治疗并在第24周达到PASI 75的患者中,82%(187/228)患者的PASI 75应答可持续至第52周。在POETYK PSO-2研究中,80%(119/148)持续接受deucravacitinib治疗的患者维持了PASI 75应答,而在中断deucravacitinib治疗的患者中,这一比例为31%(47/150)。
16周治疗期间,29%接受deucravacitinib治疗的患者发生感染,安慰剂组为22%。大部分为非严重感染,严重程度为轻度至中度,且未导致deucravacitinib停药。分别有5名deucravacitinib组患者和2名安慰剂组患者报告了严重感染。52周治疗期间,最常见的严重感染为肺炎和COVID-19。3名deucravacitinib组患者报告了恶性肿瘤(不包括非黑色素瘤皮肤癌)。
关于银屑病
银屑病是一种常见的慢性、系统性免疫介导疾病,严重损害患者的身体健康、生活质量和工作效率7。作为一个全球性严重问题,全世界至少1亿人受到各类银屑病的影响8,其中美国约有750 万人3。近四分之一银屑病患者的疾病严重程度为中度至重度3。高达90%的银屑病患者为寻常型银屑病或斑块状银屑病6,其特征是界限清楚的圆形或椭圆形斑块,表面通常覆有银白色鳞屑。
关于deucravacitinib
Deucravacitinib是一种选择性酪氨酸激酶2(TYK2)变构抑制剂。TYK2是Janus激酶(JAK)家族中的一员。Deucravacitinib通过与 TYK2 的调节结构域结合,从而稳定激酶的调节结构域和催化结构域之间的抑制性相互作用。如细胞实验所示,这会导致对受体介导的TYK2活化及其下游STAT(信号转导及转录激活因子)活化的变构抑制。JAK在JAK-STAT通路中作为同源或异源二聚体发挥作用。如细胞实验所示,TYK2与JAK1形成二聚体以介导多种细胞因子通路,也与JAK2形成二聚体以传递信号。目前尚不清楚TYK2酶抑制与成人中重度斑块状银屑病治疗有效性之间的确切机制。
EMA和全球其他国家或地区的医疗卫生部门正在就deucravacitinib用于治疗中重度斑块状银屑病的适应症进行监管审查。日本厚生劳动省正在对其用于治疗成人中重度斑块状银屑病、脓疱型银屑病和红皮病型银屑病患者的适应症进行监管审查。
注:目前deucravacitinib尚未在中国获批。
参考资料
1 SOTYKTU Prescribing Information. SOTYKTU U.S. Product Information. September 2022. Princeton, N.J.: Bristol-Myers Squibb Company.
2 Chimalakonda A, Burke J, Cheng L, et al. Selectivity profile of the tyrosine kinase 2 inhibitor deucravacitinib compared with janus kinase 1/2/3 inhibitors. Dermatol Ther (Heidelb) 2021;11(5):1763 1776. doi: 10.1007/s13555-021-00596-8.
3 Armstrong AW, Mehta MD, Schupp CW, et al. Psoriasis prevalence in adults in the United States. JAMA Dermatol. Published online June 30, 2021. doi:10.1001/jamadermatol.2021.2007.
4 Armstrong A, Gooderham M, Warren RB, et al. Deucravacitinib versus placebo and apremilast in moderate to severe plaque psoriasis: efficacy and safety results from the 52-week, randomized, double-blinded, placebo-controlled phase 3 POETYK PSO-1 trial, Journal of the American Academy of Dermatology (2022), doi: .
5 Lebwohl M, Langley RG, Paul C, et al. Evolution of patient perceptions of psoriatic disease: results from the Understanding Psoriatic Disease Leveraging Insights for Treatment (UPLIFT) survey. Dermatol Ther (Heidelb). 2022;12(1):61-78. Doi: 10.1007/s13555-021-00635-4.
6 Menter A, Gottlieb A, Feldman SR, Van Voorhees AS et al. Guidelines of care for the management of psoriasis and psoriatic arthritis: Section 1. Overview of psoriasis and guidelines of care for the treatment of psoriasis with biologics. J Am Acad Dermatol. 2008 May;58(5):826-50.
7 Armstrong AW, Schupp C, Wu J, Bebo B. Quality of life and work productivity impairment among psoriasis
patients: findings from the National Psoriasis Foundation survey data 2003 2011. PloS One. 2012;7(12):e52935.
8 World Health Organization. Global report on psoriasis. 2016. Accessed May 12, 2022.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:DNA甲基化“随机时钟”——EVOFLUX破译肿瘤演化史,重塑临床预后新维度 (2025-09-13)
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















