《癌细胞》:汽车 |
 |
来源:奇点蛋糕2022-11-09 18336023
嵌合抗原受体T(CAR-T)细胞作为一种新的治疗方法,被称为“活药”,掀起了抗肿瘤治疗的革命性变革。
嵌合抗原受体T()细胞作为一种新的治疗方法,被称为活药,掀起了抗肿瘤治疗的革命性变革。
与小分子药物不同,CAR-T细胞输注后的作用更加多样,但作为药物,其药代动力学具有异质性,难以直接量化和控制。
以往的研究主要集中在如何提高CAR-T细胞的杀伤能力,增强治疗效果。随着研究的深入和临床应用的逐步开展,CAR-T细胞治疗的不良反应越来越受到关注,如细胞因子释放综合征(CRS)、抗原逃逸、T细胞耗竭等。目前,处理这些不良反应的主要方法有全身抑制、抗体阻断炎症细胞因子或清除输注的CAR-T细胞等。
这些策略可以在一定程度上减少副作用,但也会对疗效产生一定的影响,甚至可能引起肿瘤的复发。但如果要再次给予CAR-T治疗,无论细胞获取的难度、治疗的风险,还是高昂的费用,都会让人望而却步。因此,科学家们争先恐后地开展相关研究,以期通过第三方在体内对CAR-T细胞的活性进行定量、可逆的调控,为其临床应用的进一步发展保驾护航。
从2012年到2022年,已有多篇文章报道了通过小分子或蛋白质调节CAR-T细胞活性的方法。有研究利用生物素化单链抗体(ScFv)作为亲和素CAR-T细胞(细胞外ScFv被亲和素替代)与肿瘤细胞之间的中介,实现了可控的T细胞激活和不同抗原靶向的转换[1]。一些研究使用雷帕霉素类似物作为调节剂[2]。
各种方法各有优势,但也有一定的局限性。比如现有的一些方法使用小分子或蛋白质,药代动力学或组织浸润性较差,临床上没有批准,安全性有待验证。
最近,波士顿大学Wilson W. Wong领导的研究小组提出了一系列由口服抗肝炎药物调节的多功能蛋白酶调节CAR(VIPER CAR)系统[3]。
该系统使用美国美国食品药品监督管理局()批准的药物,以剂量依赖的方式可逆地调节CAR-T细胞的活性,从而显著提高CAR-T细胞的安全性。在这个系统的基础上,Wong的团队设计了一种多靶点的VIPER CAR,拓宽了CAR-T细胞的应用范围。相关文章发表在著名杂志《癌细胞》上。

报纸首页截图
具体来说,他们将病毒非结构蛋白3(NS3)蛋白酶引入CAR-T细胞,并使用抑制NS3蛋白酶活性的药物,通过各种不同结构设计的VIPER CAR系统,实现CAR-T细胞活性的可逆调节。
NS3是丙型肝炎病毒生命周期中的关键蛋白。它可以通过在其下游非结构蛋白的连接位点水解蛋白来切割病毒蛋白,并且这种水解活性可以被许多药物抑制。目前很多药物(如格佐韦/格拉佐普韦、GZV等。)抑制NS3的蛋白水解活性,已被FDA批准用于治疗成人丙型肝炎
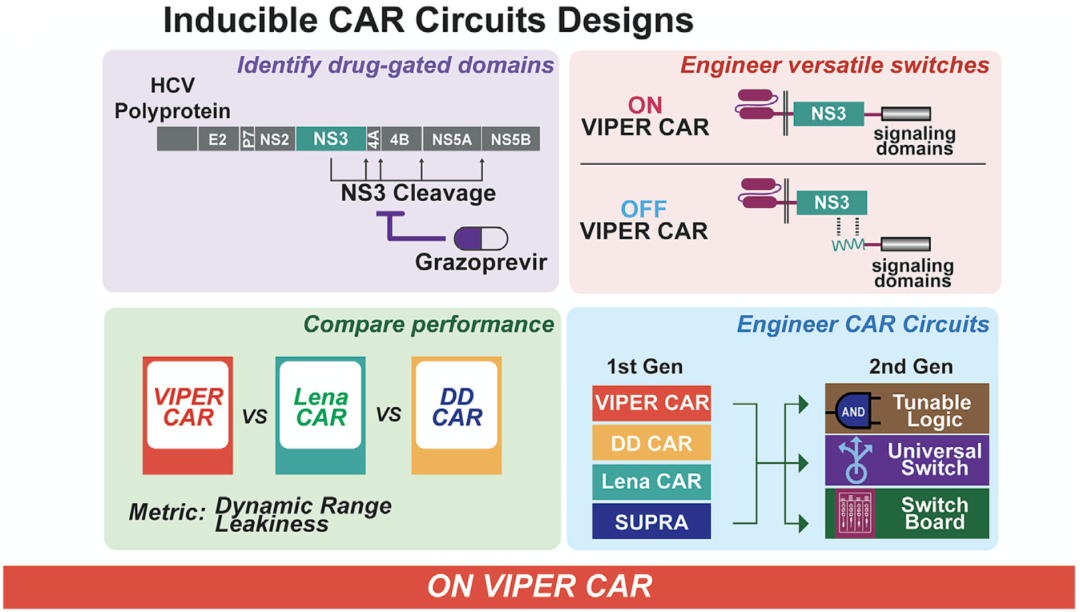
蝰蛇车系统的机理
其实NS3和CAR-T细胞的组合已经不是第一次提出了。和Jennifer R. Cochran和Crystal L. Mackall的团队[5]分别在Angewandte Chemie和Cell上发表了NS3蛋白酶控制的CAR系统的不同设计。
与以往报道不同的是,WONg的团队设计并验证了基本on或OFF VIPER CAR系统的功能和药物可控性,并在CRS动物模型上验证了传统CAR-T系统的有效控制。
此外,他们还进一步提出了更复杂的第二代VIPER CAR系统,具有多通道控制功能,以应对复杂多变的肿瘤细胞。
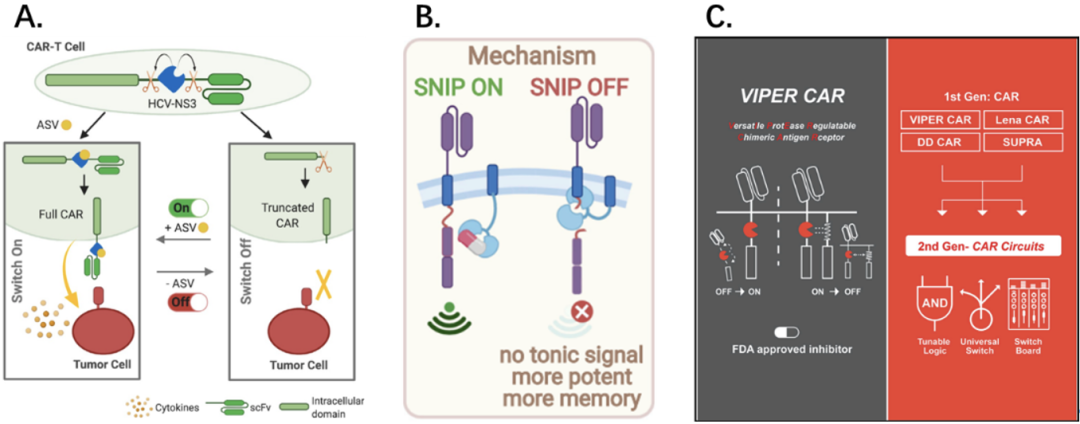
公开文献中不同设计的NS3蛋白酶控制CAR系统示意图
下图是上下车蝰蛇车的基本设计。系统(a)是一个单链系统。在没有药物的情况下,NS3起到酶消化的作用,CAR不能形成完整的信号转导。但在药物存在的情况下,NS3的水解被抑制,形成完整的CAR,起到抗肿瘤作用(即加入药物时,系统处于ON状态)。
OFF系统(B)是两个分离元件,将胞外抗原识别结构域与胞内CD3 结构域分别置于两个分离的元件,通过NS3和NS3结合肽连接。在不添加药物的情况下,NS3与靶向肽结合,连接两个分离元件,形成完整的CAR信号转导;有药物时,NS3被竞争性结合,CAR不完整,T细胞不能被激活(即添加药物时,系统处于 OFF 的状态)。
ON 和 OFF VIPER CAR机制示意图
体外实验显示VIPER CAR-T细胞系统具有肿瘤细胞杀伤能力,且其杀伤作用与药物剂量具有相关性。
而且移除药物后再次添加药物仍能恢复其功能,由此建立了由药物控制的可逆的VIPER CAR系统(下图为 ON 系统, OFF 系统得到相似结论)。小鼠体内实验进一步验证了上述结论。
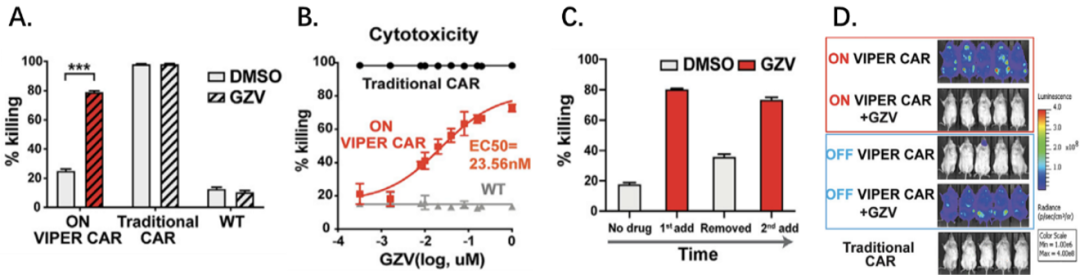
ON VIPER CAR系统药物可控性与功能验证
而对于大家非常关心的CAR-T安全性问题,他们利用CRS特异性小鼠模型验证了 OFF VIPER CAR系统,对传统CAR-T治疗不良反应CRS的有效改善。实验发现 OFF VIPER CAR系统加药后,分泌更少的与CRS相关细胞因子,小鼠的存活率也显著提高。
他们还将VIPER CARs与目前已有的临床相关药物门控CARs进行直接对比,证实VIPER CAR系统药物调控能力和体外杀伤能力最佳。
另外,鉴于VIPER CAR与其他临床相关药物门控CARs可以兼容,他们构建了靶向CD19和Her2的双靶向正交调控CAR。利用GZV调控的靶向CD19+细胞的 ON VIPER CAR,联合POM(泊马度胺,来那度胺类似物)调控的靶向Her2+细胞的 OFF VIPER CAR,通过两种药物的不同组合给药方式,实现了两种药物控制的、相互独立的双靶向抗肿瘤作用。
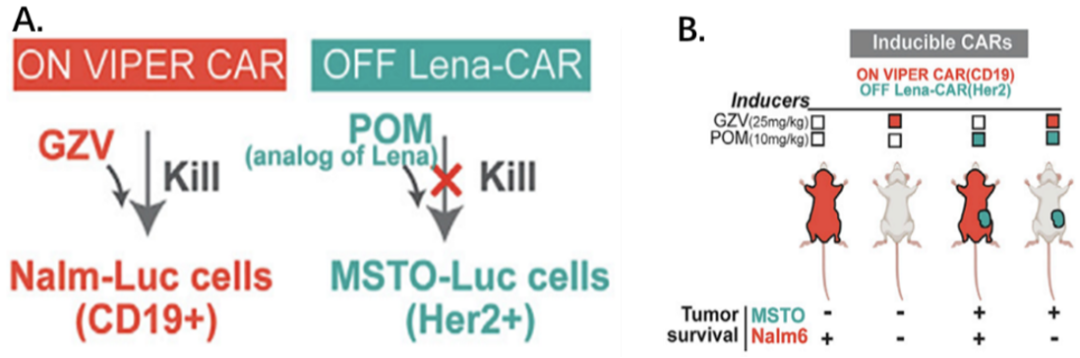
双靶向性药物门控CAR系统
最后,基于基础VIPER CAR他们进一步提出三种更复杂的 进阶版 二代VIPER CARs:
医药网新闻
- 相关报道
-
- 2025上海国内生物医药家当周13日在沪揭幕 (2025-10-14)
- 《癌症研究》:益生菌化解高脂饮食促癌的“命”!中山大学团队发现,约氏乳杆菌合成的鹅去氧胆酸,可以促进肠癌细胞凋亡 (2025-10-14)
- 挺进SCLC一线治疗!芦比替定重塑市场价值,国内合作方为绿叶制药 (2025-10-14)
- Nature子刊:同济大学戈宝学团队等揭示结核杆菌通过增强Treg细胞抑制功能,促进自身存活 (2025-10-13)
- Nature子刊:华中科技大学发现肝癌免疫治疗新靶点 (2025-10-13)
- 跨省异地就医若何间接报销?国度医保局解答 (2025-10-13)
- 宁夏出台步伐深入药械监管改造匆匆进医药家当高质量倒退 (2025-10-13)
- 国度药监局对于生脉颗粒(党参方)和调经活血胶囊转换为非处方药的布告 (2025-10-13)
- 给蛋白质装“逻辑大脑”!Nature 子刊突破:精准给药像编程,多重验证不误伤健康细胞 (2025-10-13)
- 破解肥胖相关血管收缩难题!Compr Physiol:脂肪小体经神经酰胺/ROS/KATP通道轴驱动血管高收缩性 (2025-10-13)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















