《自然·癌症》:我国科学家发现“癌王”对“合成死亡”敏感! |
 |
来源:奇点蛋糕2022-11-16 1:53
在本研究中,我们发现了metl16的一个新功能,即metl16可以通过与DNA同源重组的关键酶MRE11相互作用来抑制DNA的同源重组修复。
作为最常见的RNA修饰之一,RNA腺嘌呤碱基在氮6位的甲基化(简称m6A)自2011年重新进入研究者视野以来,一直是研究的重点[1]。作为第二个发现的RNAm6A甲基转移酶[2-3],METTL16最近成为生命科学的研究热点[4-5]。
近日,美国梅奥诊所肿瘤科楼振坤、上海同济医学院袁剑、华中科技大学同济医学院附属协和医院陶凯雄领导的研究团队在杂志《自然 癌症》上发表了METTL16功能的最新研究成果[6]。
他们发现METTL16可以与同源重组修复的关键酶MRE11相互作用,以不依赖于其甲基转移酶功能的方式,通过其结合的RNA抑制其核酸外切酶活性,从而抑制DNA的同源重组修复。在DNA损伤的情况下,metl16可以被ATM激酶磷酸化,导致其构象发生变化,RNA结合能力下降,然后MER11不再被metl16抑制。
例如,在疾病模型中,他们发现METTL16的表达可以提高胰腺癌细胞对PARP抑制剂Olapari的敏感性,特别是在与化疗药物吉西他滨联合使用时。
奥拉帕尼已被美国批准用于同源重组缺陷型胰腺癌[7]。然而,只有大约10%的胰腺癌患者具有同源重组缺陷型突变,大多数胰腺癌患者被排除在这种治疗之外。因此,METTL16具有抑制DNA同源重组修复功能的发现,对于没有同源重组缺陷突变的胰腺癌患者使用PARP抑制剂具有重要意义。

报纸首页截图
接下来,让我们看看楼振坤、袁剑和陶凯雄的团队是如何开展这项研究的。
受RNA m6A修饰的DNA修复功能研究的启发[8-9],研究人员决定探索m6A修饰酶(METTL3-METTL14,METTL16)在胰腺癌DNA损伤中的作用。
通过分析胰腺癌微阵列样本中DNA双链断裂(DSB)的水平以及met L3-metl 14和Metll16的表达水平,研究人员发现Metll16高表达的样本中DSB水平更高。此外,DSB修复报告系统(DR-GFP/EJ5-GFP)的结果表明,敲除HEK293T细胞中的METTL16可以显著提高同源重组介导的DNA修复效率(HDR)。考虑到METTL16对DNA损伤修复的影响尚未见报道,研究人员决定进一步探索。
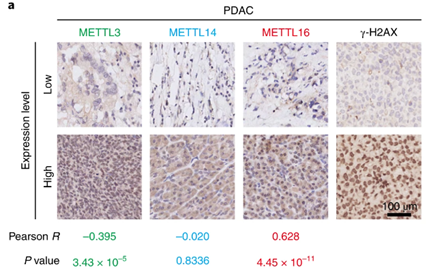
METTL16在胰腺癌中的表达水平与DSB水平呈正相关。
首先,研究人员构建了一个敲除Metl16并在敲除后重新表达Metl16的细胞系,并评估了辐射诱导的DSB水平。
结果显示,辐射处理8小时后,与野生型细胞相比,METTL16缺陷(KO)细胞中-H2AX(DSB标记)的染色水平显著降低。同时,经4小时辐射处理后,KO的DNA拖尾现象较野生型有明显改善。然而,在METTL16重新表达后,H2AX水平的变化和DNA拖尾现象被逆转。
这些结果表明METTL16可以抑制DNA修复。
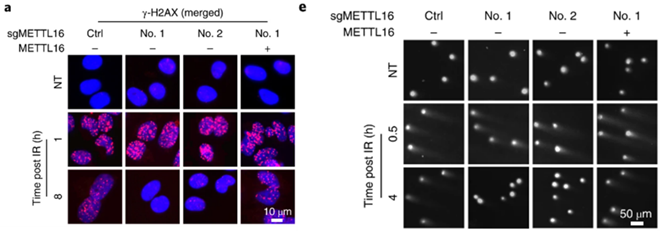
敲除METTL16可以增强DNA修复,降低DSB水平。
序列分析显示METTL16具有两个潜在的ATM/ATR磷酸化位点(Ser419和Ser455)。因此,研究人员推测METTL16可能受ATM/ATR调控。结果证明是真的。研究人员通过分析这两个位点的磷酸化状态,构建位点突变模型,发现ATM可以磷酸化METTL16上的Ser419位点,从而降低其对HDR的抑制作用。
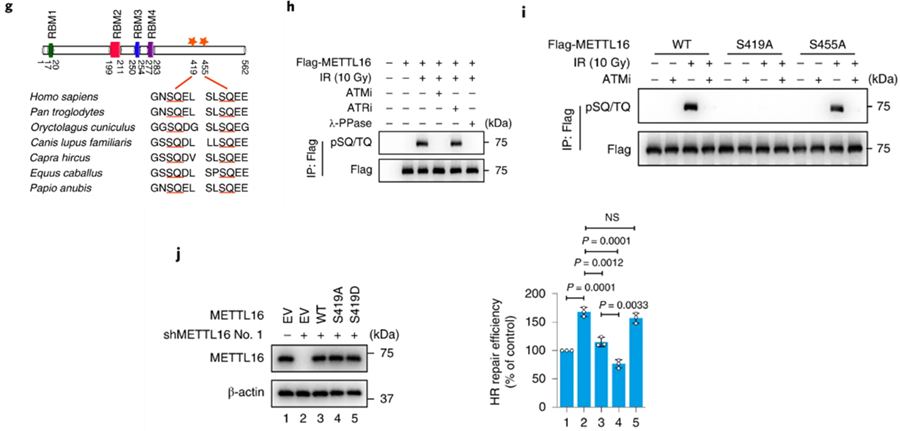
ATM可通过磷酸化METTL16减弱其对HR修复的抑制作用。
修复HDR DNA双链断裂
裂主要有三大步骤,链末端切除(end resection)、3 -单链入侵同源模板链(strand invasion)、Holliday结的分解(resolution of Holliday Junction)。那么,METTL16会影响HDR的哪个步骤呢?研究者们发现,辐射处理2h后,与METTL16正常表达的细胞相比,METTL16敲除的细胞中蛋白RPA32和RAD51水平显著增加,且重新表达METTL16能逆转这些变化。
蛋白RPA32是一种单链DNA结合蛋白,与DNA复制过程中或DNA损伤情况下产生的3 单链结合,从而起到稳定单链的作用,而RPA32染色水平的增加则意味着细胞中3 -单链的增加。这提示到,METTL16会抑制链末端切除。
另外,共沉淀实验结果显示,METTL16和链末端切除关键复合物MRN-CtIP中的MRE11存在相互作用,且辐射处理能减少这种相互作用。
这些结果说明,METTL16能够通过与MRE11互作,来抑制HDR修复DNA过程中的链末端切除。
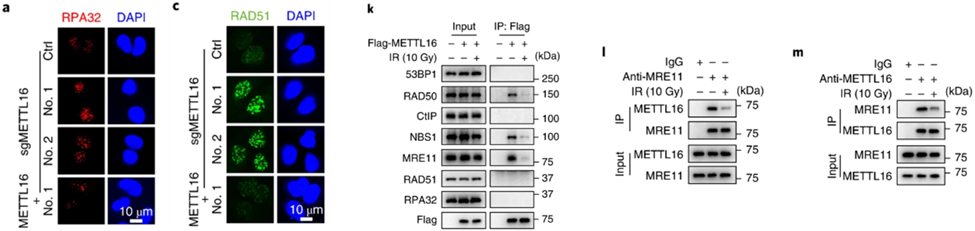
METTL16通过与MRE11的相互作用来抑制HDR中的链末端切除步骤
随之而来的问题是,METTL16是怎么和MRE11相互作用的呢?
研究人员从MRE11上存在的两个DNA结合域以及METTL16存在的四个RNA结合基序入手,通过DNase/RNase处理以及一系列的截短突变实验,证明METTL16与MRE11的相互作用是通过与这两者相结合的RNA实现的。另外,胞外核酸酶实验结果显示,METTL16-RNA复合体与MRE11结合后,会抑制MRE11核酸酶活性。
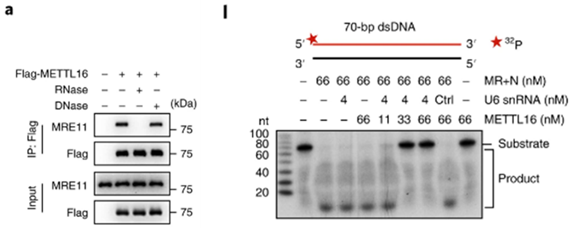
METTL16通过RNA和MRE11产生相互作用并抑制后者的核酸酶活性
开头提到,METTL16的主要功能是对RNA进行m6A修饰。然而研究者们发现,和野生型METTL16相比,丧失甲基转移酶活性的METTL16突变体(F187G),依然能够与MRE11相互作用,抑制链末端切除,进而抑制HDR效率。也就是说,METTL16和MRE11的相互作用并不依赖于METTL16的甲基转移酶活性。
另外,介导METTL16和MRE11相互作用的RNA是否存在m6A修饰,对这种相互作用也没有影响。反倒是ATM对METTL16的磷酸化,会降低其与RNA结合能力,进而减少METTL16和MRE11的相互作用。
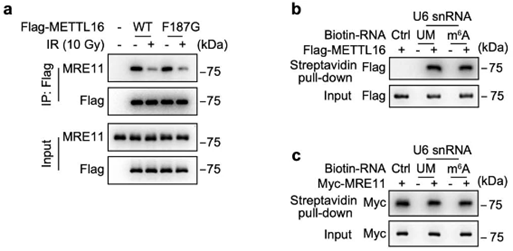
METTL16与RNA的结合,以及与MRE11的相互作用并不依赖METTL16的甲基转移酶活性或者RNA的m6A修饰
至此,研究人员已经确定了METTL16在HDR中扮演的角色:DNA损伤激活ATM后,ATM磷酸化METTL16并导致其构象改变,使得RNA从METTL16上原本的结合态分离出来,进而导致METTL16与MRE11的相互作用减少,MRE11从复合体中释放出来后参与HDR,修复DNA损伤。
考虑到METTL16对HDR的抑制作用,以及PARP抑制剂对HDR缺陷型肿瘤合成致死的特性,研究人员分析了PARP抑制剂奥拉帕利对表达不同水平METTL16的BRCA1/2野生型胰腺癌细胞的杀伤效果。
结果显示,高表达METTL16的细胞系对奥拉帕利更敏感,在高表达METTL16背景下敲除METTL16会降低细胞对奥拉帕利的敏感性,在低表达METTL16背景下过表达METTL16则会增加细胞对奥拉帕利的敏感性。METTL16表达水平与对奥拉帕利的敏感性的这种正相关在小鼠胰腺癌模型中也得到了证实。
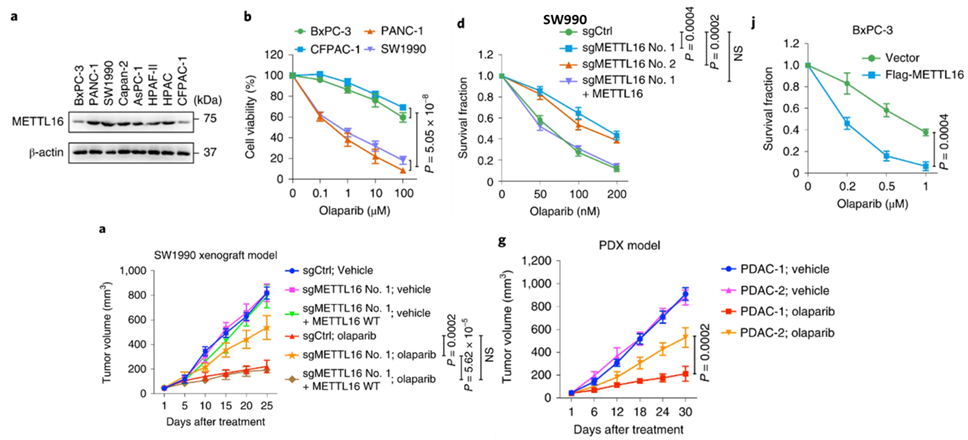
胰腺癌细胞和肿瘤中METTL16的表达水平与对奥拉帕利的敏感性呈正相关
最后,研究人员评估了METTL16表达水平对胰腺癌患者生存期,以及对胰腺癌临床疗法效果的影响。
结果显示,胰腺癌患者的METTL16表达水平与其生存期呈正相关。另外,动物模型结果显示,高表达METTL16的肿瘤对吉西他滨单药、奥拉帕利单药更敏感,肿瘤发展减缓。在高表达METTL16的肿瘤中,吉西他滨+奥拉帕利的联合使用可以使肿瘤衰退,显著延长小鼠生存期。
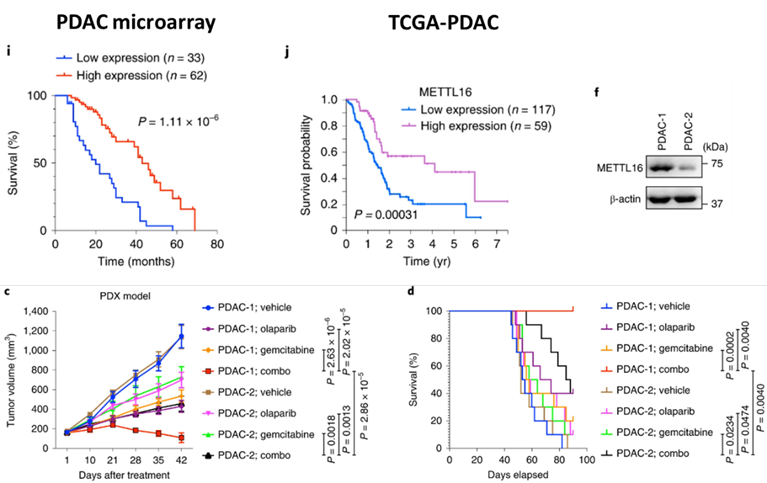
高表达METTL16的胰腺癌患者具有较好生存期,也预示着对胰腺癌治疗药物更高的敏感性
总的来说,这项研究发现了METTL16的一项全新功能,即METTL16会通过与DNA同源重组关键酶MRE11的相互作用来抑制DNA的同源重组修复。
同时,该研究揭示了METTL16的水平是一个潜在的胰腺癌预后指标,且吉西他滨+奥拉帕利的联合使用可能是治疗高表达METTL16胰腺癌的有效策略。
参考文献:
[1] Jiang X, Liu B, Nie Z, et al. The role of m6A modification in the biological functions and diseases.Signal Transduct Target Ther. 2021;6(1):74. Published 2021 Feb 21. doi:10.1038/s41392-020-00450-x
[2] Warda AS, Kretschmer J, Hackert P, et al. Human METTL16 is aN6-methyladenosine (m6A) methyltransferase that targets pre-mRNAs and various non-coding RNAs.EMBO Rep. 2017;18(11):2004-2014. doi:10.15252/embr.201744940
[3] Pendleton KE, Chen B, Liu K, et al. The U6 snRNA m6A Methyltransferase METTL16 Regulates SAM Synthetase Intron Retention.Cell. 2017;169(5):824-835.e14. doi:10.1016/j.cell.2017.05.003
[4] Su R, Dong L, Li Y, et al. METTL16 exerts an m6A-independent function to facilitate translation and tumorigenesis.Nat Cell Biol. 2022;24(2):205-216. doi:10.1038/s41556-021-00835-2
[5] Satterwhite ER, Mansfield KD. RNA methyltransferase METTL16: Targets and function.Wiley Interdiscip Rev RNA. 2022;13(2):e1681. doi:10.1002/wrna.1681
[6] Zeng X, Zhao F, Cui G, et al. METTL16 antagonizes MRE11-mediated DNA end resection and confers synthetic lethality to PARP inhibition in pancreatic ductal adenocarcinoma.Nat Cancer. 2022;3(9):1088-1104. doi:10.1038/s43018-022-00429-3
[7] Golan T, Hammel P, Reni M, et al. Maintenance Olaparib for GermlineBRCA-Mutated Metastatic Pancreatic Cancer.N Engl J Med. 2019;381(4):317-327. doi:10.1056/NEJMoa1903387
[8] Zhang C, Chen L, Peng D, et al. METTL3 and N6-Methyladenosine Promote Homologous Recombination-Mediated Repair of DSBs by Modulating DNA-RNA Hybrid Accumulation.Mol Cell. 2020;79(3):425-442.e7. doi:10.1016/j.molcel.2020.06.017
[9] Yu F, Wei J, Cui X, et al. Post-translational modification of RNA m6A demethylase ALKBH5 regulates ROS-induced DNA damage response.Nucleic Acids Res. 2021;49(10):5779-5797. doi:10.1093/nar/gkab415
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 碧迪医疗首款港澳药械通器械获批,中国恶性胸腔积液治疗实现全球同步 (2025-10-14)
- Cell子刊:华西医院仝爱平/牛挺团队开发三特异性NK细胞接合器,安全有效治疗T细胞肿瘤 (2025-10-14)
- 复旦张军平:人类是硅基生命过渡体? (2025-10-14)
- 棕榈酸喂出斑马鱼脂肪肝,跨物种复现人鼠关键通路!Sci Rep揭示代谢相关脂肪性肝病研究新工具 (2025-10-14)
- 广州医科大学最新Nature Genetics论文:揭开食管癌转移新机制,为食管癌诊疗带来新思路 (2025-10-14)
- 2025上海国内生物医药家当周13日在沪揭幕 (2025-10-14)
- 《癌症研究》:益生菌化解高脂饮食促癌的“命”!中山大学团队发现,约氏乳杆菌合成的鹅去氧胆酸,可以促进肠癌细胞凋亡 (2025-10-14)
- 挺进SCLC一线治疗!芦比替定重塑市场价值,国内合作方为绿叶制药 (2025-10-14)
- Nature子刊:同济大学戈宝学团队等揭示结核杆菌通过增强Treg细胞抑制功能,促进自身存活 (2025-10-13)
- Nature子刊:华中科技大学发现肝癌免疫治疗新靶点 (2025-10-13)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















