《神经元》:厦大团队开发鼻腔给药tau蛋白抗体,可有效改善小鼠阿尔茨海默病病理 |
 |
来源:奇点糕 2024-04-29 09:10
该研究发现,以p-tau 217为靶点的被动免疫治疗是一种改善AD神经退行性病变的有效手段。近期,厦门大学神经科学研究所赵颖俊团队发表了一项重要研究成果,他们开发了一种特异性靶向p-tau 217的单克隆抗体 mAb2A7。
通过鼻腔给药的方式将mAb2A7成功递送到雄性tau病理小鼠(PS19)的大脑后,研究团队发现,mAb2A7治疗不仅可以改善小鼠的tau病理,还能抑制其导致的神经元死亡和脑萎缩,逆转了小鼠的认知障碍,改善了小鼠的运动功能,恢复了小鼠大脑的蛋白稳态。
研究发表在《神经元》上。

论文首页截图
tau蛋白是一种高度可溶的微管相关蛋白,主要在神经元中表达。正常情况下,健康的tau蛋白会结合在微管上,用于稳定微管的结构。但在病理情况下,比如在磷酸酶的作用下,tau蛋白出现过度磷酸化,从微管上脱落,聚集形成了神经纤维缠结,疾病就这样发生了。
因此,特异性靶向磷酸化的tau蛋白可能是治疗tau病理相关疾病的有效手段。既往研究显示,在AD的早期阶段,患者的脑脊液和血浆中会出现p-tau 217水平升高的现象,此外,与p-tau 181相比,脑脊液中p-tau 217水平与AD患者脑内tau沉积的关系更为密切。
因此,赵颖俊团队打算从p-tau 217入手,试图开发出针对p-tau 217的tau蛋白抗体疗法。
有了想法后,研究团队筛选出了一种可以和人类p-tau 217特异性结合,且具有高亲和力的抗体mAb2A7。通过使用mAb2A7进行超灵敏单分子检测量化AD患者脑脊液和血液中的p-tau 217水平后,研究团队发现,与非痴呆对照组相比,AD患者脑脊液和血液中p-tau 217水平显著升高。
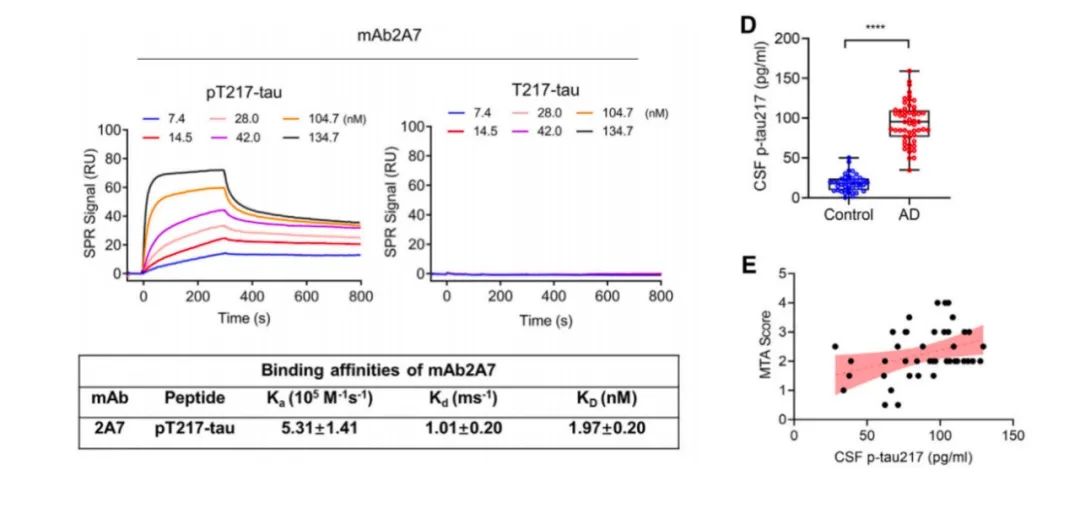
进一步分析显示,AD患者脑脊液中的p-tau 217水平与海马萎缩(内侧颞叶萎缩量表MTA评分)和认知损伤(精神状态检查量表MMSE评分)成正相关。
以上研究结果表明,p-tau 217水平与AD的神经退行性病变密切相关,这也预示着,p-tau 217是治疗AD的潜在靶点。
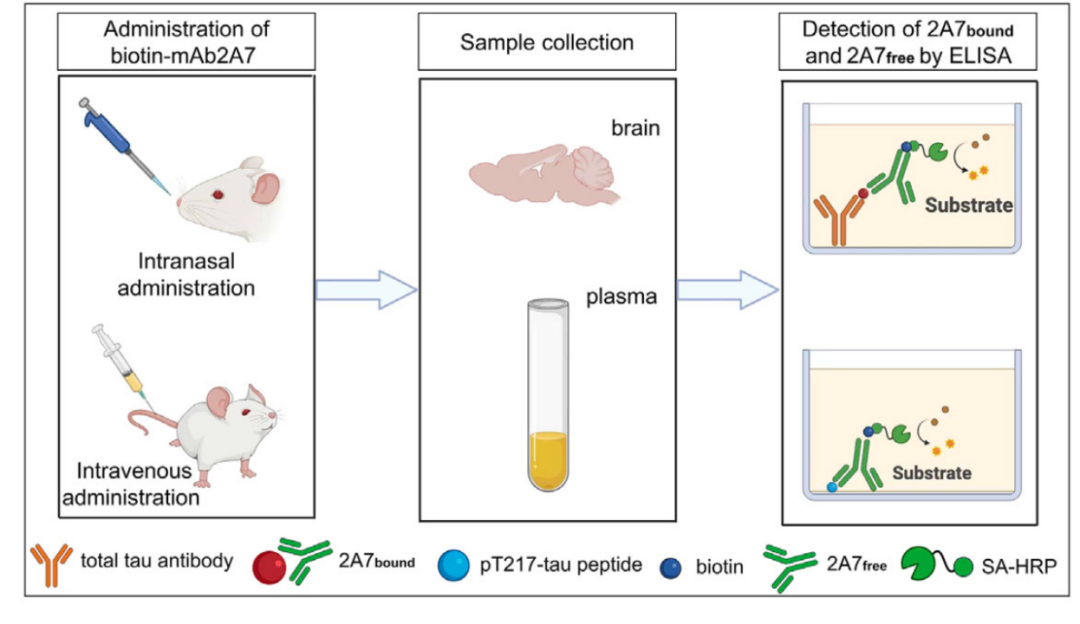
接下来,研究团队想评估一下mAb2A7的疗效。于是,研究人员构建了PS19 tau病理小鼠模型。由于雄性PS19小鼠tau蛋白磷酸化出现的比雌性小鼠更早,因此,研究团队决定使用雄性PS19小鼠进行所有的动物试验。此外,研究团队还对给药途径进行了探索,结果发现,鼻腔给药的方式能更高效地将抗体递送进入小鼠大脑。
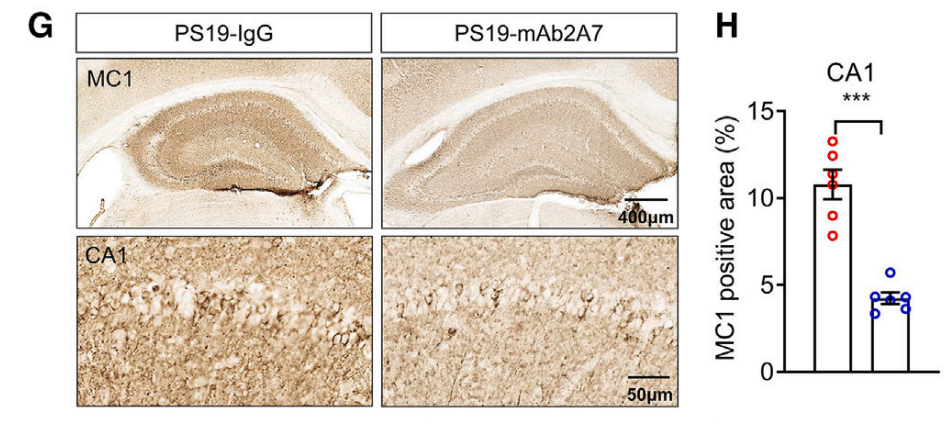
通过向5个月大的雄性PS19小鼠鼻腔注射mAb2A7(0.6 mg/kg/3天,持续3个月或5个月),研究团队发现,与对照组(注射IgG)相比,mAb2A7治疗显著减少了PS19小鼠海马区磷酸化tau蛋白的沉积。
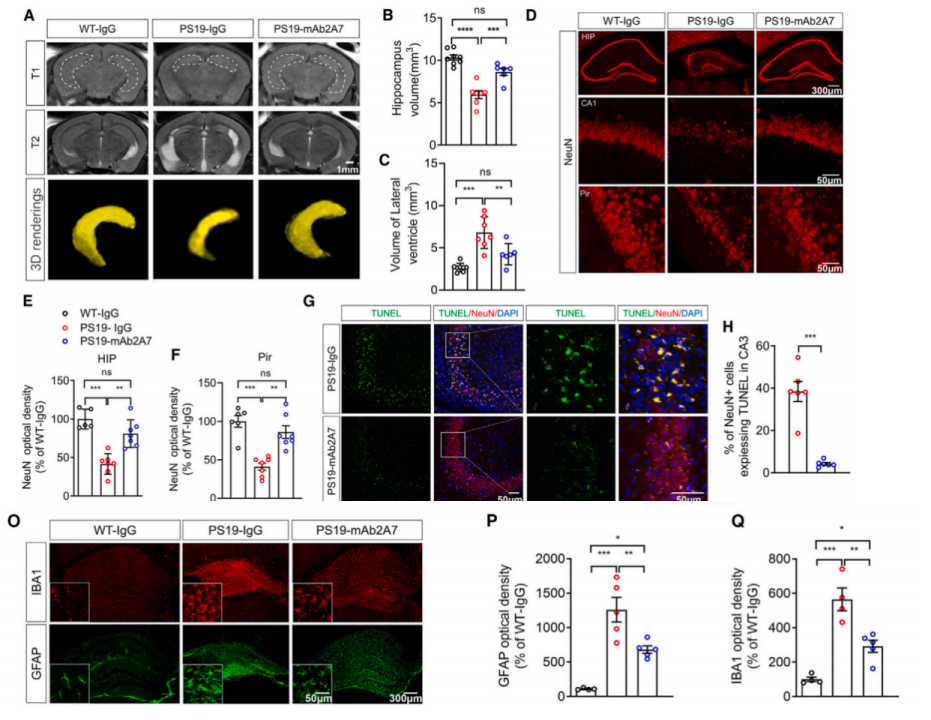
此外,在随后的包括生化分离试验、核磁共振成像分析、染色等在内的多项实验结果显示,mAb2A7治疗不仅有效减少了PS19小鼠大脑中不可溶的p-tau和总tau水平,还减少了PS19小鼠因tau病理产生的脑萎缩。更重要的是,mAb2A7治疗能显著减轻神经元的丢失和凋亡以及突触损伤。
鉴于AD的另一个重要的病理特征为脑内的神经炎症,研究团队通过评估发现,mAb2A7治疗可显著减少小胶质细胞的激活,降低炎症因子的表达水平。
对PS19小鼠进行的多项行为学分析也显示,mAb2A7治疗不仅可减轻PS19小鼠的绝望或抑郁状态,还能逆转PS19小鼠的认知功能(治疗后新物体识别测试和水迷宫测试中表现与野生小鼠一致),并改善小鼠的运动能力。
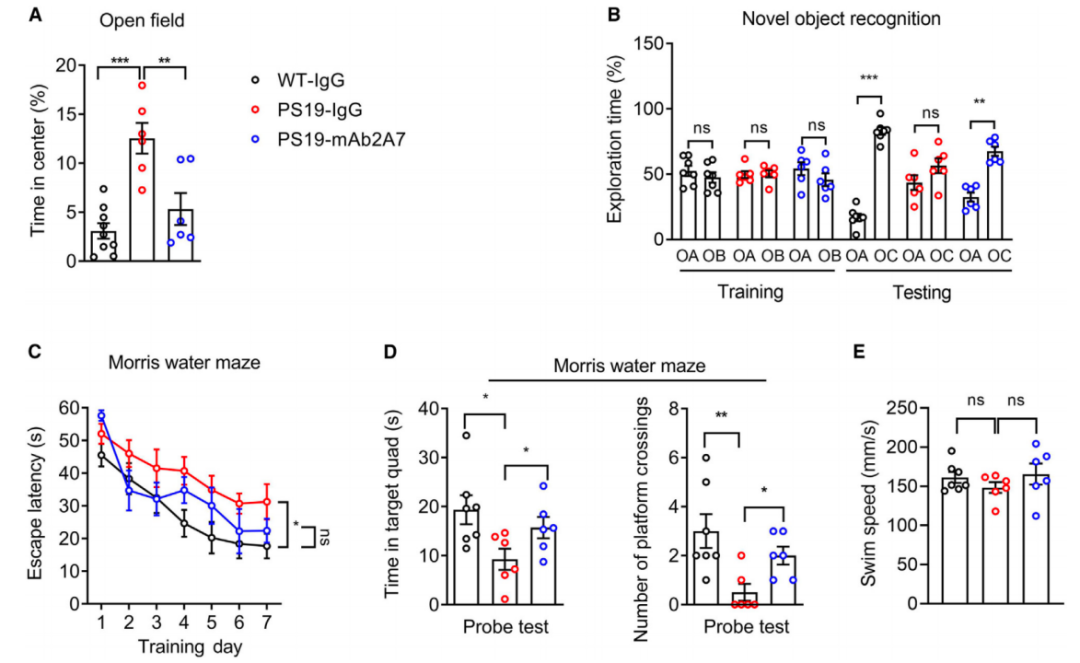
总之,以上结果均验证了,以p-tau 217为靶点的被动免疫疗法可改善小鼠的tau病理及相关的神经退行性病变。
最后,研究对PS19小鼠和野生小鼠的海马组织进行了蛋白质组学分析,结果发现,mAb2A7主要通过上调突触和神经元功能相关的蛋白表达,以及下调氧化应激和细胞凋亡相关的蛋白表达来恢复PS19小鼠大脑中的蛋白稳态。
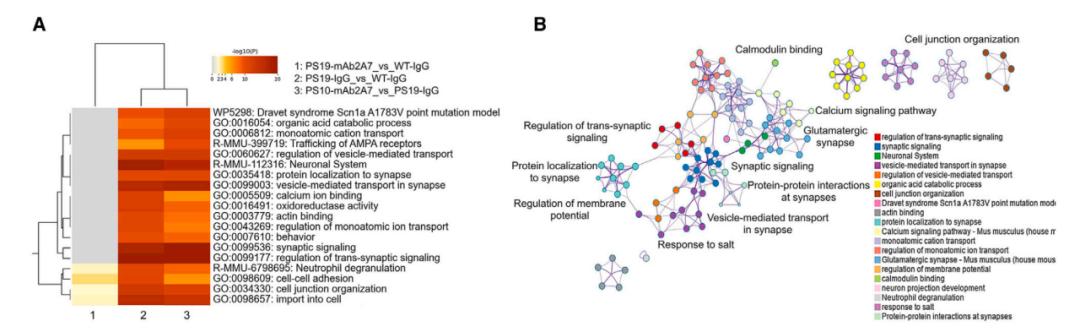
综上,该研究发现,以p-tau 217为靶点的被动免疫治疗是一种改善AD神经退行性病变的有效手段。
不过本文作者也表示,除p-tau 217外,其他过度磷酸化的tau蛋白,p-tau 181和p-tau 231也可能导致神经元损伤,未来还需要对这些磷酸点位的作用和致病机制进行分析。但不管怎么说,该研究结果无疑为AD的防治提供了新的方向。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:DNA甲基化“随机时钟”——EVOFLUX破译肿瘤演化史,重塑临床预后新维度 (2025-09-13)
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















