Nat Commun:在抗肿瘤治疗中整合靶向抗菌药物实现长期无复发生存 |
 |
来源:100医药网 2024-05-29 10:38
该研究揭示了肿瘤驻留细胞内微生物群靶向抗菌药物在肿瘤抑制中的关键作用,为TME的免疫调节开辟了一条非常规途径,并为癌症的完全治愈提供了途径。人类体内生活着数以万亿计的微生物,微生物群及其对各种生理功能、疾病、衰老、情感和认知的影响长期以来一直是人们关注的焦点。特别是,肿瘤驻留的细胞内微生物群(TRIM)最近引起了相当大的关注,因为它是致癌的重要因素。TRIM可通过血液循环从肿瘤周围组织迁移或穿过肿瘤内渗漏的脉管系统滞留在肿瘤内,而肿瘤微环境抑制(TME)则为TRIM提供了一个避难所。
越来越多的证据表明,TRIM可以降低化疗的疗效,增强药物对正常组织的毒性,促进促炎反应和的增殖。通过调节肠道微生物群来增强抗癌疗效和应答已经取得了重大进展。尽管如此,TME中细菌杀灭对肿瘤抑制的影响仍不清楚。
消除TRIM的常用策略依赖于全身剂量的。由于缺乏靶向性,全身剂量可诱发一系列负面效应,包括肠道益生菌缺乏、体内平衡破坏、疾病易感性、耐药等,尤其是对恶性。此外,抗生素的使用会影响免疫检查点抑制在抗癌治疗中的效果,并严重降低化疗对瘤和的疗效。因此,针对trim的抗菌剂是理想的,但尚未实现。
除了短期抑制率,最终的抗肿瘤目标是长期无复发生存,这需要持久的免疫记忆来对抗复发以及针对癌症转移的全身免疫反应。近年来发展的各种治疗方法,如化学动力疗法(CDT)和光热疗法(PTT),显示出显着的短期疗效;然而,TME中残留的或突变细胞仍然会导致肿瘤复发的高风险。
为了提高无复发生存率,已经提出将这些抗肿瘤疗法与基于使用免疫刺激药物(如免疫调节剂、免疫检查点阻断剂、抗原等)的免疫激活相结合。目前尚无trimm靶向抗菌药物联合抗的先例。抗肿瘤效果和免疫系统对这种组合的反应是一个悬而未决的问题。

图片来源:
近日,来自哈尔滨工业大学化学化工学院的研究者们在Nat Commun杂志上发表了题为 Long-term relapse-free survival enabled by integrating targeted antibacteria in antitumor treatment 的文章,该研究揭示了肿瘤驻留细胞内微生物群靶向抗菌药物在肿瘤抑制中的关键作用,为TME的免疫调节开辟了一条非常规途径,并为癌症的完全治愈提供了途径。
肿瘤驻留细胞内微生物群(TRIM)在癌变中的作用引起了极大的兴趣。然而,trimm靶向抗菌药物对肿瘤微环境(TME)中肿瘤抑制和免疫调节的影响仍未被探索。在此,研究者报告了长期无复发生存,通过协调抗菌药物与抗肿瘤治疗,解决了和模型中TRIM引起的加重免疫抑制和肿瘤过度生长。
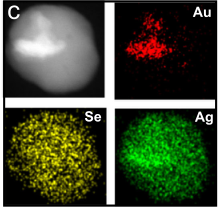
Au@Ag2Se-FA 纳米颗粒的表征
图片来源:
研究者发现TRIM可以减少T细胞和m1样tam的数量,增加m2 - tam的数量,上调抗炎细胞因子,下调促炎细胞因子,从而加重大肠杆菌注射小鼠和非无菌环境下饲养小鼠的TME免疫抑制。将trimm靶向抗菌药物整合到单一药物的抗肿瘤治疗中,可有效解决免疫抑制和肿瘤过度生长问题。
明显的T细胞免疫应答和m2 -to- m1样的TAM复极化被激活,全身免疫刺激作用被限制在合理的时间内。这种治疗可以引发长期的免疫记忆,防止肿瘤复发,并对的迁移产生强烈的全身抗反应。患者无复发生存期 700天。乳腺癌和前列腺癌都显示出治疗的有效性。

结合trimm靶向抗菌药物与抗肿瘤治疗的示意图
图片来源:
综上所述,本研究开辟了在不使用免疫刺激药物的情况下有效激活TME的途径,并将trim靶向抗菌药物与抗肿瘤治疗联系起来,强调了抗菌药物在免疫调节和肿瘤抑制中的重要作用。trimm靶向抗菌药物与免疫调节之间的关系比本工作所提出的更为深刻和复杂,值得进一步研究。
尽管免疫疗法在特定类型的恶性肿瘤中显示出相当大的临床前景,但在许多其他病例中,它们的效果要差得多。这项工作的发现可能会对免疫疗法的无效提供更深入的认识,并为临床根治性抗肿瘤治疗提供突破。 ( 100yiyao.com)
参考文献:
Yuanlin Wang et al. Long-term relapse-free survival enabled by integrating targeted antibacteria in antitumor treatment. Nat Commun. 2024 May 17;15(1):4194. doi: 10.1038/s41467-024-48662-x.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:DNA甲基化“随机时钟”——EVOFLUX破译肿瘤演化史,重塑临床预后新维度 (2025-09-13)
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















