仅需「坚持8周耐力锻炼」,就能由内而外的改变!Nature多组学研究:运动从基因表达到蛋白质功能重塑我们的身体 |
 |
仅需「坚持8周耐力锻炼」,就能由内而外的改变!Nature多组学研究:运动从基因表达到蛋白质功能重塑我们的身体
来源:100医药网 2024-08-14 09:20
这项研究涵盖了19种组织、25种分子平台和4个训练时间点的9,466项检测,发现了数以千计的共享和组织特异性分子改变,并在多个组织中发现了性别差异。在这个快节奏的时代,健康已成为全民热议的话题,而运动作为不打针不吃药、且终生受益的良方,一直被广为推崇。
以往研究已分别从转录组学、表观基因组学、蛋白质组学和代谢组学等各种 组学 平台证实,运动几乎可以影响人体内所有的器官系统[1],其强大的功效包括延缓衰老、增强力、降低全因死亡以及癌症风险、减少心脏代谢和神经系统疾病等等。
然而,迄今为止的研究通常仅在某个特定时刻覆盖一两个组学领域,并且倾向于侧重单一性别和组织,例如运动对男性或女性骨骼肌、心脏或血液的影响,这也导致我们仍缺乏能全面理解运动训练诱导的适应性分子变化。
为满足这一需求,近期,来自美国斯坦福大学、麻省理工学院和哈佛大学等的研究人员就深入探索了「耐力训练」对身体多层面的影响,揭示了运动带来的不仅仅是体形的变化,更是一场细胞级的革命!本研究发表于Nature杂志,题为 Temporal dynamics of the multi-omic response to endurance exercise training 。(文章稍长,请耐心阅读哦~)

9,466次试验,涉及19种组织和25种分子平台
本研究由MoTrPAC研究小组进行,实验对象是六月龄的雄性和雌性Fischer 344大鼠,这些大鼠被安排进行为期1、2、4或8周的跑步机耐力训练,并分别在最后一次训练的48小时后收集样本(血液、血浆、胃肠肌、心脏、肝脏、白色脂肪组织、肾脏、肺部、棕色脂肪组织、海马区等)。同时,本研究设定性别匹配的久坐未训练大鼠作为对照组。
研究人员分别从基因组学、蛋白质组学、代谢组学以及蛋白质免疫测定技术等分析手段出发,总共进行了9,466次试验,涉及19种组织和25种分子平台。以上所有的数据和分析结果均存储在公共数据库中,供公众访问和进一步研究(https://motrpac-data.org/)。
多个组织耐力训练反应分析
在深入探究多种组织对训练反应的独特特性时,科研团队对六种核心组织进行了细致的分子层面剖析:腓肠肌(小腿肌肉的主要组成部分)、心脏、肝脏、白色脂肪组织、肺和肾脏。这一系列组织涵盖了人体主要的功能系统,从能量生产到代谢调控,再到免疫防御。通过这一研究,别出7,115个独特的基因,它们在训练响应中展现出活跃的变化。
令人瞩目的是,超过三分之二的这些基因表现出了组织特异性,意味着它们的响应模式在特定组织中独具特色。白色脂肪组织在这之中脱颖而出,拥有最多的特异性基因,这一现象暗示了脂肪组织在耐力训练中扮演着一个复杂而关键的角色,它不仅负责能量的存储与释放,还在运动适应过程中承担着更为精细的调节任务。
更进一步,研究者们揭示了2,359个基因在至少两种组织中展现了差异化的特征,这表明了分子适应性变化在不同组织间的交叠和协同。在这之中,肺和白色脂肪组织之间共享了最多的一组独特基因,共计249个,这些基因显著富集于免疫相关的生物途径中。
这一发现提示我们,运动不仅强化了肌肉和心肺功能,还深刻地影响着免疫系统的布局与运作,尤其是在促进肺部的抗炎状态和脂肪组织中的免疫细胞动员方面,展现了运动对整体健康维护的多维度贡献。
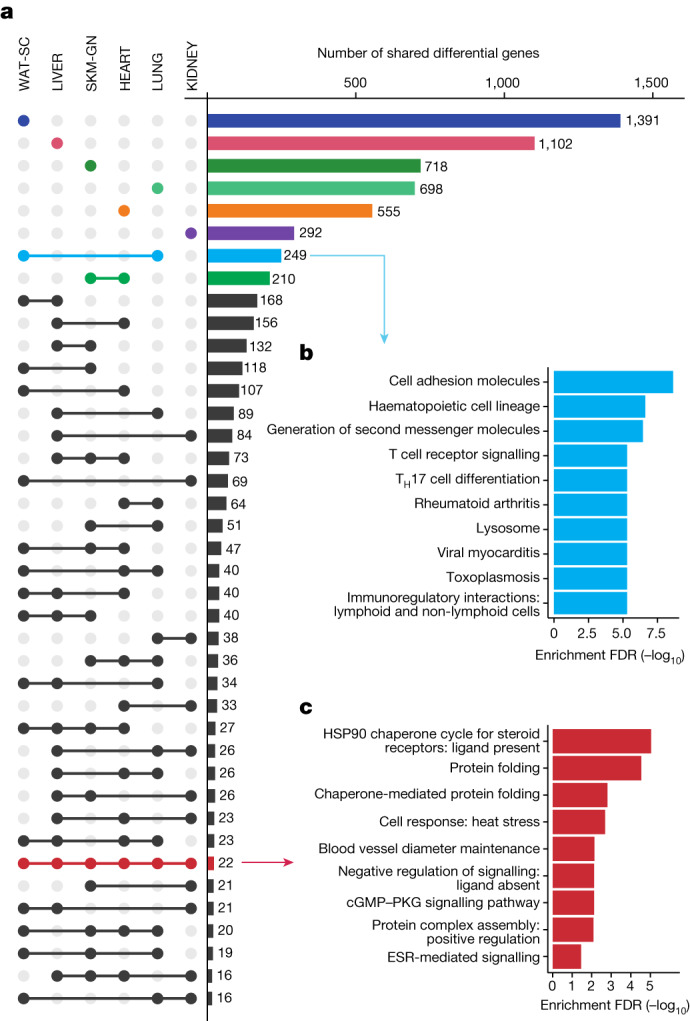 图1:多组织对耐力运动训练
图1:多组织对耐力运动训练
尤为值得一提的是,研究精确定位了22个基因,它们在全部六种组织中均呈现出训练调节的迹象,尤其与热休克反应密切相关。这些基因的普遍响应,例如热休克蛋白家族成员HSPA1B和HSP90AA1的显著上调,凸显了运动作为一种全身性刺激,能够激活机体广泛的保护机制。
利用蛋白组、转录组数据,比较不同组织中显著富集的转录因子,研究人员观察到,血液中与造血相关的转录因子GABPA、ETS1、KLF3和ZNF143显著富集,这些转录因子调控着血细胞的生成与成熟,进而影响着整个机体的循环健康与免疫响应。这暗示了耐力训练不仅增强了肌肉与心肺功能,还可能通过优化造血环境,间接提升了全身的免疫状态与抗病能力。
在心脏和骨骼肌这两个直接参与运动的 前线 组织中,则出现了与肌肉生长和功能密切相关的Mef2家族转录因子基序的富集。Mef2家族,特别是MEF2C,作为肌肉发育与维持的核心调控者,其活性的增强预示着训练对肌肉纤维的重塑与强化,从而支持了更高强度的体力活动。
此外,研究人员还发现,在肝脏中,与再生相关的调控因子EGFR1、IGF和HGF的磷酸化水平上升,而这些因子正是细胞增殖与修复的关键驱动力。
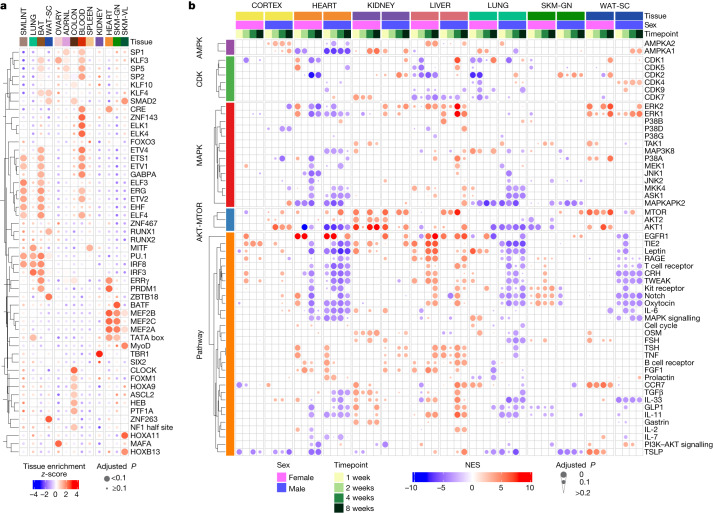
图2:耐力训练调节的信号通路
研究结果的一致性
研究人员将结果与现有的运动研究和疾病本体论注释相结合,系统地评估了数据的转化价值,最终结果支持大鼠数据与人类研究的高度一致性及其与人类疾病的相关性。
运动训练反应:时间和性别的差异
研究发现,许多组织在其训练反应中显示了性别差异:在8周的训练调节特征中58%表现出性别分化。在训练的第1 -2周,雌鼠和雄鼠的小肠和血浆已经有较多的变化;而棕色和白色脂肪组织中的分别上调和下调的特征仅在第8周才能观察到。
对于肾上腺组织,雌鼠和雄鼠在第1周时就可以观察到最大的相反的差异特征;而其他组织,比如横纹肌肌肉组织(腓肠肌、股外侧肌和心脏)则具有相对一致性的上调特征。促炎细胞因子等特异性细胞因子在组织中也表现出与性别相关的变化,例如雌鼠会在第1-2周受到差异性调节,而雄鼠则是在第4-8周。
总体上,研究数据表明了运动对人体的影响可能存在着性别差异。
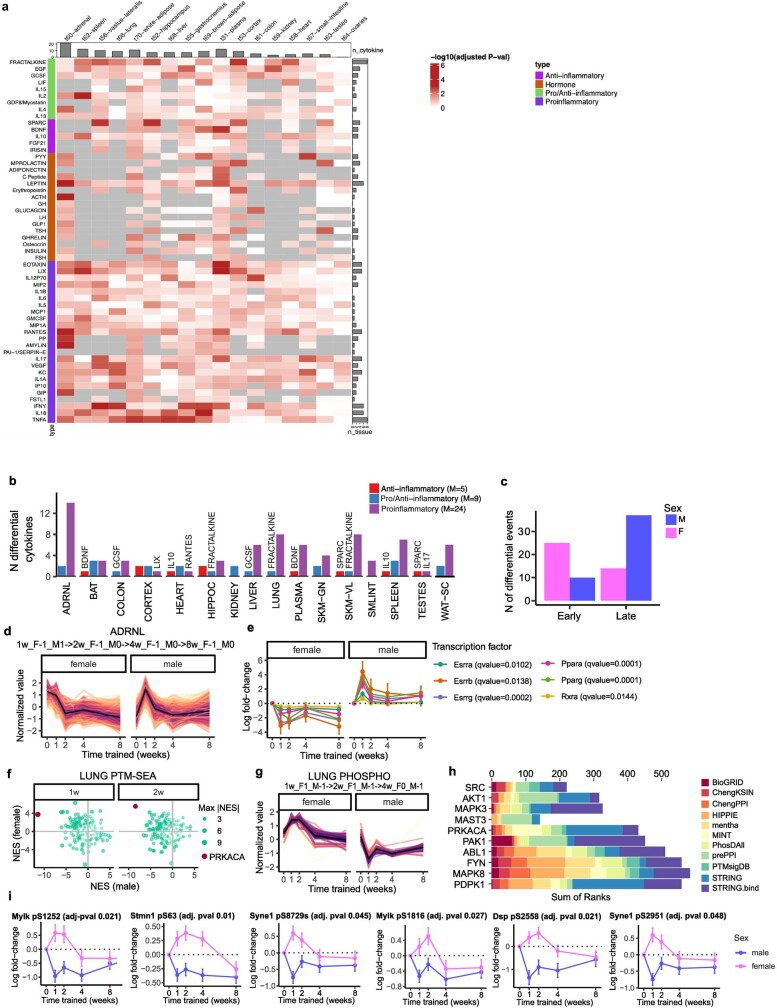 图3:耐力训练反应的性别差异
图3:耐力训练反应的性别差异
运动对于肝脏的 塑造
最后,研究人员总结了代谢组学和非代谢组学数据集的生物体代谢变化,发现肝脏中显著富集的代谢物种类最多,其次是心脏、肺和海马体。
聚焦于肝脏,研究者们发现了一系列引人注目的代谢模式转变。磷脂酰胆碱的含量升高,预示着细胞膜的流动性与稳定性得到了加强,这是肝脏在应对运动负荷时所采取的一种保护策略。与此同时,三酰甘油的减少则标志着脂肪分解活动的增强,这不仅有助于减轻肝脏负担,也为身体其他部位提供了更多的能量来源。更为有趣的是,过氧化物酶体的蛋白质丰度与乙酰化程度均有所提升,这些微小但至关重要的细胞器,在脂质代谢过程中扮演着核心角色,它们的活跃表明了肝脏正积极调整自身功能,以适应运动带来的代谢挑战。
总之,这些分子级的适应与变化,不仅仅是对运动刺激的即时反应,更是机体在长期运动训练中逐步进化和完善的结果。
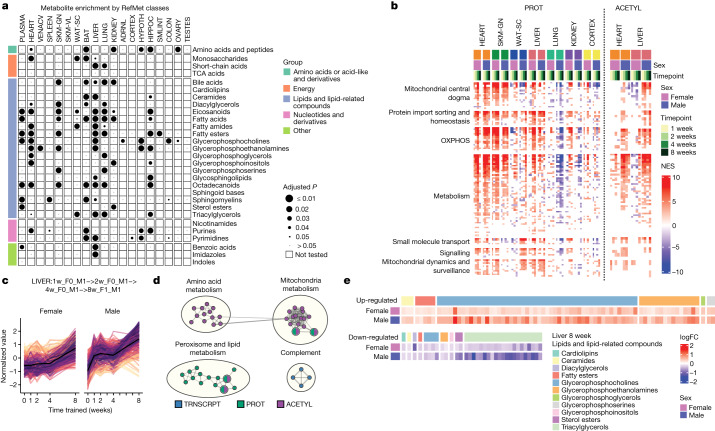 图4:耐力训练反应引起的新陈代谢变化
图4:耐力训练反应引起的新陈代谢变化
小结
这项研究涵盖了19种组织、25种分子平台和4个训练时间点的9,466项检测,发现了数以千计的共享和组织特异性分子改变,并在多个组织中发现了性别差异。
整体而言,研究突显了多组学方法揭示的独特训练反应,可为未来有关运动如何改善全身和特定组织健康的假设驱动研究提供支持。
总而言之,适当的运动训练对身体健康益处多多,大家赶紧动起来吧!
参考文献:
[1] Pedersen BK, Saltin B. Exercise as medicine - evidence for prescribing exercise as therapy in 26 different chronic diseases. Scand J Med Sci Sports. 2015;25 Suppl 3:1-72. doi:10.1111/sms.12581
[2] MoTrPAC Study Group; Lead Analysts; MoTrPAC Study Group. Temporal dynamics of the multi-omic response to endurance exercise training. Nature. 2024;629(8010):174-183. doi:10.1038/s41586-023-06877-w
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 【参会指南】9月26-27日,2025(第九届)细胞外囊泡前沿与转化大会(厦门站)即将开幕! (2025-09-18)
- 西湖大学最新Cell子刊论文:利用孕妇肠道菌群预测早产风险 (2025-09-17)
- Cell:高分子量tau蛋白抑制海马体神经元活动,导致阿尔茨海默病的认知衰退 (2025-09-17)
- 两篇《自然》:肺癌私联神经元!科学家首次发现小细胞肺癌细胞会在脑内与神经元形成突触,借助电信号促进肿瘤生长 (2025-09-16)
- Sci Adv:新型双特异性抗体有望成为抗击巨细胞病毒的“免疫特种兵” (2025-09-16)
- 《神经病学》:代糖或伤认知!8年随访发现,摄入较多代糖与记忆力、语言流畅性和整体认知能力下降速度提升32%、173%和62%相关 (2025-09-16)
- Nature子刊:超越ADC,中国博后发明ABC药物,重拳出击,精准靶向 (2025-09-16)
- Cell子刊:“滴血验癌”新突破,王延博/张硕等利用细胞外囊泡,精准检测10多种癌症 (2025-09-16)
- 47亿!派林生物易主中国生物,血液制品行业格局将重塑 (2025-09-15)
- 【9月16日直播预告】从样本到洞察:蛋白质组学智能实验室的自动化流程与AI高效赋能 (2025-09-15)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















