NCB:剑桥大学团队发现,一种治疗青光眼的药物可以让细胞“吐出”tau蛋白,改善小鼠认知! |
 |
来源:奇点糕 2024-11-27 14:01
研究发现一种治疗青光眼的药物——碳酸酐酶抑制剂——可以降低细胞tau蛋白水平。来自剑桥大学的研究团队利用转基因斑马鱼模型,对1400多种经过美国食品药品监督局()批准的药物化合物进行了筛选,发现一种治疗青光眼的药物 碳酸酐酶抑制剂 可以降低细胞tau蛋白水平。
碳酸酐酶抑制剂可以使溶酶体移动至细胞表面,促进细胞 吐出 tau蛋白,从而降低总tau水平和磷酸化tau水平。对于携带人类tau突变的小鼠模型,碳酸酐酶抑制剂治疗使小鼠大脑tau水平下降,记忆和认知能力得到提高。
研究发表在《自然 化学生物学》杂志上。

研究人员构建了具有明显tau毒性,并且适用于中等通量筛选的脊椎动物模型 转基因斑马鱼tau蛋白病变模型 在鱼视网膜中表达人类野生型tau。由于tau蛋白毒性,视网膜细胞会在几天之内迅速退化,表现为光感受器丢失和感光细胞退化,这种退化过程可以有效模拟tau病理变化。
研究人员共测试了1437种药物,以斑马鱼杆状光感受器变性改善评价tau毒性,筛选选中了methocarbamol。3 M浓度的methocarbamol可以显著挽救tau诱导的感光细胞退化、脊柱和体轴的形态缺陷,降低总tau和磷酸化tau水平。
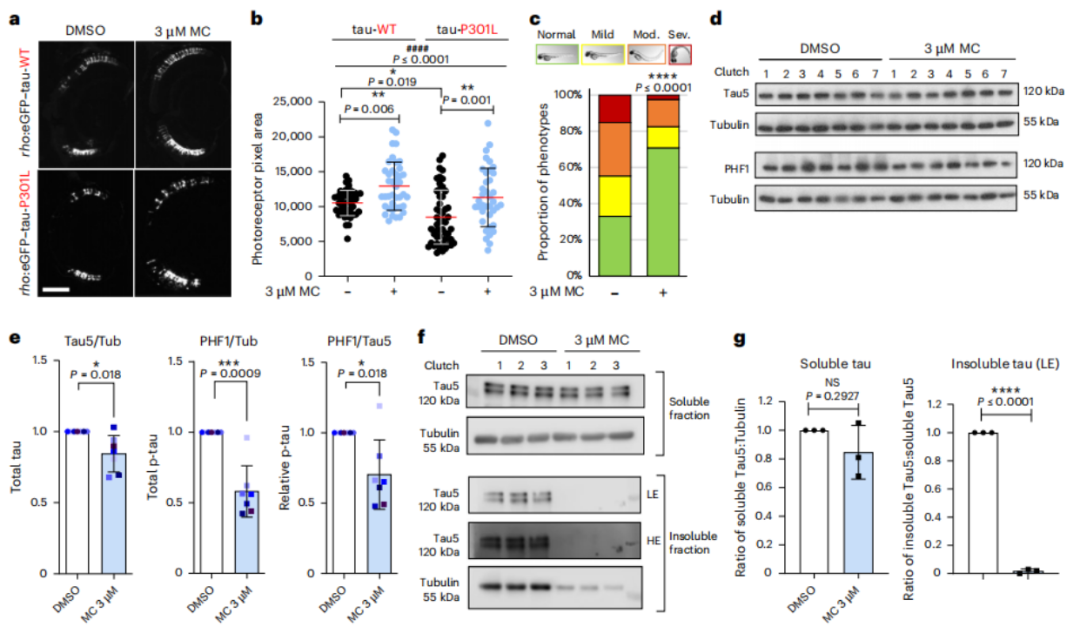
methocarbamol改善tau毒性相关病理、降低tau水平
methocarbamol是一种碳酸酐酶(CA)I抑制剂,根据药物数据库预测,会与其他CA同工酶相互作用。研究人员假设CA在methocarbamol改善tau毒性中起到关键的调节作用。通过进行RNA逆转录,研究人员找到了斑马鱼眼睛和神经元中表达CA的基因,并通过CRISPR Cas9使这些基因表达水平降低,10天后,可以观察到斑马鱼光感受器丢失和形态缺陷得到改善。也就是说,抑制CA可以预防斑马鱼模型中的tau毒性。
使用荧光信号标记神经元中的tau蛋白可以发现,抑制CA表达可以加速tau蛋白的清除速度。研究人员假设CA抑制剂是通过溶酶体清除tau的,但是在加入溶酶体抑制剂氯化铵之后,并没有阻止CA抑制剂对tau清除的加速作用。类似的实验显示,CA抑制剂对光感受器的保护作用也不依赖于自噬和蛋白酶体。
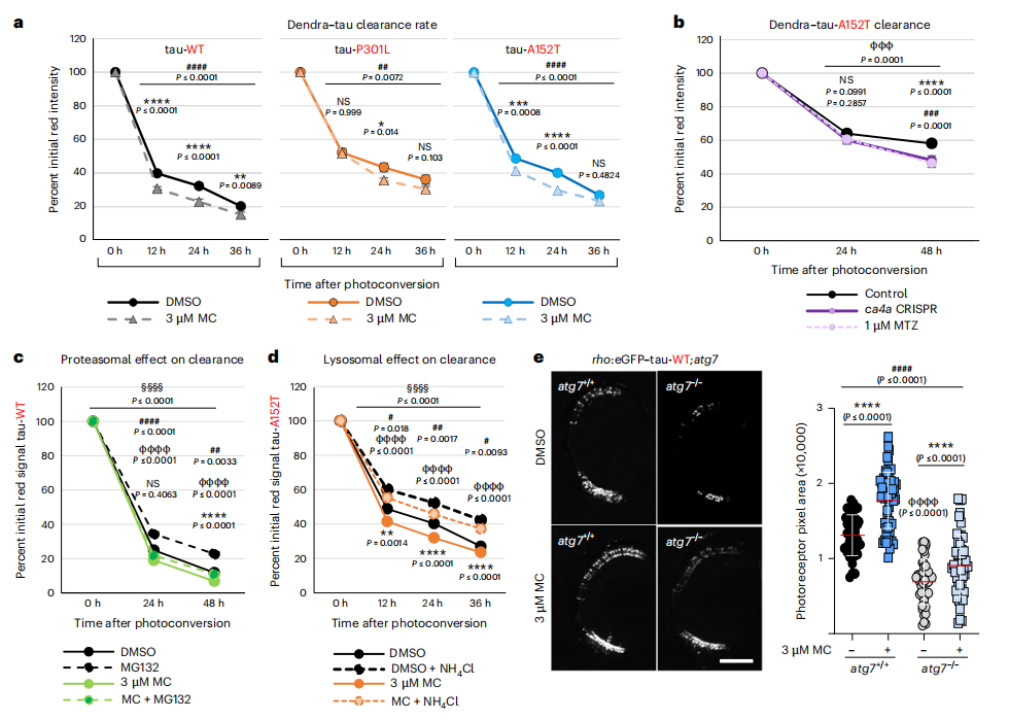
CA抑制增加tau清除率,但不会影响体内蛋白酶体或自噬降解
这就奇怪了,CA抑制剂究竟是如何促进tau清除的呢?
溶酶体除了可以降解细胞内的蛋白质,还可以将毒性蛋白通过胞吐作用排出到细胞外。通过之前的实验可知,虽然氯化铵抑制溶酶体酸化,影响溶酶体内部的降解环境,但是并没有影响tau清除,而CA抑制剂促使溶酶体的pH升高,增强了溶酶体的胞吐作用,使溶酶体移动至细胞边缘与细胞膜融合,释放tau至细胞外基质。这些被分泌出去的tau未被磷酸化,不具备引发蛋白聚集的 种子能力 ,因此可以减轻tau积累带来的细胞毒性。
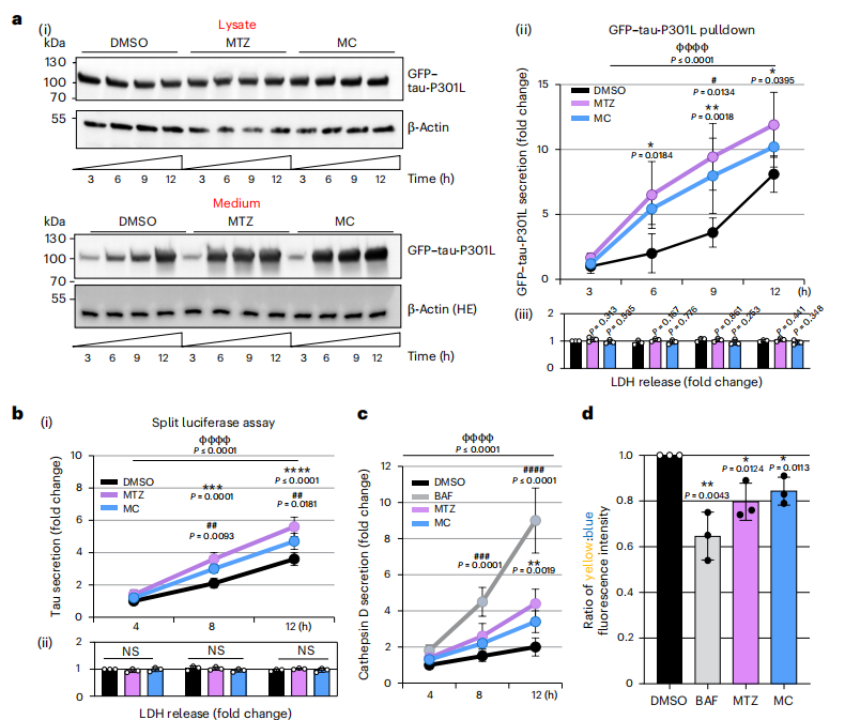
CA抑制剂通过溶酶体胞吐诱导tau分泌
接下来,研究人员在携带P301L tau突变的转基因小鼠中测试了CA抑制剂甲唑胺的效果。通过皮下植入渗透性微型泵,连续28天给药(10、20或50mg/kg/天),结果显示,低浓度甲唑胺也可以显著抑制小鼠大脑的CA活性,并且显著降低总tau-P3-1L水平;50mg/kg/天可以有效减少过度磷酸化tau水平,显著降低了毒性tau积累。
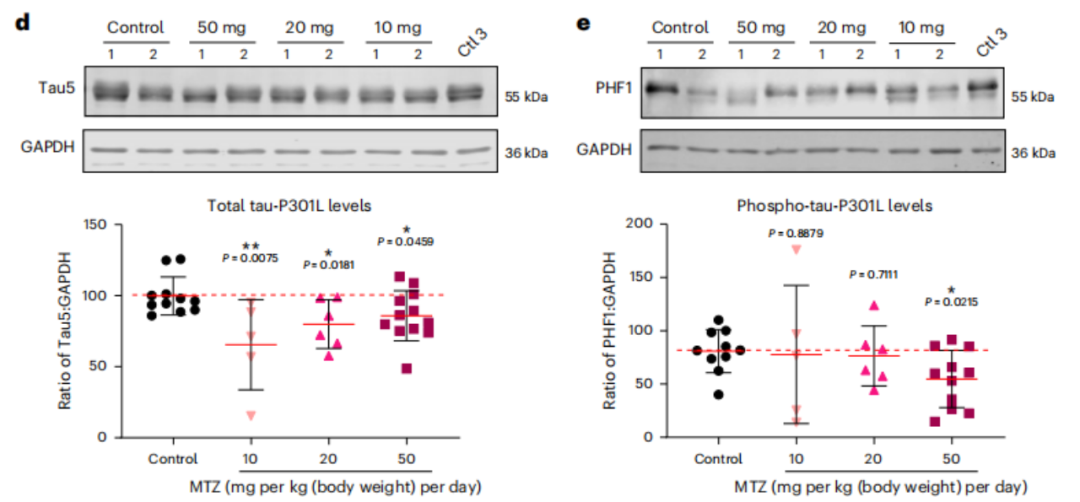
小鼠总tau和磷酸化tau水平降低
在携带P301S tau突变的PS19转基因小鼠中评估甲唑胺对认知的治疗效果。小鼠从6月龄开始逐渐形成tau聚集,在8-10月龄表现出较为严重的神经退行性症状。在小鼠8-9月龄和9-10月龄时分别植入皮下渗透性微型泵,进行每日20mg/kg甲唑胺给药,为期28天。结果显示,甲唑胺治疗显著减少了小鼠海马的神经元丢失,降低磷酸化tau积累,并且提高了小鼠对新事物的识别能力。
总的来说,研究证明CA抑制剂可以调节溶酶体酸化,促进通过胞吐作用的tau分泌,从而降低神经元内的tau水平,改善斑马鱼和小鼠模型中的神经元丢失和行为缺陷,展示了CA抑制剂用于治疗tau异常聚集为主要病理特征的神经退行性疾病的可能性,同时也说明,刺激毒性蛋白的非常规分泌可能是治疗相关疾病的有效方法。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:DNA甲基化“随机时钟”——EVOFLUX破译肿瘤演化史,重塑临床预后新维度 (2025-09-13)
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















