Cell:肠道微生物如何影响肺部健康?“肠 |
 |

肠道微生物:不为人知的远距离调控者
在我们人体的微观世界中,肠道微生物群长期被视为 局域者 ,主要负责调控消化吸收和局部免疫平衡。然而,越来越多的研究发现,肠道微生物的影响远不止于此,它们能够通过复杂的 肠-器官轴 (gut-organ axis)与身体的其他远处器官展开 对话 ,这种神秘的沟通机制正在重新定义微生物群与人体健康的关系。尤其是该研究揭示的 肠-肺轴 (gut-lung axis),为呼吸系统疾病的研究提供了全新的视角。
肠道微生物通过调节代谢产物、免疫细胞迁移以及神经调控信号等方式,影响着包括肺部在内的多个远距离器官。例如,某些微生物代谢物可以作为化学信使,通过血液或淋巴循环传递信号,直接影响肺部免疫微环境。此外,特定的肠道免疫细胞,比如 II 型先天淋巴细胞(ILC2),在肠道受刺激后能够迁移至肺部,并参与调控气道的免疫反应。
在该研究中,研究人员首次明确了一种肠道原生动物Tritrichomonas musculis (T.mu)如何通过这种肠-肺轴对肺部免疫环境进行 远程调控 。研究发现,T.mu 的存在激活了肠道内的 ILC2,并通过一种依赖于鞘氨醇-1-磷酸(S1P)信号通路的机制,促使这些细胞迁移到肺部。在肺部,这些由肠道而来的免疫细胞与 T 细胞、B 细胞形成三方协作网络,显著影响了肺部的嗜酸性粒细胞积累。正是这种远程调控,使得 T.mu 能够加剧哮喘的过敏性炎症,同时增强对结核分枝杆菌的抵抗力。
Tritrichomonas musculis:隐藏在肠道中的免疫调控大师
在肠道微生物群的庞大 生态系统 中,Tritrichomonas musculis (T.mu)可能并不为人熟知,但它的存在和作用却耐人寻味。作为一种肠道共生原生动物,T.mu 与宿主和其他微生物形成了一种微妙的 协作关系 ,这种关系不仅维持了宿主的免疫平衡,还为研究人员揭示了许多新的免疫学奥秘。
与许多共生微生物类似,T.mu 在正常情况下对宿主没有明显的致病性。研究发现,T.mu 通过与肠道菌群的协作,激活了一系列免疫调控机制。例如,它能够通过刺激肠道杯状细胞(tuft cell)释放白介素-25(IL-25),激活肠道 II 型先天淋巴细胞(iILC2)。这些细胞进一步释放重要的免疫调节因子,如白介素-5(IL-5)和白介素-13(IL-13),从而增强宿主对寄生虫和某些细菌的免疫防御能力。
值得注意的是,T.mu 的作用不仅限于肠道。在某些条件下,它能够通过复杂的鞘氨醇-1-磷酸(S1P)信号通路,诱导活化的 iILC2 迁移至肺部。这种跨器官的免疫细胞流动,显著改变了肺部的免疫微环境,使其更容易积累嗜酸性粒细胞(eosinophils)。这不仅加剧了哮喘等过敏性疾病,还在一定程度上增强了宿主抵御结核分枝杆菌感染的能力。
与细菌不同,T.mu 作为原生动物,其免疫调控作用更为独特。例如,它通过代谢物琥珀酸(succinate)与肠道菌群合作,共同激活免疫反应。这种协作关系使 T.mu 成为肠道微生态系统中的 关键玩家 ,其存在对于微生物群的平衡和宿主免疫功能的维持至关重要。
T.mu 的独特性不仅在于其与宿主和平共处的能力,更在于它能够调控远距离器官的免疫反应。这种 幕后主导者 的身份提醒我们,在肠道微生物的世界中,原生动物的作用可能被长期低估。随着研究人员对 T.mu 及其协作网络研究的深入,我们或许能够发现更多关于肠道微生态系统如何塑造人体健康的惊人秘密。
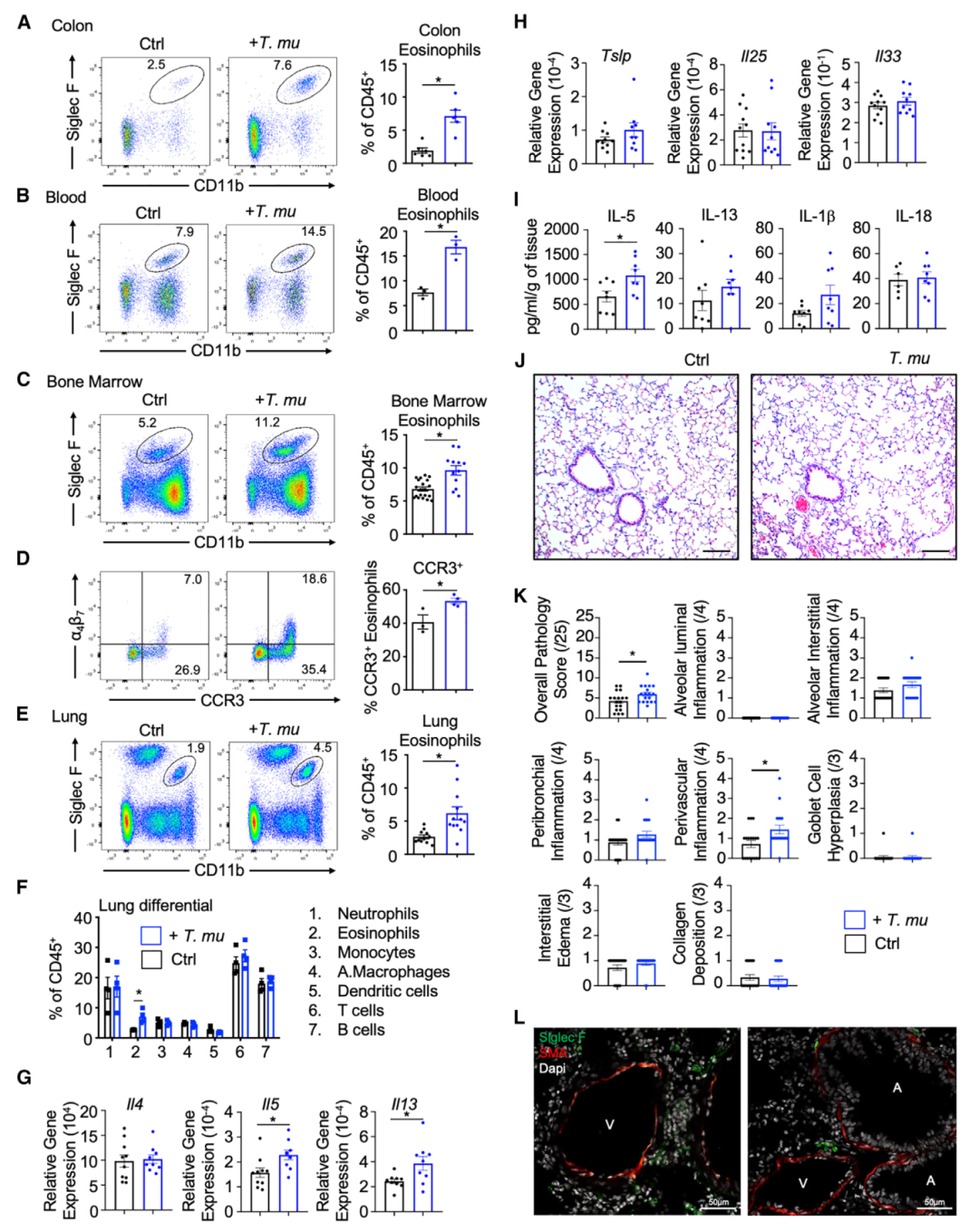
Tritrichomonas musculis 定植诱导全身性嗜酸性粒细胞增多(Credit:Cell)
实验设计研究人员对C57BL/6小鼠进行了实验,分为两组:一组未接受处理,另一组通过口服灌胃给予 2 10⁶ 个纯化的 T.mu。3周后对小鼠的多种组织进行了免疫学和组织学分析。
嗜酸性粒细胞的分布变化
(A C) 流式细胞术分析 显示,与对照组相比,T.mu 定植小鼠的结肠、血液和骨髓(BM)中 CD11b+ SiglecF+ 嗜酸性粒细胞的比例显著增加,表明全身性的嗜酸性粒细胞增多。
(D) 骨髓中表达 CCR3 和整合素 4 7 的嗜酸性粒细胞频率显著上升,这些受体与嗜酸性粒细胞的黏附和迁移密切相关。
肺部免疫环境的变化
(E) 肺部嗜酸性粒细胞的比例显著升高,而其他主要免疫细胞种类的频率无显著变化。
(F) 定植小鼠的肺部免疫细胞总量分析进一步证实了嗜酸性粒细胞的显著积累。
肺部相关基因表达
(G) 肺组织中 Il4、Il5 和 Il13 的mRNA表达显著增加,这些基因与 II 型免疫反应密切相关。
(H) 与此相对,Tslp、Il25 和 Il33 的表达水平无显著变化,说明嗜酸性粒细胞积累的机制可能主要依赖于 Il5 和 Il13。
肺部组织学变化
(I) 体外培养的肺组织培养液显示 IL-5 和 IL-13 的浓度显著升高。
(J) H E 染色的肺组织切片中可观察到周围显著的嗜酸性粒细胞积聚,但未见明显的炎症、杯状细胞增生或纤维化。
(K) 病理评分量化分析显示定植小鼠的肺部病理变化显著。
(L) 免疫荧光成像 显示肺部血管周围有大量的嗜酸性粒细胞积累,进一步证实其定植效应。
跨越肠道边界:II 型先天淋巴细胞的旅程
免疫系统中的 II 型先天淋巴细胞(ILC2)长期以来被认为是 驻地守卫 ,其主要任务是在肠道等局部组织中维持免疫平衡。然而,Tritrichomonas musculis (T.mu)的存在打破了这种传统认知,它通过一系列精妙的信号通路,驱动 ILC2 跨越肠道边界,远征至肺部,从而开启了免疫调控的新篇章。
研究发现,T.mu 的关键作用在于激活肠道内的炎性 ILC2(iILC2)。这种激活依赖于肠道杯状细胞(tuft cell)释放的白介素-25(IL-25),IL-25 刺激 iILC2 分泌大量的白介素-5(IL-5)和白介素-13(IL-13),不仅增强了肠道局部的免疫防御,还促使这些免疫细胞通过淋巴管进入血液循环。在这一过程中,T.mu 借助鞘氨醇-1-磷酸(S1P)和其受体 S1PR4 的信号通路,为 iILC2 的迁移提供了 导航系统 。研究数据显示,T.mu 的存在显著提高了血液和淋巴液中 S1P 的浓度,而这种信号分子是 iILC2 离开肠道的关键。
抵达肺部后,这些来自肠道的 iILC2 不仅保留了其炎性特性,还在肺部免疫网络中扮演了核心角色。它们通过释放 IL-5 和 IL-13,显著增加了肺部嗜酸性粒细胞的数量,这些细胞是哮喘等过敏性疾病的主要参与者。同时,iILC2 还与 T 细胞和 B 细胞形成了一个复杂的免疫协作网络,共同塑造肺部免疫环境。令人惊讶的是,这种跨器官迁移的免疫调控既可能加重过敏性炎症,又能增强对结核分枝杆菌的抵御能力。
T.mu 激活和引导 ILC2 的机制展现了肠道微生物对远距离器官调控的惊人潜力。这种 肠-肺轴 免疫调控方式不仅揭示了肠道微生态的复杂性,也为理解呼吸道疾病的免疫基础提供了全新视角。
三方协作:免疫网络如何塑造肺部环境
免疫系统的复杂性在于其精确的细胞协作,而在 T.mu 引导的免疫调控中,肺部免疫环境的塑造则是一个令人惊叹的三方协作过程。这一过程由 II 型先天淋巴细胞(ILC2)、T 细胞和 B 细胞共同完成,它们通过信号互作,创造了一个有利于嗜酸性粒细胞(eosinophils)积累的独特环境。
当 T.mu 激活的炎性 ILC2(iILC2)抵达肺部后,它们与局部的 T 细胞和 B 细胞紧密协作,形成了一个免疫调控的 工作组 。研究发现,ILC2 是这一网络的核心调控者,它们通过表达诱导性 T 细胞共刺激分子(ICOS)和 OX40 配体(OX40L),与 T 细胞和 B 细胞形成直接的物理和功能性联系。ICOS 与其配体 ICOSL 的相互作用尤为重要,实验数据显示,B 细胞是肺部 ICOSL 的主要来源,占比高达 90%。这一信号通路的活化直接调节了 ILC2 的存活与功能。
在这个免疫网络中,ILC2 通过分泌白介素-5(IL-5)和白介素-13(IL-13),驱动嗜酸性粒细胞的募集和扩增。而 T 细胞,特别是 CD4+ T 细胞,通过 OX40-OX40L 信号轴增加 IL-2 的产生,进一步支持了 ILC2 的活性和嗜酸性粒细胞的积累。此外,B 细胞不仅通过提供 ICOSL 支持 ILC2,还可能通过分泌免疫球蛋白参与免疫微环境的调控。
这一三方网络的协作,不仅导致嗜酸性粒细胞在肺部的积累,还塑造了一个炎性基调,使肺部对外界刺激更加敏感。这种调控网络在哮喘模型中尤为突出,表现为显著的嗜酸性炎症加重。然而,这种机制并非单纯的 有害效应 。在结核分枝杆菌感染的背景下,嗜酸性粒细胞的积累和去颗粒化过程有效限制了病菌的扩散,展现了这种免疫调控的 双刃剑 特性。
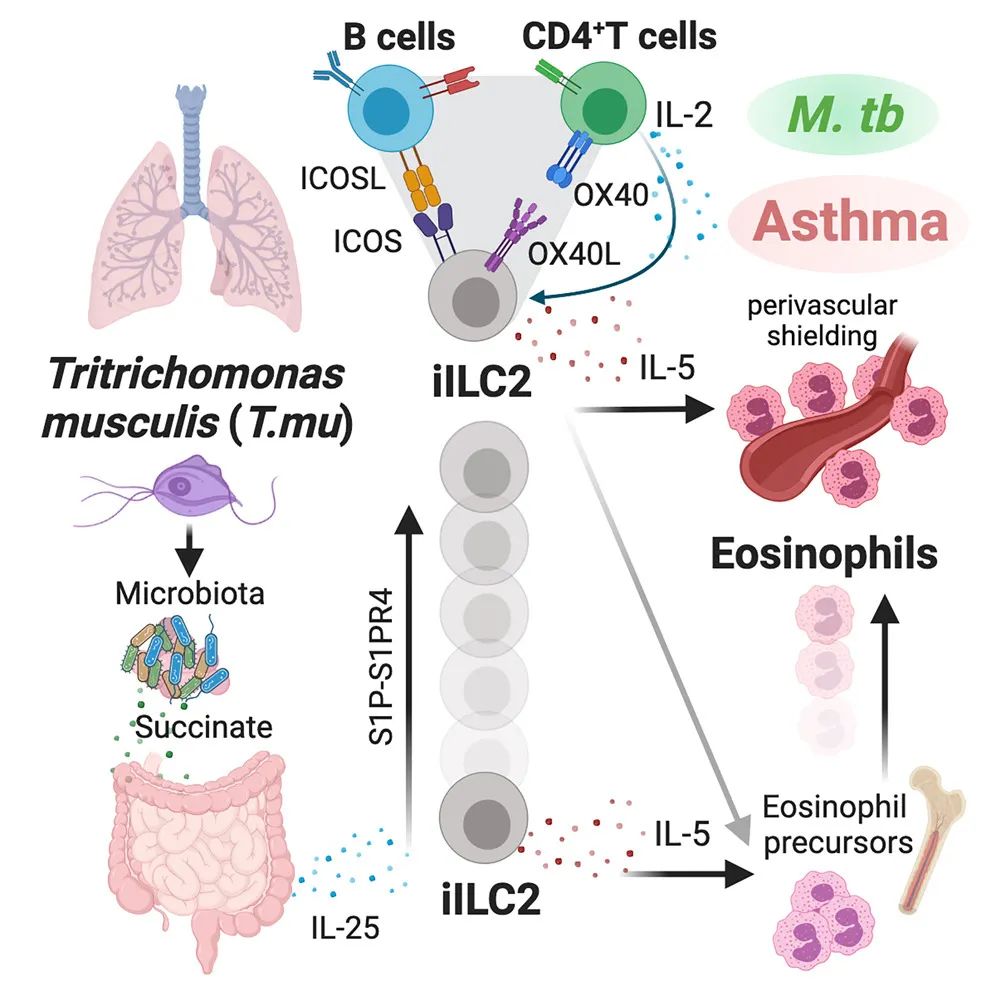
模式图(Credit:Cell)
从哮喘到结核:一体两面的疾病调控
T.mu 作为肠道微生态中的 隐秘调控者 ,它对呼吸系统疾病的影响展现出 一体两面 的特性:一方面,它通过免疫调控网络加剧了过敏性哮喘的炎症反应;另一方面,它又增强了宿主抵御结核分枝杆菌(M.tb)感染的能力。这种双重作用为我们理解免疫系统的复杂性提供了新的视角。
研究表明,在过敏性哮喘的模型中,T.mu 的存在显著加剧了气道的炎症反应。实验中,接受 T.mu 定植的小鼠在接触尘螨(HDM)等过敏原后,表现出更严重的气道病理变化,包括肺部嗜酸性粒细胞(eosinophils)数量激增、支气管周围的炎症显著加重,以及血清 IgE 水平的升高。这些变化与 T.mu 引发的肠-肺轴免疫调控密切相关,特别是其对 II 型先天淋巴细胞(ILC2)和嗜酸性粒细胞的调控网络,使得肺部对外界过敏原更加敏感,进一步加剧了哮喘的病理进程。
然而,同样的免疫调控机制在结核感染的背景下展现了积极的一面。研究发现,T.mu 引发的嗜酸性粒细胞积累显著提高了宿主在早期阶段对 M.tb 感染的抵御能力。嗜酸性粒细胞通过去颗粒化释放抗菌分子,有效限制了 M.tb 的扩散,并降低了感染向脾脏等外周器官传播的可能性。实验数据显示,T.mu 定植的小鼠在 M.tb 感染后肺部嗜酸性粒细胞的数量显著增加,与此同时,脾脏中的 M.tb 菌落形成单位(CFU)显著减少。这种保护效应在感染早期尤为明显。
T.mu 对哮喘和结核的双重影响展现了其免疫调控功能的复杂性。这种 一体两面 的特性不仅提醒我们原生动物对宿主健康的深远影响,也突出了免疫系统调控中的平衡与权衡。
肠道中的微生物,肺部的疾病答案?
哮喘是一种复杂的慢性气道疾病,其病理机制涉及多种免疫反应和遗传、环境因素的交互作用。然而,近年来的研究表明,肠道微生物群可能是这一疾病的重要,甚至能够为哮喘患者的分类和个性化治疗提供关键线索。在该研究中,研究人员揭示了肠道微生物通过 肠-肺轴 调控呼吸系统免疫的独特机制,这一发现为哮喘的精准诊断与治疗打开了新的大门。
研究发现,T.mu 通过激活肠道内的免疫细胞(如 II 型先天淋巴细胞 ILC2),驱动其迁移至肺部,并与局部免疫细胞形成复杂的协作网络。这种免疫网络在某些哮喘患者中可能发挥了重要作用。尤其是在严重哮喘患者的气道样本中,研究人员检测到了与 T.mu 相关的原生动物 DNA 痕迹,这提示某些哮喘患者可能具有特定的肠道微生物特征。尽管目前相关数据有限,这一发现已为哮喘患者的微生物分类提供了初步依据。
通过分析肠道微生物群的组成,未来有望识别出与哮喘亚型相关的特定微生物标志物。例如,原生动物是否存在,以及它们如何通过影响嗜酸性粒细胞和其他免疫细胞作用于气道炎症,可以作为潜在的生物标志,用于预测患者对治疗的反应。此外,研究还表明,针对 T.mu 的免疫调控通路,例如白介素-5(IL-5)和 OX40L 信号轴的抑制,可能为哮喘的个性化治疗提供新的药物靶点。
原生动物与肠道健康:被忽视的微生物群成员
当提到肠道微生物群时,我们往往首先联想到细菌,而原生动物往往被忽略。作为多样性极高的真核微生物,原生动物不仅是肠道微生物群的重要组成部分,更在宿主免疫调控和健康维持中扮演着独特的角色。在该研究中,研究人员首次揭示了原生动物如何通过复杂的机制与细菌和宿主免疫系统协同工作,从而深刻影响全身健康。
T.mu 是一种常见于鼠类肠道的共生原生动物,具有显著的免疫调控能力。研究表明,它能够通过与肠道细菌群的代谢协作,间接激活宿主的免疫反应。例如,T.mu 通过促进肠道代谢物琥珀酸(succinate)的积累,刺激杯状细胞(tuft cell)释放白介素-25(IL-25),进而激活 II 型先天淋巴细胞(ILC2)。这一过程不仅提高了宿主对寄生虫和细菌感染的防御能力,还影响了远距离器官如肺部的免疫环境。
与细菌不同,原生动物在宿主肠道内的作用更为微妙。它们通常不会引发急性疾病,但却能通过慢性和隐匿的方式重塑宿主免疫系统。例如,该研究显示 T.mu 可在不引发明显炎症的情况下,显著改变肠道嗜酸性粒细胞的分布,同时促进抗菌和抗寄生虫免疫。更重要的是,原生动物的存在还可能对细菌群落的多样性和稳定性产生积极影响,为维持肠道生态平衡做出贡献。
然而,原生动物对宿主的影响并非单一的 有益 或 有害 。T.mu 的研究揭示了这种 双刃剑 特性:在某些情况下,原生动物通过调控免疫网络保护宿主免受感染;但在另一些情况下,它们可能加剧过敏性疾病的严重程度。这种复杂的免疫调控作用提醒我们,肠道生态系统的健康不仅取决于细菌,还与原生动物密切相关。
肠-肺轴研究的新方向
肠道与肺部的 跨器官对话 揭示了人体免疫系统的复杂性,而 T.mu 的研究进一步将这一领域推向了新的高度。作为肠道-肺轴的重要研究案例,T.mu 不仅拓展了人们对肠道微生物群功能的认知,还为医学和免疫学研究开辟了多个新的方向。然而,如何将这些发现转化为临床应用,仍然面临一系列亟待解决的挑战。
首先,该研究展示了 T.mu 通过跨器官免疫调控影响疾病结局的潜力,为过敏性哮喘和结核病等疾病的精准治疗提供了新思路。例如,通过调节 T.mu 引发的免疫信号通路(如白介素-5和OX40L信号轴),或针对其驱动的嗜酸性粒细胞积累,可以开发出更加个性化的治疗策略。此外,原生动物相关的微生物组特征也可能成为生物标志物,帮助医生在哮喘患者中识别特定的亚型,从而实现更精准的诊断和干预。
然而,原生动物在微生物群中的角色仍是一个未完全解开的谜题。尽管 T.mu 的研究证明了其对肺部免疫调控的显著作用,但如何将这些发现推广到人类尚需进一步验证。比如,目前在人类哮喘患者的研究中,原生动物 DNA 的检测频率相对较低,这可能反映了样本收集的限制或个体间的巨大差异。此外,肠道微生物群的复杂性也为研究增加了困难,如何区分原生动物与其他微生物协作的具体贡献仍需深入探索。
另一个值得注意的方向是,如何平衡 T.mu 的双重作用。它既可以通过促进嗜酸性粒细胞积累加重过敏性疾病,又能增强宿主对感染性疾病的防御能力。未来研究需要寻找方法,在保留其免疫防御优势的同时,减轻对过敏性炎症的负面影响。
总的来说,肠-肺轴研究的前景令人振奋。通过更深入地理解原生动物、细菌和宿主免疫之间的复杂相互作用,我们不仅能够更好地理解疾病的机制,还可能开发出基于微生物群调控的全新治疗手段。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 国度疾控局:筹划用6年建成迷信高效的沾染病监测预警系统 (2025-09-24)
- 安康察看:向“体重治理”宣战,浙江若何出招? (2025-09-24)
- 国度药监局对于宣布15项医疗东西行业尺度 (2025-09-24)
- 对于印发儿童肺炎支原体肺炎诊疗指南(2025年版)的关照 (2025-09-24)
- Nature子刊:中山大学崔隽团队揭示代谢物草酰乙酸抵御流感新通路 (2025-09-24)
- 中国“黑马”竞逐GLP-1超长效之王 (2025-09-23)
- 【9月24日】线上研讨会:适应性采样技术——引领灵活靶向富集的未来 (2025-09-23)
- 诺奖得主David Baker推出RFdiffusion3,颠覆蛋白质设计格局,开启全原子生物分子设计新时代 (2025-09-23)
- 《癌症研究》:内鬼实在太多了!科学家发现,小胶质细胞的TBK1信号激活会吸引乳腺癌入脑 (2025-09-23)
- 阿尔茨海默病领域顶刊中文版第一期正式发布,26位中国认知领域主流专家共同推进AD诊疗发展 (2025-09-22)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















