Trends in Biotechnology:体外“创造”人类大脑已不再遥不可及!一文读懂脑类器官的“进化史” |
 |
1.1 脑功能区
过去十年中,脑类器官的研究取得了显著进展,但早期的脑类器官存在两个主要限制:一是缺乏明确的脑区划分,二是无法模拟特定脑区的发育。
为克服这些限制,研究人员开发了多脑区特异性脑类器官,通过模拟体内神经发育的模式线索和形态发生信号,成功概括了特定大脑区域的特征。
例如,通过双重SMAD抑制和WNT、TGF- 等信号通路的调节,可以诱导类器官向皮质、纹状体、内侧神经节隆起、丘脑、海马、下丘脑和中脑等不同脑区发育。
此外,通过微流体装置实现多个正交形态因子梯度的精确控制,进一步提升了类器官的区域特异性和成熟度。这些进展使得大量区域特异性脑类器官的生成成为可能,为脑疾病研究提供了更精准的模型(图1)。
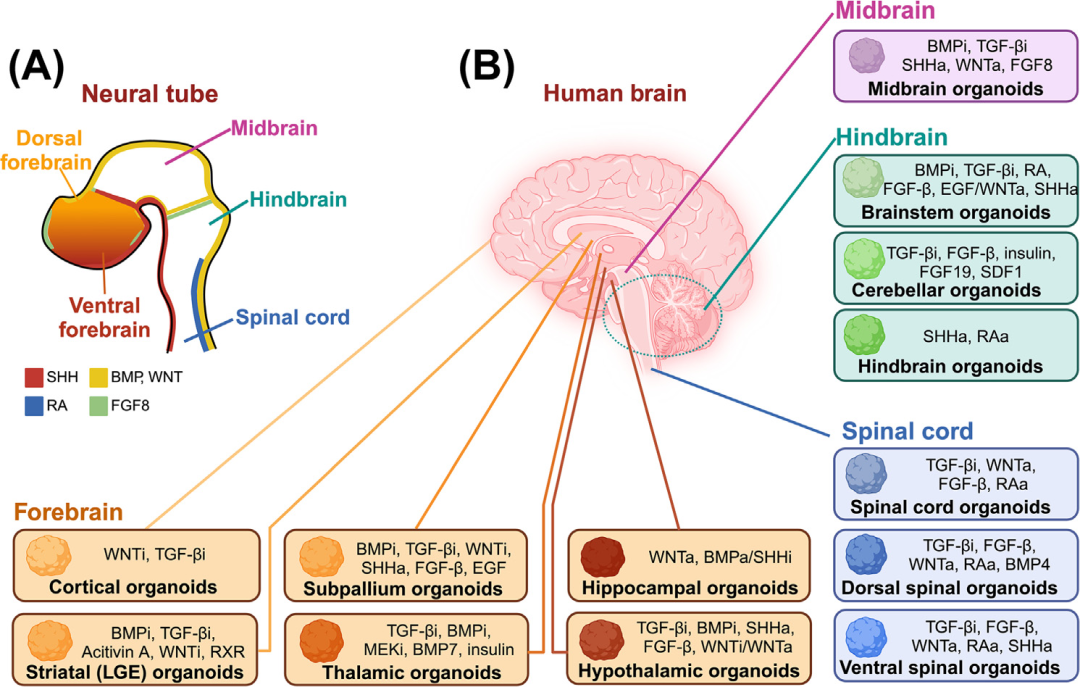
图1
1.2 神经回路
早期脑类器官模型存在两个主要限制:一是无法概括特定脑区的发育;二是无法模拟脑区间的相互作用,包括信号转导、细胞间通信、细胞迁移和神经回路的形成。
为解决这些问题,研究人员开发了脑区特异性类器官,并通过融合这些类器官创建了 多脑区组装体 。这些组装体能够模拟脑区间的功能连接,例如通过融合皮质和纹状体类器官来研究运动障碍相关神经回路,或通过融合视网膜和丘脑类器官来重建视觉回路。
此外,还开发了更复杂的三向或四向组装体,如皮质-脊髓-肌肉组装体,用于研究运动功能。这些组装体在模拟神经回路和大脑区域相互作用方面具有巨大潜力,可用于研究从运动和感觉处理到认知和执行功能的复杂行为。
然而,这些模型仍面临挑战,如缺乏标准化的融合方法和无法完全再现白质结构。尽管如此,最近的技术进展正在帮助克服这些挑战,推动脑类器官模型在神经科学研究中的应用(图2)。
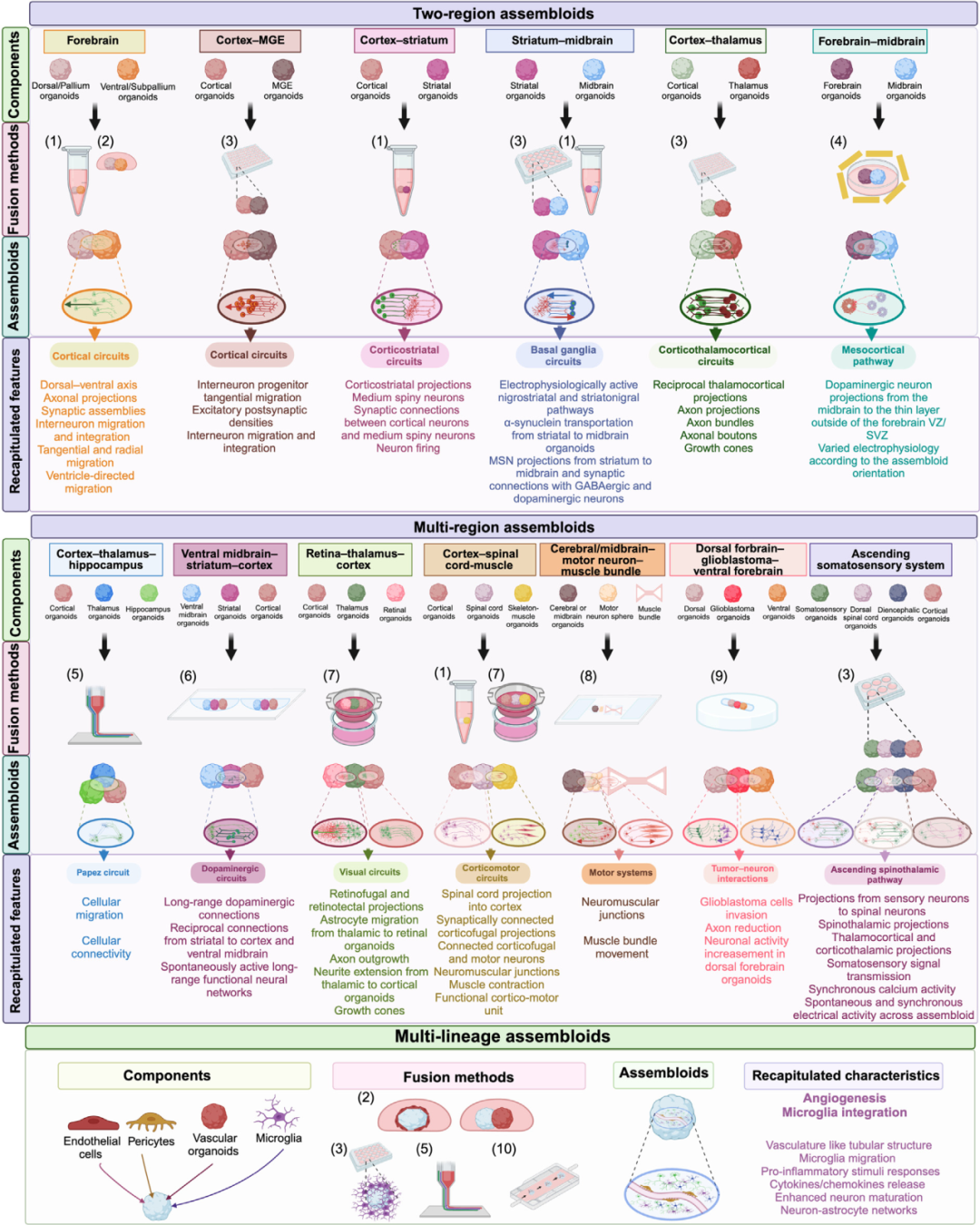
图2
2. 类器官的突触功能和电活动
改进的类器官模型在神经科学研究中展现出巨大潜力,具备成熟突触和电活性神经元网络等特征。例如,中脑类器官中观察到突触发生,且电镜显示突触结构。
神经元电活动通过钙成像和电生理学得到证实,钙成像显示类器官神经元具有钙活性,且与体内小脑回路模式相似。全细胞膜片夹持和多电极阵列(MEA)被用于记录类器官的电生理特性,但传统MEA存在空间记录限制。为此,研究者开发了三维MEA和3D多功能中尺度框架,能够更好地记录类器官的神经网络活动,同时减少对类器官的损伤。
此外,3D双MEA设备和弹性组织样纳米电子学也被设计用于长期记录类器官的电生理活动。然而,这些技术可能干扰类器官的细胞结构和发育。因此,一种新的3D折叠电记录平台kirigami被开发出来,其超薄电极可以几何地容纳悬浮中的类器官,实现长期整合和连续记录神经元活动(图3)。
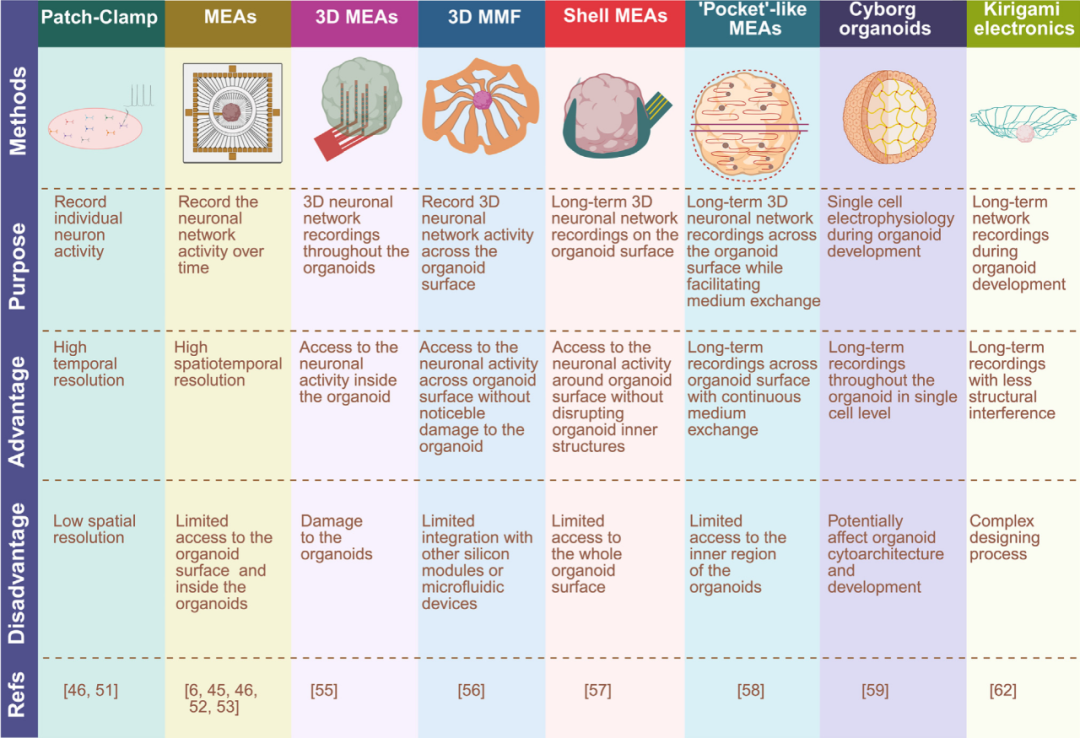
图3
3. 增强脑类器官建模的能力
3.1 脑类器官细胞死亡
类器官培养面临细胞死亡等挑战,可能是由于氧气和营养物质无法充分渗透到核心。为解决此问题,研究者引入摇动方法或在气液界面培养类器官切片,以增强营养物质进入类器官内部。此外,微流控平台结合可灌注培养室和气液界面,可培养全脑类器官,减少缺氧核心形成。
类器官的血管化通过与内皮细胞共培养或共包埋,可增加营养物质进入核心并重现血脑屏障。类器官芯片方法通过微流体通道和腔室设计,实现血管细胞与类器官的同步和定向,增强神经元分化,减少细胞死亡,为精准医学测试提供了新的平台(图4)。
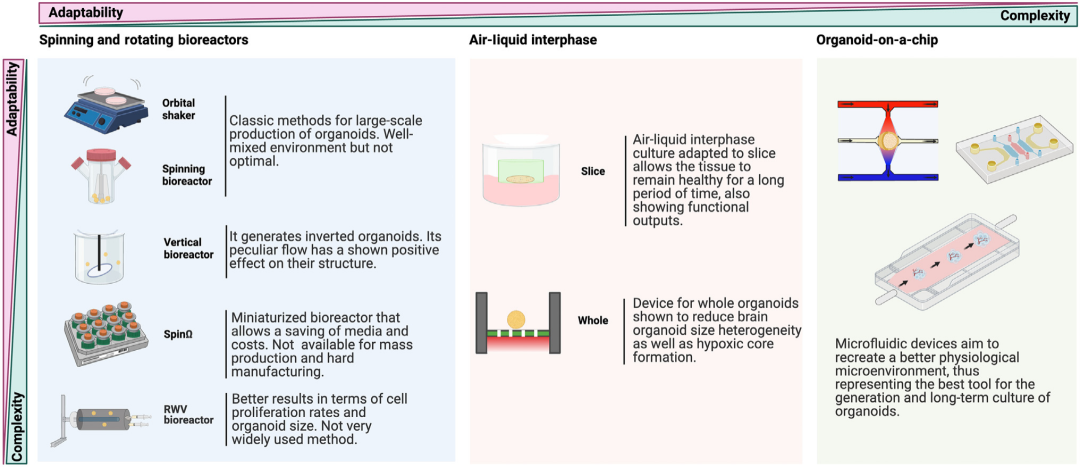
图4
3.2 漫长的胶质形成过程
类器官中已证实星形胶质细胞和少突胶质细胞祖细胞的自发诱导,但它们出现较晚。加入少突胶质细胞系生长因子和激素可促进少突胶质细胞成熟和髓鞘形成,但需3个月分化时间。
为缩短时间,使用表达少突胶质细胞发育必需转录因子的人OLIG2或SOX10多能干细胞报告系,将髓鞘层形成时间缩短至42天。
3.3 类器官缺乏小胶质细胞
早期类器官模型因缺乏小胶质细胞等免疫细胞类型,限制了对脑部疾病免疫反应的研究。近期,通过将来自诱导多能干细胞(iPSC)的小胶质样细胞(MLC)或小胶质细胞前体与类器官共培养,成功整合小胶质细胞。这些细胞表现出迁移能力、细胞内Ca ⁺信号传导和对促炎刺激的反应。
此外,将MLC或巨噬细胞前体细胞与类器官结合,可影响类器官的细胞因子和趋化因子释放,调节相关基因表达。过表达髓细胞特异性转录因子PU.1可使MLC在类器官中表现出完整的补体和趋化因子系统。这些方法增强了类器官模拟涉及重要免疫成分的脑疾病的能力。
3.4 脑类器官生成方案的低效率和可重复性
脑类器官的生成程序冗长且存在显著差异。为克服传统方法局限,3D生物打印被采用。该技术需专用生物墨水支持细胞存活和分化。纤维蛋白基和海藻酸盐/Matrigel生物墨水已被用于支持神经组织生长和生成成熟神经组织。通过过表达转录因子,可在数天内获得血管化类器官。
生物打印的3D神经组织可形成类似功能性神经回路的结构。先进的微加工类胚体圆盘装置可扩大类器官生成并降低变异性。这些进步加速了营养物质灌注,提高了类器官生成的速度和可重复性。
3.5 适合模拟年龄依赖性和神经退行性疾病
类器官模型的改进,如长期培养和整合小胶质细胞,增强了其在模拟衰老相关脑部疾病中的适用性。然而,类器官通常处于早期发育阶段,缺乏衰老相关神经退行性疾病的特征。
为模拟衰老,中脑类器官在不含抗氧化剂的BDNF和GDNF中培养,表现出衰老相关基因和DNA损伤标记上调。诱导衰老的药物羟基脲和A 42诱导剂Aftin-5也被用于类器官,但药物的非特异性影响仍需解决。
散发性阿尔茨海默病可通过加入人血清模拟,而帕金森病的 -syn聚集和神经毒素MPTP诱导的神经元死亡可用于模拟帕金森病病理。这些改进使类器官更适合模拟衰老相关的神经退行性疾病。
4. 脑类器官作为疾病模型
4.1 阿尔茨海默病和额颞叶痴呆
携带阿尔茨海默病(AD)相关基因突变的脑类器官表现出A 沉积、磷酸化tau蛋白水平升高及神经网络活动异常。APOE4变异的类器官A 聚集和tau磷酸化增加,神经元突触数量增多,星形胶质细胞A 摄取受损,胆固醇积累增加。A 水平升高与突触蛋白减少、细胞凋亡相关。
模拟额颞叶痴呆(FTD)的类器官中,自噬-溶酶体途径受损导致神经元丢失。多谱系组装体促进AD神经炎症研究,MLC与类器官共培养可减轻A 诱导的损伤,而APOE4纯合子MLC与APP复制类器官共培养则表现出更高的A 沉积和磷酸化tau水平(图2)。
4.2 帕金森病
中脑类器官是研究帕金森病(PD)相关多巴胺能神经元病理的常用模型,包含多巴胺能神经元。携带LRRK2 G2019S突变的中脑类器官表现出多巴胺能神经元数量和复杂性减少。
携带三倍体SNCA基因的中脑类器官形成路易体样包涵体和泛素 -syn嗜酸性核。与纹状体类器官组合时,过表达SNCA的中脑类器官轴突投射减少且随机,电生理和网络活性降低, -syn在中脑类器官中积累。这些组合体为研究病理性 -syn的细胞间传递假说提供了模型。
4.3 COVID -19相关的神经系统疾病
COVID-19大流行引发了神经系统疾病,研究发现SARS-CoV-2可在大脑中复制并导致长期大脑结构性变化或认知缺陷。类器官被广泛用于研究SARS-CoV-2的中枢神经系统致向性,不同脑区域类器官对感染的敏感性不同,可能与ACE2表达水平有关。
感染后的类器官表现出神经退行性疾病的病理特征,如tau蛋白错位、A 积累和突触丢失,且APOE4神经元感染更严重。研究表明COVID-19可能增加神经或神经退行性疾病风险,但仍需更多研究支持。
医药网新闻
- 相关报道
-
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 肠道菌群还能操控皮肤炎症?清华大学最新Immunity论文,揭示肠道菌群代谢物驱动银屑病炎症的机制 (2025-09-11)
- 构建中国人衰老时钟,200多位中国学者联合推出X-Age项目(耄耋计划),推动健康长寿研究 (2025-09-11)
- 参天公司青光眼引流器"港澳药械通"上市许可获广东省药监局批准 (2025-09-10)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















