突破!Adv Healthc Mater:人诱导多能干细胞构建含免疫细胞的血管化皮肤类器官,皮肤研究迈上新台阶 |
 |
突破!Adv Healthc Mater:人诱导多能干细胞构建含免疫细胞的血管化皮肤类器官,皮肤研究迈上新台阶
来源:100医药网 2025-08-25 09:26
本研究成功构建出含血管网络和驻留免疫细胞的血管化皮肤类器官,其能模拟人体皮肤结构与功能,为皮肤生物学及免疫介导疾病研究提供革命性平台。
皮肤作为人体最大的器官,承担着屏障保护、体温调节、防御等多种重要功能。其复杂的结构包括表皮、真皮和皮下脂肪层,而网络和免疫细胞在维持皮肤稳态中发挥着关键作用。然而,长期以来,构建具有完整血管系统和免疫细胞的功能性皮肤模型一直是科研领域的一大挑战。
近日,发表在Adv Healthc Mater上的一项研究Coordinated Development of Immune Cell Populations in Vascularized Skin Organoids from Human Induced Pluripotent Stem Cells成功开发出一种源自人类诱导多能的血管化皮肤类器官(VSKO),该模型实现了免疫细胞群与血管化皮肤的协同发育,为皮肤生物学研究和相关疾病治疗带来了新希望。

研究团队首先尝试将人类胎儿胎盘内皮集落形成细胞(ECFC)整合到人类诱导多能干细胞(hiPSC)衍生的皮肤类器官(SKO)中,形成内皮化皮肤类器官。结果显示,ECFC能够形成毛细血管样结构,但这种方法存在明显局限,不仅无法建立完整的血管网络,还会阻碍表皮的完全分层和毛囊的形态发生。免疫荧光显微镜和流式细胞分析进一步证实,尽管ECFC实现了内皮化,但生长因子减少的基底膜基质(GFR-M)的使用对SKO的成熟产生了抑制作用,导致角质形成细胞分层受阻,且未观察到毛囊发育。
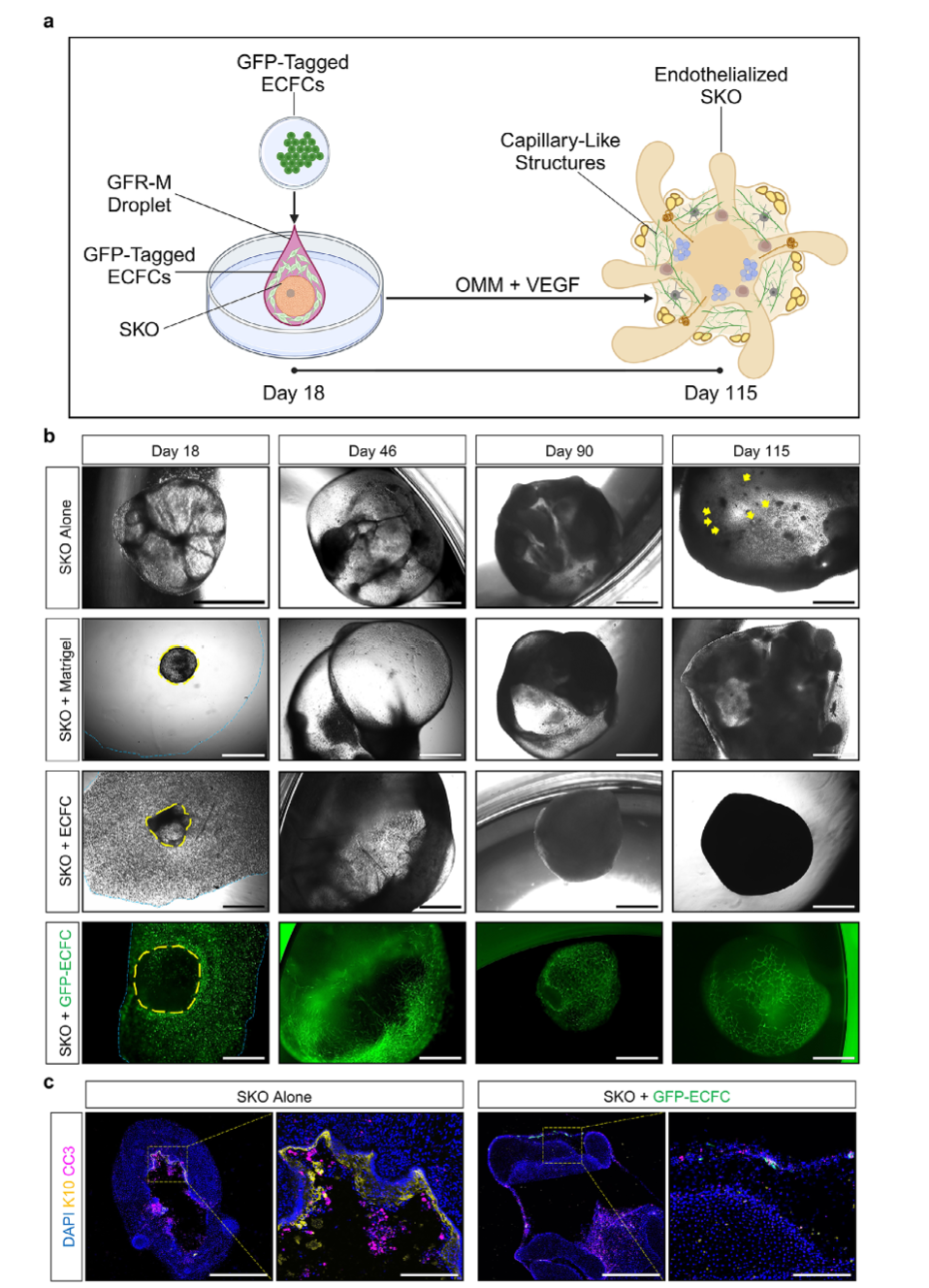
图 1:内皮化皮肤类器官的发育
为克服上述局限,研究团队转而采用hiPSC衍生的血管类器官(VO)与SKO共培养的方法。他们首先成功诱导hiPSC分化为血管类器官,该过程通过添加特定因子促进中胚层谱系分化,并在早期加入转化生长因子- 抑制剂和GFR-M液滴,以促进内皮毛细血管的快速发育。流式细胞分析显示,VO包含多种细胞类型,如内皮细胞(CD31+)、造血细胞(CD45+)、间充质细胞(CD90+)和周细胞(PDGFR +)等。免疫荧光分析证实,VO中存在动脉毛细血管(DLL4+)、静脉毛细血管(EMCN+)以及 -平滑肌肌动蛋白阳性的壁细胞,表明其能够模拟人体血管的多种表型。
在构建血管化皮肤类器官时,研究团队将一个SKO置于两个VO之间,利用气液界面培养系统进行共培养。这种培养方式模拟了人体皮肤暴露于外界环境的状态,有助于促进SKO的分化。结果显示,VO中的血管结构能够向SKO迁移,形成复杂的血管网络,并且VO中的内皮细胞、壁细胞、造血细胞和间充质细胞成功整合到VSKO的皮肤成分中。VSKO表现出发育良好的厚表皮层,且未出现核心,证实了该模型的稳定性和功能性。
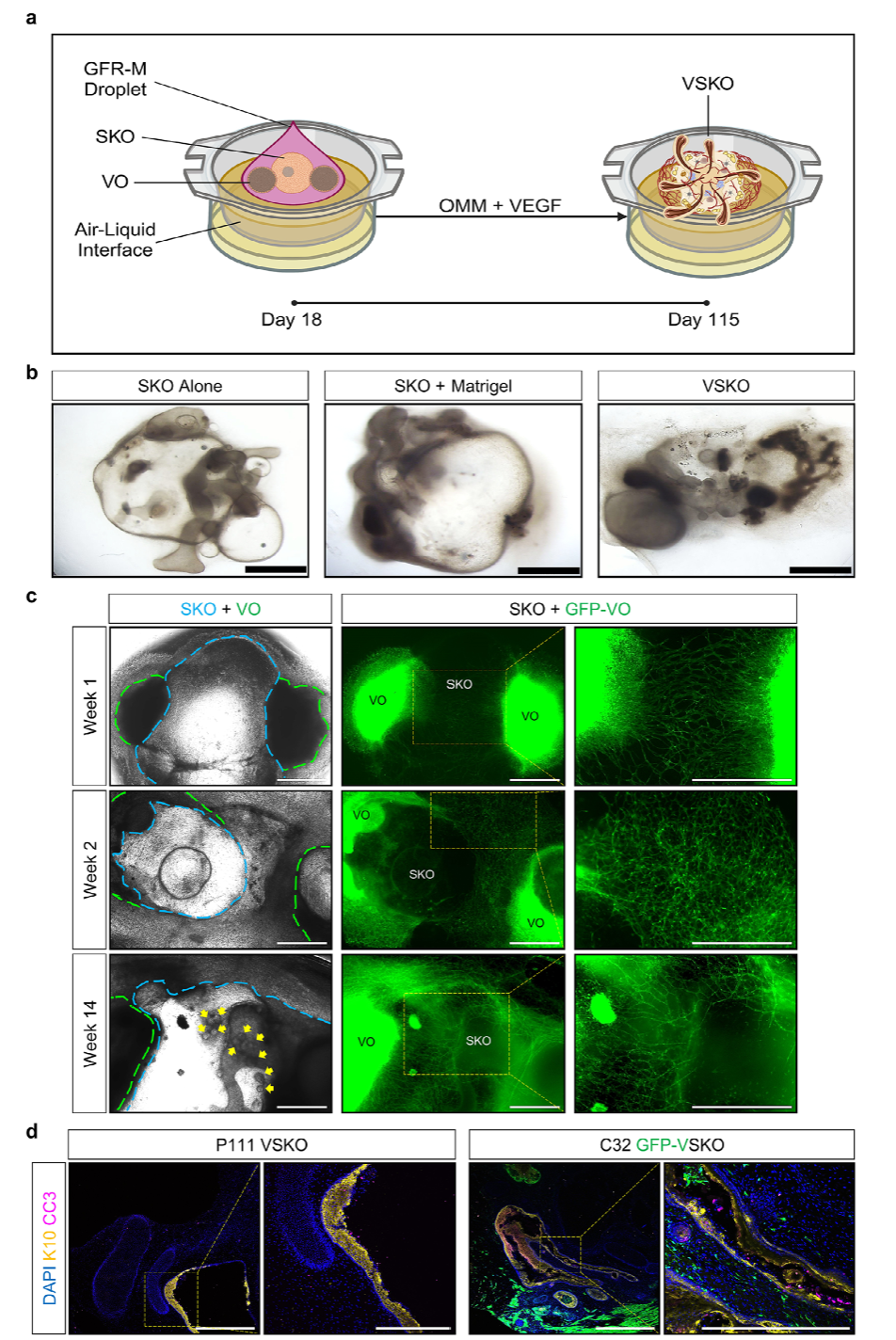
图 2:血管化人类皮肤类器官的发育
与内皮化SKO模型不同,VSKO中观察到了毛囊的形成和角质化过程。组织学染色显示,VSKO具有厚上皮层、毛囊和真皮乳头,与之前报道的SKO特征一致。免疫荧光分析证实,内皮毛细血管深入到毛囊的毛囊周围区域,且血管样结构由VO来源的细胞形成,表明VO在VSKO的血管化过程中发挥了关键作用。此外,VSKO中的毛囊表达SOX2、K14、K15和K17等标志物,与现有SKO模型一致,证实了其皮肤结构的完整性。
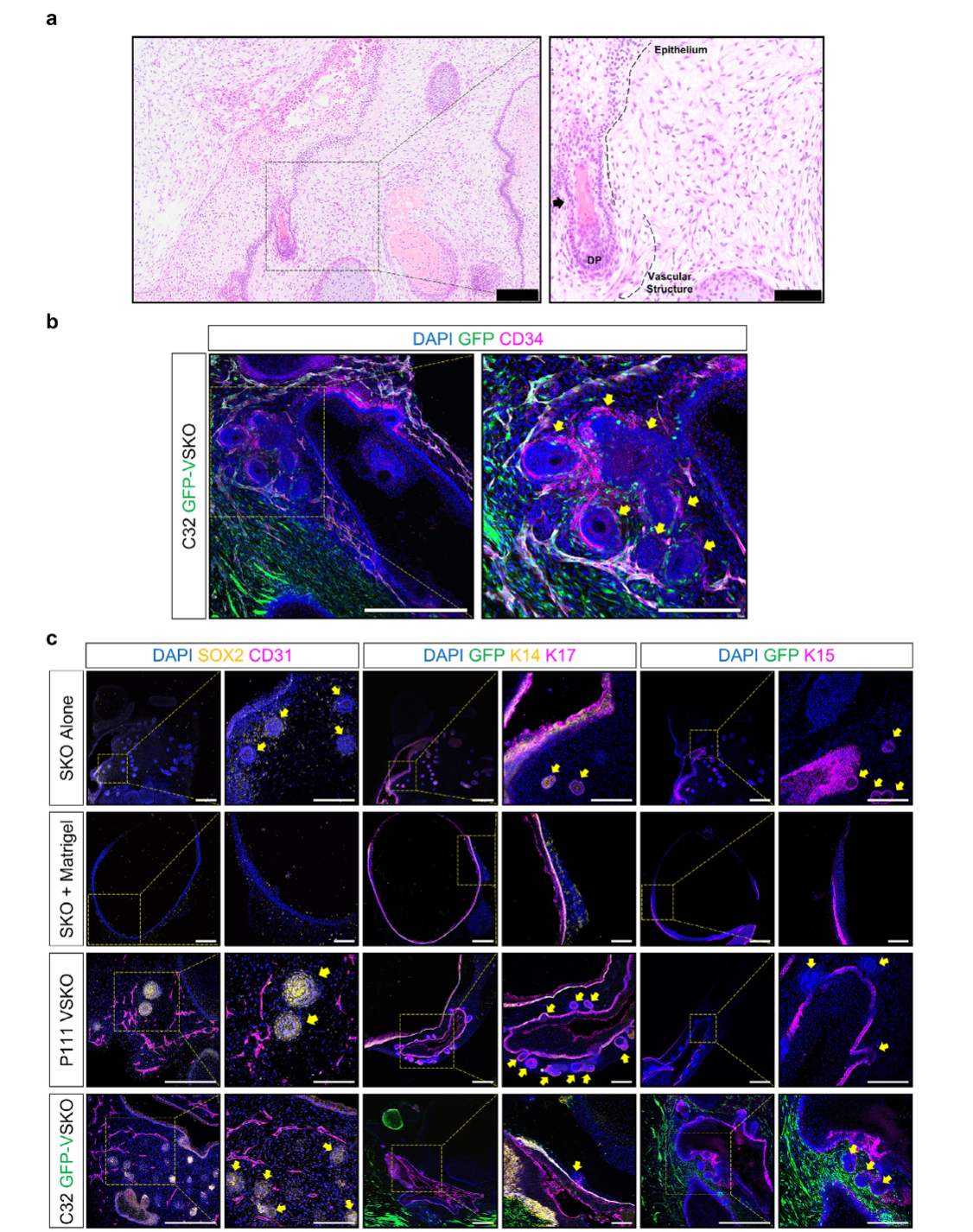
图 3:血管化人类皮肤类器官的毛囊特征
值得注意的是,VSKO中还存在驻留免疫细胞群。研究发现,VO在分化过程中会形成造血细胞谱系,到第21天时,CD45+细胞数量显著增加并分散在整个类器官中。在VSKO中,CD45+造血细胞从VO迁移到皮肤成分中,主要分布在真皮层,少数存在于表皮层。进一步分析显示,这些免疫细胞包括巨噬细胞(CD68+)、朗格汉斯细胞或真皮树突状细胞(CD207+)以及中性粒细胞(CD66b+),表明VSKO成功模拟了皮肤的免疫微环境。
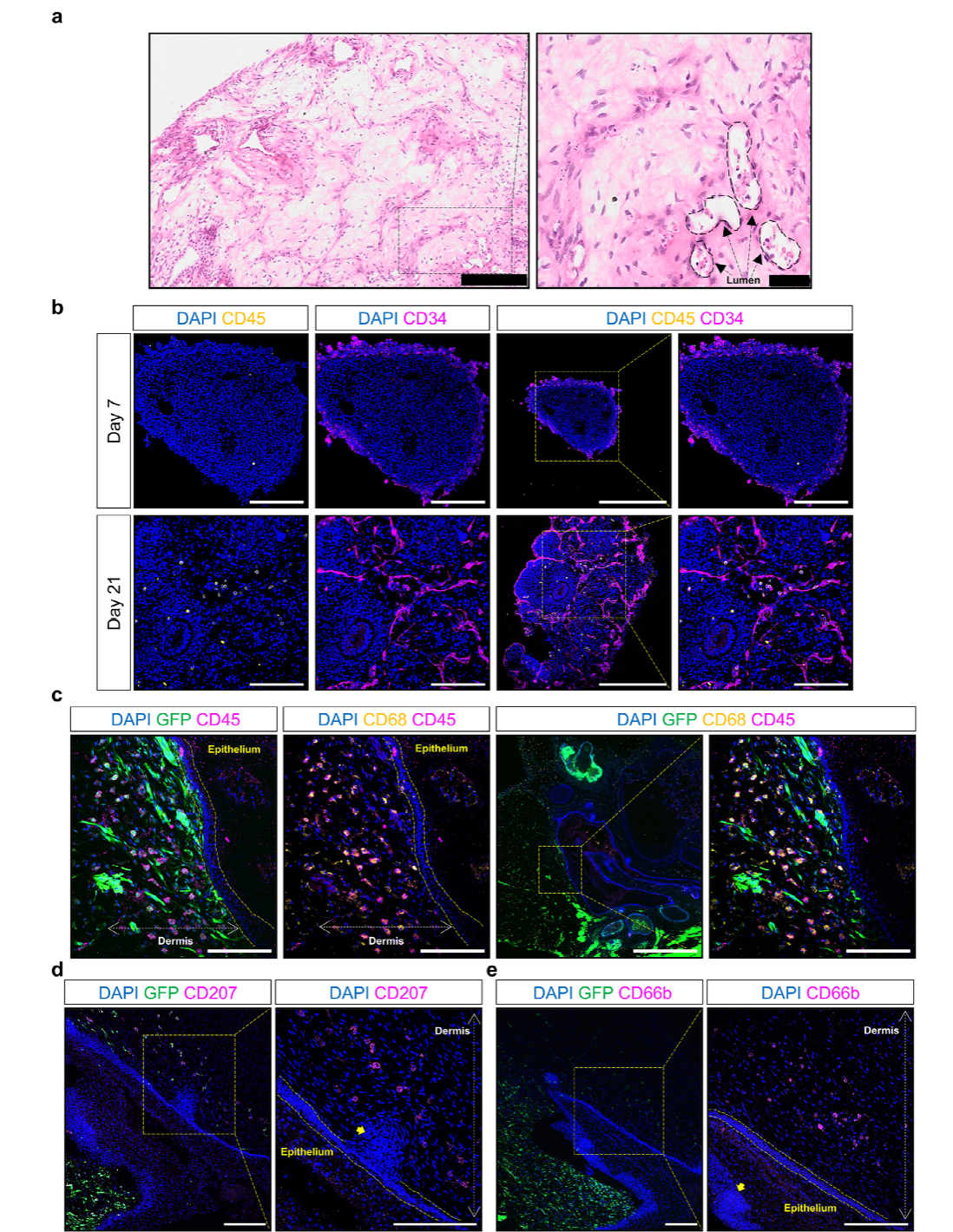
图 4:血管类器官来源的免疫细胞迁移至皮肤类器官中
综上所述,这项研究成功构建了一种具有完整血管网络和驻留免疫细胞的血管化皮肤类器官,该模型在结构和功能上更接近人体皮肤,为研究人类皮肤生物学、免疫-皮肤相互作用提供了一个革命性的平台。其在炎症性和其他免疫介导的皮肤疾病研究中具有广泛的应用前景,同时也为再生医学、药物筛选和疾病建模等领域开辟了新的研究途径,有望推动相关领域的快速发展。(100yiyao.com)
参考文献:
Mostina M, Sun J, Sim SL, et al. Coordinated Development of Immune Cell Populations in Vascularized Skin Organoids from Human Induced Pluripotent Stem Cells.Adv Healthc Mater. Published online August 16, 2025. doi:10.1002/adhm.202502108
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature子刊:浙江大学方向前/赵玥绮/唐睿康/刘昭明团队开发抗衰老的时空自适应纳米疗法 (2025-10-07)
- Neuron:大脑“超清摄像头”问世!神经观测有望进入新时代 (2025-10-07)
- 科研人员绘制图谱解析风险SNP驱动的促肿瘤机制 (2025-10-06)
- Nature子刊:邓攀团队提出AI框架——CellNavi,为细胞研究装上“导航仪” (2025-10-06)
- Nature头条:如何才能科学地睡个好觉?做到这三点至关重要 (2025-10-05)
- 中国科学院最新论文,登上Science封面 (2025-10-05)
- 《细胞》子刊:微生物守护卵巢健康!科学家发现,雌性小鼠生育年龄与微生物有关,微生物代谢物可防止卵巢储备加速流失 (2025-10-04)
- 珍·古道尔的遗产:她改变科学的三种方式 (2025-10-04)
- Nature Aging:沈舒滢/季明亮/赵兴团队发现骨关节炎治疗新靶点,并提出基于LNP-mRNA的新疗法 (2025-10-03)
- Nature Medicine:颠覆认知!体重不减反增,为何依然能逆转糖尿病前期? (2025-10-03)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















