PNAS:浙江大学曲萌等发现,抑制生物钟蛋白,可阻止肝癌发展 |
 |
来源:生物世界 2023-01-15 11:23
该研究为生物节律调控肝癌发生发展提供了分子机制,也为靶标生物钟小分子的开发及在肝癌治疗中的应用提供了理论基础。肝细胞癌(Hepatocellular Carcinoma)是最常见的原发性肝癌,平均五年生存率仅为约18%。随着脂肪性肝病的迅速增加,全球肝癌发病率正逐年上升,已引起各国的普遍关注。作为当前中晚期肝癌的一线治疗方案,阿替利珠单抗(PD-L1单抗)联合贝伐单抗(抗肿瘤生成)疗法相较此前的标准药物索拉菲尼,在生存率和响应率方面均有显著改善,但总体治疗效果仍存在较大提升空间。
生物节律是生命进化史上最保守的生理机制之一,它调控生物体的生理和行为,使之与昼夜交替相适应。灵长类动物的全身有超过80%的蛋白质编码基因呈现出昼夜节律性表达的特征。正因如此,参与调控包括睡眠、进食、激素分泌、代谢、反应等在内几乎所有的生理过程;昼夜节律的紊乱与众多临床相关疾病如睡眠障碍、肥胖、、癌症等的发生密切相关。
肝脏是生物节律发挥代谢调控作用的核心执行器官,表现为:1)肝脏中呈现昼夜节律性表达基因的比例最高;2)器官特异性敲除肝脏中的生物钟基因,除了会导致肝内代谢的失调,亦可促进肥胖、糖尿病等全身性代谢疾病。尤其,有多项研究结果提示,肝癌的发生发展与生物节律紊乱息息相关,包括:1)肝癌组织中的生物节律常常是紊乱的;2)长期的生物节律紊乱可促使脂肪在肝脏内堆积,并可能诱导自发性肝细胞癌的发生;3)临床数据发现,生物钟基因的突变及表达变化跟肝癌病人的生存时间有显著关联。然而,因上述结论多为描述性,生物节律调控肝癌发生发展的分子机制尚不明确。
近日,浙江大学国际健康医学研究院、 一带一路 国际医学院、医学院附属第四医院曲萌课题组和美国南加州大学Steve A. Kay课题组合作,在PNAS杂志发表了题为:Circadian regulator BMAL1::CLOCK promotes cell proliferation in hepatocellular carcinoma by controlling apoptosis and cell cycle的研究论文。
该研究首次报道了生物节律核心转录因子复合体BMAL1::CLOCK对肝细胞癌的促进作用。该研究发现,在裸鼠人源肝细胞癌移植瘤中敲减BMAL1或CLOCK基因可显著抑制肿瘤的生长,在细胞水平表现为细胞周期阻滞和细胞凋亡活性升高。BMAL1::CLOCK控制多个细胞周期因子的节律性表达,遗传学鉴定发现其中WEE1和p21共同参与了BMAL1::CLOCK对肝细胞癌生长的促进作用。

不同于正常细胞,肿瘤细胞依赖G2/M期细胞周期检验点以维持基因组稳定性。抑制G2/M期检验点将导致癌细胞携带DNA损伤进行细胞分裂,造成基因组不稳定并触发细胞凋亡。WEE1是参与G2/M期检验点的关键激酶,敲低Wee1基因可抑制癌细胞增殖,因此WEE1抑制剂已被广泛应用于肿瘤临床试验。
研究团队发现BMAL1::CLOCK直接结合肝癌细胞中Wee1基因启动子并促进基因的转录。与此同时,通过调控REV-ERB表达水平,BMAL1::CLOCK间接抑制细胞周期蛋白依赖性激酶抑制剂p21的转录。作为肿瘤抑制因子,p21的高表达导致细胞周期的阻滞,而缺失则会诱导肝细胞的持续增殖及肝癌发生。研究团队进一步证明,过表达WEE1或敲减p21都可一定程度上逆转BMAL1::CLOCK活性降低对肝癌细胞生长的抑制作用。
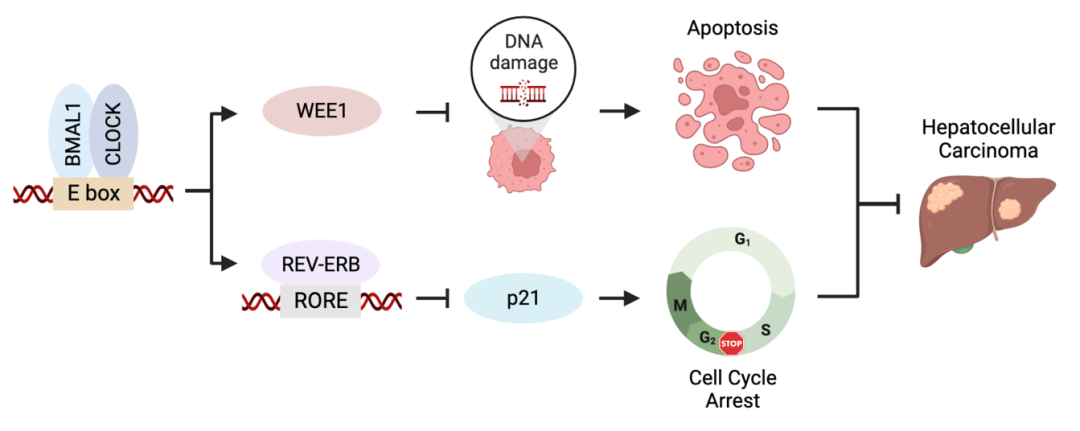
综上所述,该研究为生物节律调控肝癌发生发展提供了分子机制,也为靶标生物钟小分子的开发及在肝癌治疗中的应用提供了理论基础。鉴于WEE1常在肝癌组织中高度表达,而p21更倾向于低表达,未来有望在临床研究中通过抑制BMAL1::CLOCK的活性达到纠正二者表达水平进而治疗肝癌的效果。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nat Biomed Eng:用“声波画笔”调控大脑!新型全息超声技术有望打开人类神经疾病治疗新大门 (2025-10-07)
- 《神经元》:短期高脂饮食也同样危险!科学家发现,两天的高脂饮食即可激活小鼠大脑特定抑制性神经元,导致认知受损,恢复正常饮食可逆转 (2025-10-07)
- 相分离研究登上Nature:超越转录调控,mRNA协调易凝聚蛋白稳态 (2025-10-07)
- 动辄百万美元奖金,这些科学大奖想要与诺贝尔奖竞争:它们含金量如何? (2025-10-06)
- Nature:T细胞耗竭的悖论——并非“精疲力竭”,而是“生产过剩”引发的蛋白毒性风暴 (2025-10-06)
- Cell:沉默的基因组,喧嚣的转录场——解密结核菌适应性的隐藏驱动力 (2025-10-06)
- Nature:谁掌控了人类生命的第一个开关?一个被“驯化”的逆转录病毒的自白 (2025-10-06)
- 三个月,改写生命!全球首例帕金森病实现功能性治愈 (2025-10-05)
- AJP:迄今最长时间真实世界安全性分析显示,艾司氯胺酮鼻喷剂的安全性与临床研究和产品说明书中已确定的一致 (2025-10-05)
- Nature子刊:谭蔚泓/邱丽萍团队开发核酸适配体武装的单核细胞疗法,治疗阿尔茨海默病 (2025-10-05)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















