淋巴瘤新药!TG Therapeutics新一代口服PI3Kδ抑制剂umbralisib在美国申请上市! |
 |

2020年01月18日讯 /BIOON/ --TG Therapeutics是一家致力于为B细胞介导的疾病患者开发创新疗法的生物制药公司。近日,该公司宣布,已启动向美国食品和药物管理局(FDA)滚动提交新药申请(NDA),寻求加速批准该公司口服、每日一次的、磷酸肌醇-3-激酶δ(PI3Kδ)和CK1-ε双效抑制剂umbralisib(TGR-1202),用于先前已接受治疗的边缘区淋巴瘤(MZL)和滤泡性淋巴瘤(FL)患者。该公司已收到FDA的指导,即MZL和FL适应症提交单份DNA是可以接受的。此前,已授予umbralisib治疗MZL的孤儿药资格(ODD)和突破性药物资格(BTD)。该公司预计,将在2020年上半年完成NDA的滚动提交。
TG Therapeutics执行主席兼首席执行官Michael S.Weiss表示:“我们非常高兴启动提交umbralisib的新药申请,并收到了的指导,将MZL和FL纳入单一NDA。这对我们来说是一个极为重要的里程碑,因为它使我们更接近于为之前接受过治疗的MZL和FL患者群体提供一种新的治疗选择。我要感谢参与这些重要试验并帮助推进umbrasib的患者及其家人以及研究团队,以及TG团队为启动本次NDA提交而不懈努力。这是一个有影响的2020年的开始,因为我们期待着UNITY-CLL试验和多发性硬化症ULTIMATE I II试验的III期数据,以及基于这些数据的潜在监管提交。”
此次NDA提交,基于评估umbralisib单药IIb期注册指导临床研究(UNITY-NHL)MZL队列和FL队列的数据。这是一项多中心、开放标签研究,MZL队列旨在评估umbralisib单药治疗MZL患者,这些患者之前至少接受过一种抗CD20方案;FL队列旨在评估umbralisib单药治疗FL患者,这些患者之前接受过至少两种治疗方案,包括抗CD20方案和烷基化制剂;2个队列的主要终点均为独立中央审查委员会(IRC)评估的确定的总缓解率(ORR)。
2019年4月,在美国癌症研究协会(AACR)年会上公布的MZL队列数据显示,在既往已接受至少一种抗CD20疗法的复发性或难治性MZL患者中,umbralisib单药治疗的总缓解率(ORR)为52%,其中完全缓解率(CR)为19%、部分缓解率(PR)为33%,疾病稳定率(SD)为36%。中位随访12.5个月时,中位缓解持续时间(DoR)尚未达到。额外的疗效数据包括:临床受益率88%、86%的患者负担减少、治疗至缓解的中位时间为2.7个月、12个月无进展生存率为66%、中位无进展生存期尚未达到。研究中,umbralisib的耐受性和安全性良好。
2019年10月,TG公司宣布:FL队列达到了由IRC评估确定的所有治疗患者(n=118)的ORR主要终点,结果达到了该公司ORR为40-50%的目标指导值。重要的是,umbralisib单药治疗耐受性良好,安全性与之前报告的一致。详细数据将在未来召开的医学上公布。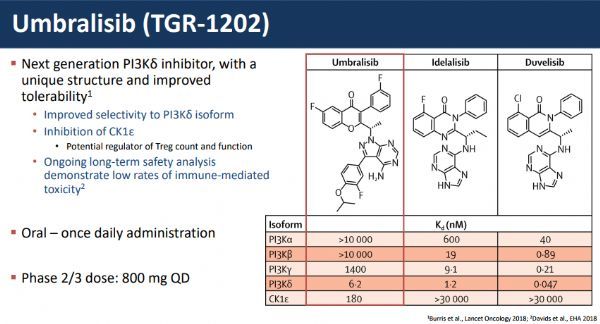
umbralisib是一种口服、每日一次的PI3Kδ和CK1-ε双效抑制剂,这可能使其克服第一代PI3Kδ抑制剂相关的某些耐受性问题。磷脂酰肌醇-3激酶(PI3K)是一类参与细胞增殖和存活、细胞分化、细胞内运输和免疫等多种细胞功能的酶。PI3K有四种亚型(α、β、δ和γ),其中δ亚型在造血来源的细胞中强烈表达,常与B细胞相关淋巴瘤有关。
umbrasib对PI3K的δ亚型具有摩尔效力,并且对α、β、γ亚型具有高选择性。umbralisib还独特地抑制酪蛋白激酶1-ε(CK1-ε),这可能具有直接的抗癌作用,也可能调节先前PI3K抑制剂中观察到的与免疫介导不良事件相关的T细胞活性。
当前已批准的PI3Kδ抑制剂与介导的毒性有关,如肝毒性、肺毒性和结肠炎。与已批准的PI3K抑制剂相比,umbralisib的特异性差异、其对CK1-ε的独特抑制作用以及其独特和专利的化学结构可能会在PI3K抑制剂类中具有差异化特征。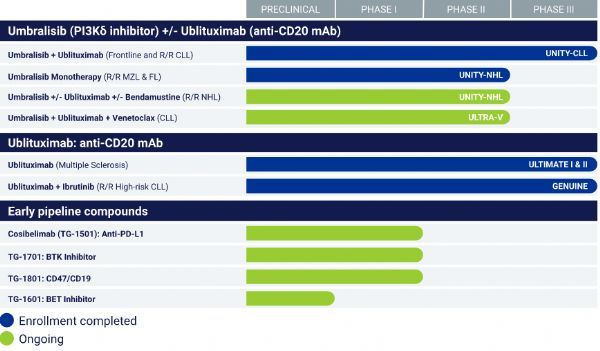
umbralisib已在血液系统恶性的临床前模型和临床研究中证明了其活性。目前,在CLL和NHL患者中开展的IIb期和III期试验正在继续评估umbralisib的治疗潜力。
除了umbralisib之外,TG公司也正在开发一款ublituximab(TG-1101),这是一种糖工程化嵌合IgG1单克隆抗体,靶向CD20,目前处于III期临床开发,评估治疗癌症(慢性淋巴细胞[CLL]、非霍奇金淋巴瘤[NHL])和非癌症(多发性骨髓瘤[MM])适应症。此外,TG公司还有多款资产进入了I期临床,包括PD-L1单抗TG-1501、共价结合布鲁顿酪氨酸激酶(BTK)抑制剂TG-1701等。(100医药网100yiyao.com)
医药网新闻
- 相关报道
-
- Science:一种经过改造的肠道细菌有望对抗肾结石 (2025-07-26)
- Science:人类首次实现 用“专属食物”精准遥控肠道内的活体药物 (2025-07-26)
- Science子刊:一种新发现的lncRNA可能解释了2型糖尿病患者肌肉量减少的原因 (2025-07-26)
- 中国药企如何“智闯”沙特? (2025-07-26)
- 马来西亚医疗旅游理事会推出MYMT 2026,打造马来西亚首个医疗旅游年 (2025-07-25)
- Int J Radiat Oncol Biol Phys:MRI导航精准放疗——让高剂量直击肿瘤顽固区,疗效提升还不伤正常组织 (2025-07-25)
- 研究发现乳酸穿梭调控巨噬细胞极化并参与2型糖尿病进程 (2025-07-25)
- 癫痫手术步入毫米时代,仁济多学科联手“机器人+激光”精准消除脑内病灶 (2025-07-25)
- Science:从源头看懂食物过敏——生命早期的一波Thetis细胞浪潮,决定你一生的饮食自由 (2025-07-25)
- Mol Neurodegener:血管“信使”藏玄机,内皮糖蛋白借囊泡激活星形胶质细胞,为阿尔茨海默病治疗指新向 (2025-07-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040
 |
 |
| 解决便秘的偏方 | 女孩向往 |
 |
 |
| 婴儿出生时瞬间 | 西红柿养生功效 |
|


















