20亿市场新变局,石药、恒瑞接手国采紫杉醇供应! |
 |
医药网3月31日讯 3月27日,国家组织药品集中采购和使用联合采购办公室(下称“联采办”)发布《关于确定部分地区注射用紫杉醇(白蛋白结合型)替补供应企业的通知》,确定由石药集团欧意药业有限公司和江苏恒瑞医药股份有限公司作为原新基(Celgene)供应地区的替补供应企业。同时,联采办相关负责人就有关问题回答记者的提问。
原研药不存在“超国民待遇”
此前,因不符合GMP要求,国家药品监督管理局发公告称,决定暂停进口、销售和使用Celgene Corporation的注射用紫杉醇(白蛋白结合型),这一大品种市场生变。米内网数据显示,注射用紫杉醇(白蛋白结合型)在国内重点省市公立医院终端市场2018年的销售额为21.3亿元,2019年前3季度的销售额为21.1亿元。
联采办相关负责人指出,此次取消美国Celgene Corporation注射用紫杉醇(白蛋白结合型)中选资格,是按照《国务院办公厅关于印发国家组织集中采购和使用试点方案的通知》(国办发〔2019〕2号)关于“出现不按合同供货、不能保障质量和供应等情况时,要相应采取赔偿、惩戒、退出、备选和应急保障措施,确保药品质量和供应”的规定,以及《全国药品集中采购文件》(GY-YD2019-2)关于中选产品出现质量和供应问题无法履行协议的规定。
《全国药品集中采购文件》(GY-YD2019-2)中明确,采购周期内中选企业出现无法供应等情况,致使协议无法继续履行时,从本次药品集中采购该品种其他中选企业中确定替补的供应企业。据此,由注射用紫杉醇(白蛋白结合型)的其他两家中选企业石药集团欧意药业、江苏恒瑞医药分别按其中选价格,替补供应原定由美国Celgene Corporation供应的省份。
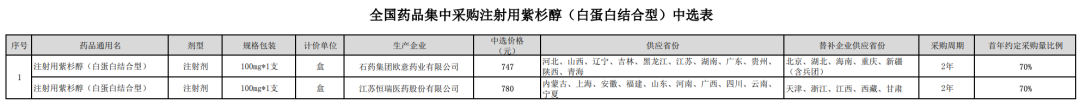
美国Celgene Corporation是注射用紫杉醇(白蛋白结合型)的原研生产企业,在今年1月确定的第二轮全国集采名单中,其白蛋白紫杉醇作为为数不多的几个原研药中选。该公司与当时国内3家视同通过一致性评价的公司(分别为江苏恒瑞、石药欧意和齐鲁制药)共同参与竞标,并以第三顺位价格入围。
前述负责人指出,对这次事件的处置,充分体现了国家组织药品集中采购对内外资企业一视同仁、严格要求、质量问题零容忍的态度。同时提醒所有企业,药品质量直接关系人民健康,无论外资或内资,原研药或仿制药,境外或境内生产,都要强化质量意识、切实负责起质量责任,在质量问题上没有例外,不存在“超国民待遇”。
替补后“实质性降价”
考虑到在集采竞标时,石药欧意、江苏恒瑞和Celgene Corporation(由百济神州代理商业化)分别以747、780、1150元的报价中标。而在替补供应原则中规定,欧意药业、江苏恒瑞医药将分别按其中选价格,替补供应原定由美国Celgene Corporation供应的省份,也就是说原研厂家的出局,为白蛋白紫杉醇的集采价带来又一波下降。
联采办相关负责人指出,此次替补程序严格依据采购文件相关条款规定,由相关省份委托联采办,确认其他两家中选企业的意愿后,按照《全国药品集中采购文件》(GY-YD2019-2)关于中选企业选择供应省份的规则,由上述两家替补企业选择供应省份。替补后,各省约定采购量和采购协议周期不变。目前,已顺利完成以上替补程序,联采办已就结果发布了通知。
联采办也指出,“由石药集团欧意药业和江苏恒瑞医药接替Celgene Corporation供应,相关省份群众的用药负担会有所下降。”而对于记者提出的有关供应企业替补后能否确保临床使用一问,前述负责人称“根据企业申报材料,两家替补公司产能充足,能够保障相关省份该品种的稳定供应。”
BMS/百济神州紧急回应
国家药监局的禁令发布之后,百济神州紧急发布了对白蛋白紫杉醇中国供应情况的更新。百济神州创始人、首席执行官兼董事长欧雷强先生在声明中表示,作为ABRAXANE®在中国的销售代理,对此次供应中断感到非常失望。在百济神州,药品质量是重中之重。百济神州要求自己和合作伙伴都履行最高行业标准。百济神州正在与百时美施贵宝沟通,尽快进行整改工作。
而百济神州也强调,根据和新基签订的协议,百济神州负责该产品在中国的推广和销售,百时美施贵宝负责按照法规要求进行生产、注册和进口许可证的维护,以及为中国市场提供成品制剂。除了正在进行的、对现有合同生产机构的整改工作外,BMS已向国家药品监督管理局递交更换生产厂的补充申请,从其另一家工厂为中国供货。该申请目前正在审评中。
除百济神州之外,BMS 也在3月26日作出了回应,表示最近国家药品监督管理局在对美国新基公司的注射用紫杉醇(白蛋白结合型)的第三方受托生产企业的生产流程检验的过程中,发现了一些有待进一步改进的方面。BMS对此非常重视,正积极配合监管部门与该第三方受托生产企业密切合作,以帮助其采取针对性的相应整改措施;同时,作为备选方案,BMS也在进行替代工厂的注册申请,以期尽快恢复注射用紫杉醇(白蛋白结合型)在中国大陆市场的供应。
声明中也强调,在这段时期内,国家药品监督管理局决定暂停进口、销售和使用美国新基公司的注射用紫杉醇(白蛋白结合型)。该决定并不影响BMS在中国大陆以外的市场,继续供应美国新基公司的注射用紫杉醇(白蛋白结合型)。同时,也没有其他任何BMS药品在该第三方受托生产企业生产。
医药网新闻
- 相关报道
-
- 对于进一步欠缺医药价钱和招采信誉评估轨制的关照 (2025-06-06)
- 首个国产九价HPV疫苗获批上市 (2025-06-05)
- 辅助生殖用度怎样报销?——海南省辅助生殖报销政策 (2025-06-05)
- 本年11月尾前完成全国三级公立西医院儿科设置全笼罩 (2025-06-04)
- 对于医防管穿插复合型策略人才步队建设倒退的意见 (2025-06-04)
- 再次征求对于增强药品受托临盆监视治理任务的布告 (2025-06-03)
- 药品追溯码入库环节信息采集光阴紧缩至1分钟左右 (2025-06-03)
- 我国已同意宣布儿童相关畛域国度尺度210余项 为儿童安康生长保驾护航 (2025-06-03)
- 山东为儿童筑起安康防地 动静展开疾病筛查和干涉 (2025-05-30)
- 匆匆进窘境儿童安康生长 五部分部署展开主题运动 (2025-05-30)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















