自然:阿尔法折叠和人工智能蛋白质折叠革命的下一步是什么 |
 |
事实证明,大多数使用ColabFold的研究人员只是想得到一个蛋白质结构。但其他研究人员将其作为一个平台,修改AlphaFold的输入,以解决新的应用。Jumper说,我没想到会有各种各样的黑客攻击。
到目前为止,最受欢迎的黑客攻击是在蛋白质复合物上使用这种工具,蛋白质复合物由几个相互作用的-通常相互交织的-肽链组成。就像核孔复合物一样,细胞中的许多蛋白质在与多个蛋白质亚基形成复合物中起作用。
AlphaFold旨在预测单个肽链的形状,其训练完全由这种蛋白质组成。但是这个网络似乎已经了解了复合材料是如何折叠在一起的。在AlphaFold的代码发布几天后,来自东京大学蛋白质的生物信息学家Yoshitaka Moriwaki在Twitter上表示,如果用一个长的链接序列将两个蛋白质序列缝合在一起,它可以准确预测它们之间的相互作用。Baek很快分享了另一种预测从RoseTTAFold的发展中收集的化合物的技术。
ColabFold后来增加了预测化合物的能力。2021年10月,DeepMind发布了一个名为AlphaFold-Multimer的更新。与前者不同,它是专门为蛋白质化合物而训练的。Jumper的团队将其应用于PDB的数千种化合物,发现它预测了大约70%的已知蛋白质相互作用。
这些工具已经在帮助研究人员发现潜在的新蛋白质伙伴。Elofsson的团队使用AlphaFold预测了6.5万个人类蛋白质对的结构,根据实验数据怀疑这些蛋白质对存在相互作用。贝克领导的团队使用AlphaFold和RoseTTAFold模拟了酵母编码的几乎每一对蛋白质之间的相互作用,发现了100多种以前未知的化合物。埃洛夫松说,这样的筛选只是一个起点。他们在预测一些蛋白质配对方面做得很好,特别是稳定的蛋白质配对,但很难识别更多的瞬时相互作用。埃洛夫松说,‘看起来不错并不意味着它就是对的。你需要一些实验数据来证明你是对的。
Kosinski说,核孔复合体的工作是预测和实验数据可以一起工作的一个很好的例子。这并不像我们把所有的30种蛋白质都扔进折叠中,然后得到结构。为了将预测的蛋白质结构放在一起,该团队使用了核孔复合物的三维图像,这些图像是由一种称为低温电子断层扫描的低温电磁形式捕获的。在一个例子中,一个可以确定蛋白质接近程度的实验发现了化合物的两种成分之间令人惊讶的相互作用,这一点随后被AlphaFold的模型所证实。
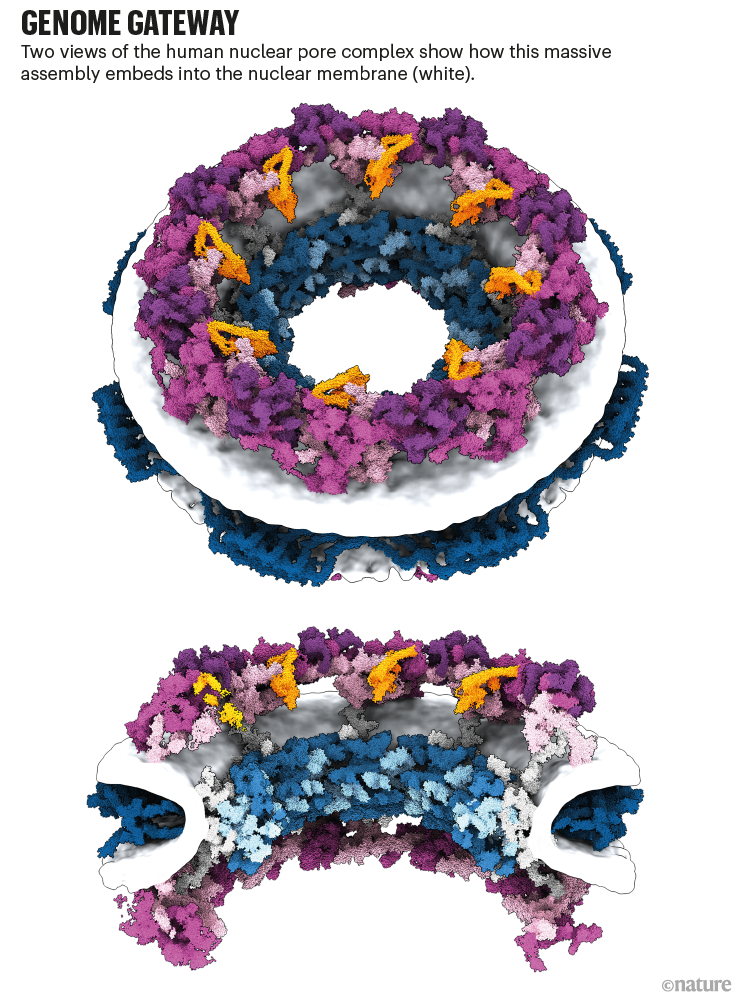
Gateway:人类核孔复合体的两个视图显示了它是如何嵌入核膜的。
医药网新闻
- 相关报道
-
- Science:一种经过改造的肠道细菌有望对抗肾结石 (2025-07-26)
- Science:人类首次实现 用“专属食物”精准遥控肠道内的活体药物 (2025-07-26)
- Science子刊:一种新发现的lncRNA可能解释了2型糖尿病患者肌肉量减少的原因 (2025-07-26)
- 中国药企如何“智闯”沙特? (2025-07-26)
- 马来西亚医疗旅游理事会推出MYMT 2026,打造马来西亚首个医疗旅游年 (2025-07-25)
- Int J Radiat Oncol Biol Phys:MRI导航精准放疗——让高剂量直击肿瘤顽固区,疗效提升还不伤正常组织 (2025-07-25)
- 研究发现乳酸穿梭调控巨噬细胞极化并参与2型糖尿病进程 (2025-07-25)
- 癫痫手术步入毫米时代,仁济多学科联手“机器人+激光”精准消除脑内病灶 (2025-07-25)
- Science:从源头看懂食物过敏——生命早期的一波Thetis细胞浪潮,决定你一生的饮食自由 (2025-07-25)
- Mol Neurodegener:血管“信使”藏玄机,内皮糖蛋白借囊泡激活星形胶质细胞,为阿尔茨海默病治疗指新向 (2025-07-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040
 |
 |
| 解决便秘的偏方 | 女孩向往 |
 |
 |
| 婴儿出生时瞬间 | 西红柿养生功效 |
|


















