一年前 张峰的科学论文成功转型为一家新公司 融资2亿美元 开创了mRNA传递的新方式 |
 |
来源:生物世界2022-10-14 1:21
这种新的递送平台SEND可以在细胞模型中有效工作,随着它的进一步发展,它可以为广泛的分子药物开辟一类新的递送方法,包括基因编辑和基因替换。
目前,用于人类基因治疗的递送载体主要有慢病毒、腺病毒、腺相关病毒(AAV)、脂质纳米粒(LNP)等。然而,这些递送载体中的一些将随机整合到基因组中,一些将是低效的,一些将导致不必要的反应。
整个生物医学界都在努力开发新的更强的分子疗法,但将这些疗法准确有效地传递到细胞中充满了挑战。现在,张峰为这些挑战带来了一个全新的答案,试图解决基因编辑/基因治疗交付的最大问题。
日前,据美国科技媒体Business Insider报道,张峰创办了一家名为Aera Therapeutics的新公司,这也是张峰创办的第七家生物技术公司。此前,张峰曾参与建立了Editas、Beam、Pairwise、夏洛克、arbor和Proof Diagnostics,涵盖了CRISPR-Cas9基因编辑疗法、碱基编辑疗法、基于CRISPR的农业育种、基于CRISPR和新型基因编辑工具的开发。
目前,Aera Therapeutics已完成由Arch和Google Ventures提供的2亿美元融资。目前公司还处于隐身状态,更多信息还不得而知。但这家公司是基于张峰实验室一年前发表的一篇科学论文。接下来,我们将通过本文了解张峰这家新公司的底层技术和发展方向。
2021年8月19日,张峰的团队发表了一篇研究论文,题为:哺乳动物逆转录病毒样蛋白peg 10包装自己的mrna,并可以为mrna递送进行伪分型[1]。
研究团队开发了一个全新的RNA递送平台SEND(选择性内源封装用于细胞递送)。SEND的核心是逆转录病毒样蛋白PEG10,它可以与自身的mRNA结合,并在其周围形成一个球形保护囊。研究小组对其进行了修改,并将其设计为包装和运送RNA。
研究团队使用SEND系统将CRISPR-Cas9基因编辑系统递送到小鼠和人类细胞中,并成功编辑了目标基因。这将为基因治疗提供一种全新的递送载体。SEND系统利用人体成分自我组装成类似病毒的颗粒。与其他传递载体相比,它引起的免疫反应更少,更安全。
张峰说,SEND技术可以补充现有的病毒递送载体和脂质纳米颗粒,以扩展基因递送和编辑治疗细胞的工具箱。

受逆转录转座子启发
在整个进化过程中,逆转录病毒和逆转录病毒元件将它们的遗传密码插入到哺乳动物的基因组中。尽管许多这些整合的病毒样序列威胁着宿主基因组的完整性,但其中一些序列已被哺乳动物细胞重组,在发育中发挥重要作用。其中,约8%的人类基因组是远古时期感染人类的逆转录病毒的残余。
PEG10蛋白天然存在于人体内,来源于逆转录转座子,一种类似病毒的遗传元件。他们在数百万年前将自己整合到人类祖先的基因组中。随着时间的推移,PEG10已经被人体吸收,成为对生命非常重要的蛋白质库的一部分。
2018年1月,犹他大学Jason Shepherd的实验室在Cell上发表了一篇论文[2]。这项研究发现,反转座子衍生蛋白ARC可以形成病毒样结构,参与细胞间RNA的转移。

这项研究表明,有可能设计反转录转座子蛋白作为递送平台,但当时,这些蛋白尚未成功用于在哺乳动物细胞中包装和递送特异性RNA。
值得一提的是,杰森谢泼德(Jason Shepherd)基于这项研究创立的公司VNV(Chris)已被Aera Therapeutics收购,杰森谢泼德也曾担任Aera的科学顾问。
为了探索反转录转座子作为基因传递平台的潜力,张峰的团队开始在人类基因组中系统地寻找这种蛋白质,寻找能够形成保护性被膜的蛋白质。经过初步分析,张峰的团队发现人类基因中有48个编码蛋白质的基因,其中19个在小鼠和人类中都存在。
在体外细胞实验中,张峰的团队发现,在这些蛋白质中,PEG10具有最突出的潜力,细胞可以释放PEG10颗粒,这些PEG10颗粒中的大多数也含有自己的mRNA,这表明PEG10可能能够包装特定的RNA分子。
开发交付平台
将PEG10发展成为一个交付平台
,张锋团队对PEG10进行了改造,首先,他们在PEG10的mRNA序列中找到了识别和包装其RNA的序列,然后对PEG10蛋白和该mRNA序列进行改造,以便PEG10能够选择性包装RNA。然后研究团队用融合蛋白修饰PEG10蛋白,以促进其与细胞膜的融合,帮助其更好地进入细胞。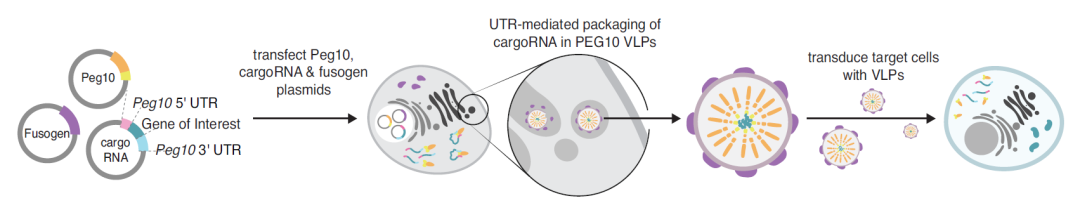
通过这一系列的改造,PEG10有望靶向特定种类的细胞、组织或器官,并进行RNA递送。
推进基因治疗
SEND系统由人体内自然产生的蛋白质组成,这意味着它可能不会触发免疫反应。如果后续进一步研究证实了这一点,那么SEND将有望成为具有最小副作用的可重复使用基因治疗递送载体。
张锋团队使用SEND成功将CRISPR-Cas9系统以mRNA形式成功递送至人类和小鼠细胞中,并编辑了特定基因。接下来,张锋团队还将在动物中进一步测试SEND,并对其进行进一步改造设计,使该系统能够向各个组织和细胞中递送mRNA。
张锋表示,这项研究表明,可以利用PEG10以及人体中其他类似蛋白质来设计新的递送载体,并开发出新的基因疗法。
这一全新递送平台SEND能够在细胞模型中有效工作,并且随着进一步发展,可以为广泛的分子药物开辟一类新的递送方法 包括用于基因编辑和基因替换。SEND技术也将补充病毒递送载体和脂质纳米颗粒,以进一步扩展向细胞递送基因和编辑疗法的工具箱。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:DNA甲基化“随机时钟”——EVOFLUX破译肿瘤演化史,重塑临床预后新维度 (2025-09-13)
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















