Cell:来自不可培养细菌的抗生素Clovibactin有望高效攻击有害细菌,同时不会触发细菌耐药性产生 |
 |
来源:100医药网原创 2023-09-23 13:49
在一项新的研究中,来自荷兰乌特勒支大学、德国波恩大学、德国感染研究中心、美国东北大学和 NovoBiotic 制药公司的研究人员发现一种从以前无法研究的细菌中分离出来的新型强效抗生素似乎能够对付有害细在一项新的研究中,来自荷兰乌特勒支大学、德国波恩大学、德国感染研究中心、美国东北大学和 NovoBiotic 制药公司的研究人员发现一种从以前无法研究的细菌中分离出来的新型强效似乎能够对付有害细菌,甚至是具有多重耐药性的 超级细菌 。这种抗生素被命名为 Clovibactin,能够以一种不同寻常的方式杀死细菌,使细菌更难产生耐药性。相关研究结果发表在2023年9月14日的Cell期刊上,论文标题为 An antibiotic from an uncultured bacterium binds to an immutable target 。

迫切需要新的抗生素
抗生素耐药性是人类健康面临的一个重大问题,全世界的科学家们都在寻找新的解决方案。论文共同通讯作者、乌特勒支大学化学系研究员 Markus Weingarth 博士说, 我们迫切需要新的抗生素来对付对大多数临床使用的抗生素产生越来越强耐药性的细菌。
然而,发现新抗生素是一项挑战:过去几十年来,几乎没有新抗生素被引入临床,而且即便有新的抗生素,它们往往与已知的老抗生素相似。
Weingarth说, Clovibactin与众不同。由于 Clovibactin是从以前无法生长的细菌中分离出来的,致病细菌以前没有见过这种抗生素,没有时间产生耐药性。
来自细菌暗物质的抗生素
Clovibactin是由美国一家小型早期公司NovoBiotic 制药公司和东北大学微生物学家Kim Lewis教授共同发现的。早些时候,他们开发了一种设备,可以培养 细菌暗物质(bacterial dark matter) ,即所谓的不可培养细菌。
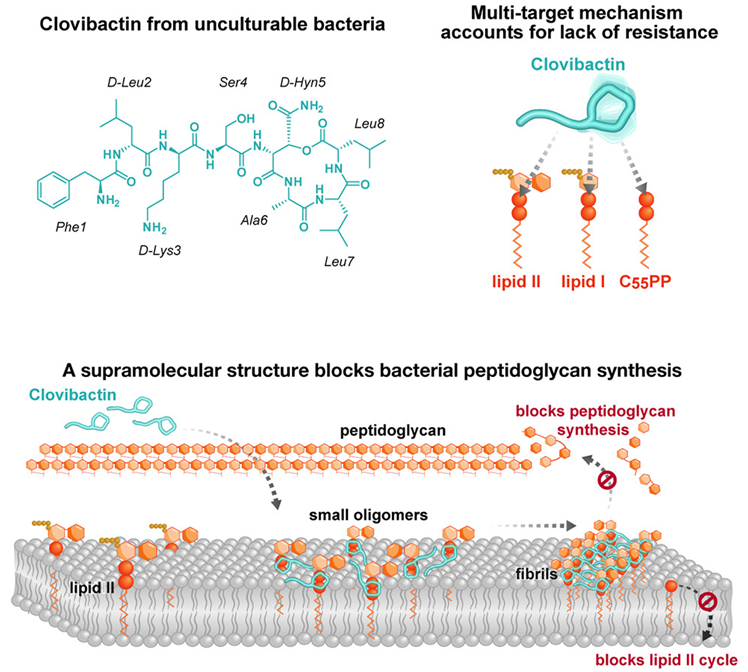
图片来自Cell, 2023, doi:10.1016/j.cell.2023.07.038。
耐人寻味的是,99% 的细菌都是 不可培养的 ,以前无法在实验室中培养,因此也就无法用来开发新型抗生素。美国研究人员利用这种名为 iCHip 的新设备,在从北卡罗来纳州的沙质土壤中分离出的一种名为 Eleftheria terrae ssp.Carolina的细菌中发现了Clovibactin。
在这项新的研究中,NovoBiotic 制药公司发现Clovibactin 能成功攻击多种细菌病原体。它还成功治疗了感染超级细菌金黄色葡萄球菌的小鼠。
广泛的靶标谱
Clovibactin 的杀菌机制似乎与众不同。它不仅靶向一种前体分子,而且靶向三种不同的前体分子,这些前体分子都是构建细胞壁所必需的。这是论文共同通讯作者、波恩大学的Tanja Schneider教授及其研究团队发现的。
Schneider说, Clovibactin的多靶标攻击机制能够在不同位置同时阻断细菌细胞壁的合成。这提高了药物的活性,并大大增强了细菌耐药性产生的门槛。
笼状结构
Weingarth博士及其研究团队揭开了 Clovibactin 究竟如何阻断细菌细胞壁合成。他们利用一种名为固态核磁共振(NMR)的特殊技术,研究了 Clovibactin 在细菌中等类似条件下的作用机制。
Weingarth 说, Clovibactin就像一只紧紧围住焦磷酸的手套。这就是 Clovibactin 的名字由来,它源自希腊语 Klouvi ,意思是笼子。
Clovibactin杀菌机制的显著特点是,它只与细胞壁前体分子中常见的不可改变的焦磷酸结合,却忽略了靶标中可变的糖肽部分。 由于 Clovibactin 只与靶标中不变的、保守的部分结合,细菌将更难对它产生耐药性。事实上,我们在这项新研究中没有观察到任何针对 Clovibactin 的耐药性。
纤维捕获靶标
Clovibactin 还能做得更多。在与靶分子结合后,它会在细菌膜表面自组装成较大的纤维。这些纤维可长期稳定存在,从而确保靶分子在杀灭细菌所需的时间内一直处于封闭状态。
Weingarth说, 由于这些纤维只在细菌膜上形成,而不在人类膜上形成,因此它们可能也是Clovibactin选择性地破坏细菌细胞而对人类细胞无毒的原因。因此,Clovibactin 有潜力用于设计在杀死细菌病原体的同时不会产生耐药性的改良药物。 ( 100yiyao.com)
参考资料:
1. Rhythm Shukla et al. . Cell, 2023, doi:10.1016/j.cell.2023.07.038.
2. New antibiotic from microbial dark matter could be powerful weapon against superbugs
https://www.uu.nl/en/news/new-antibiotic-from-microbial-dark-matter-could-be-powerful-weapon-against-superbugs
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature Materials:清华大学喻国灿/程功等开发新型LNP,不在肝脏蓄积,让mRNA疫苗更安全、更高效 (2025-08-06)
- Nature头条:超加工食品让减肥更加困难,还会影响心血管代谢健康 (2025-08-06)
- 北京生命科学研究所发表最新Cell论文 (2025-08-06)
- STM:中山大学团队找到肠癌“照妖镜”,首次发现抑制SIRT2可以让肠癌细胞“现身”! (2025-08-05)
- Nature:王者换代?AI设计的OpenCRISPR-1正式挑战Cas9霸主地位,开启基因编辑新范式 (2025-08-05)
- Cell:顾名夏/苗一非/郭敏哲团队,在同一个球状体中实现肺和肠道类器官的血管化,成功构建多谱系类器官 (2025-08-05)
- 《细胞》:中美团队首次发现,分泌蛋白AOAH可以解除肿瘤对T/树突细胞的免疫抑制! (2025-08-05)
- Nature子刊:仅仅看到病人,大脑就会激活免疫系统,让身体提前做好防御准备 (2025-08-04)
- 困扰韦东奕的牙周问题有救了?王松灵院士团队发表牙髓干细胞治疗牙周炎的临床试验数据 (2025-08-04)
- Cell子刊:赖仞团队揭示高脂饮食通过肠道细菌促进血栓形成的新机制 (2025-08-04)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















