《Gastric Cancer》揭示幽门螺杆菌通过TLR6通路诱导宿主免疫耐受机制 |
 |
来源:网络 2024-07-17 09:34
幽门螺杆菌是最早被发现能在人类胃内寄生的微生物,已感染了超过50%的人类。Hp与胃炎和胃癌等疾病密切相关,被世界卫生组织定为一类致癌物。近日,首都医科大学基础医学院李长龙副教授团队在《Gastric Cancer》上发表题为 Sustained exposure toHelicobacter pylori induces immune tolerance bydesensitizing TLR6 的研究论文。该研究揭示了(Hp)持续感染过程中,通过调控宿主胃上皮细胞TLR6/JNK信号通路抑制IL-8分泌,减少中性粒细胞募集从而实现逃逸的机制。该发现为Hp的清除治疗提供了新的策略。首都医科大学基础医学院章秀林博士为该论文的第一作者,李长龙副教授为通讯作者。

Hp是最早被发现能在人类胃内寄生的微生物,已感染了超过50%的人类。Hp与胃炎和等疾病密切相关,被世界卫生组织定为一类致癌物。Hp感染胃上皮后,会诱发持续的炎症反应并导致细胞增殖和DNA复制错误的增加,进而促进肿瘤发生。胃上皮细胞是固有免疫反应的第一道防御屏障,其表面Toll样受体(TLRs)对微生物成分敏感。Hp在长期感染过程中通过干扰免疫应答来逃避宿主免疫系统的清除。TLRs已被证实在微生物病原体诱导的免疫耐受中起到关键作用,但Hp通过TLR信号通路诱导免疫耐受的具体机制尚不清楚。
该研究将胃上皮细胞GES-1与Hp和Hp裂解液进行持续30代的共培养,以模拟体内感染情况。同时构建感染Hp 90周的长爪沙鼠动物模型。动态追踪GES-1细胞和长爪沙鼠在Hp感染过程中TLRs通路及炎症因子表达变化。结果发现,Hp的急性感染能迅速激活TLR6炎症通路。在Hp的慢性感染期,TLR6对细菌成分敏感性降低,IL-1 、IL-8等表达被抑制。在慢性感染期激活TLR6/JNK信号通路可增强胃上皮IL-8表达,从而促进中性粒细胞募集,减少Hp在长爪沙鼠胃黏膜的定植。结果表明,TLR6可能成为Hp清除治疗的潜在靶点。
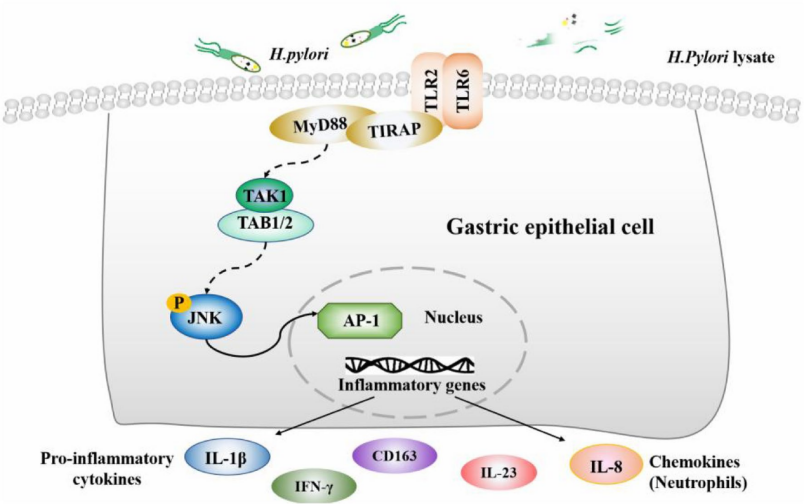
幽门螺杆菌通过TLR6/JNK信号通路上调促炎因子表达的机制
该研究受国家(332070537)、北京市教委重点项目(KZ20210025037)和科技部重点研发项目(2022YFF0711005)的资助。

李长龙,首都医科大学基础医学院医学遗传学与发育生物学学系副教授,硕士生导师。长期从事实验动物疾病模型及幽门螺杆菌感染致胃癌的机制研究。近5年主持国家自然科学基金2项、科技部重点研发计划子课题1项、北京科委重大专项课题1项、北京教委重点课题1项,发表论文20余篇,参编北京市地方标准6项、专著2部。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Cell:RAEFISH技术为研究复杂组织中的RNA活性提供了更大、更好的窗口 (2025-10-27)
- 关于举办“损容性皮肤病及医美”稳态管理创新人才高级培训班的通知 (2025-10-27)
- 东北林业大学,首次发表Science论文 (2025-10-27)
- 雷浪潮:建设生养敌对型社会 推进老有所养、老有所为 (2025-10-27)
- 第八届中国医疗东西立异守业年夜赛总决赛在津启幕 (2025-10-27)
- 三阴性乳腺癌迎“破局者”!J Hematol Oncol:现货 CAR-NKT 细胞三重绞杀肿瘤,成本直降90% (2025-10-27)
- Nature子刊:多发性硬化症与独特的口腔微生物组相关联 (2025-10-27)
- Oncogene:帕博西尼和泰拉格司他组合使用有望治疗结直肠癌 (2025-10-27)
- Nature Aging:胡洪波/张惠媛/吴玉章/胡佳团队绘制人类T细胞衰老图谱 (2025-10-26)
- Nat Metab:厦门大学林圣彩团队揭示葡萄糖感知通路的关闭是维持大脑髓鞘修复的关键 (2025-10-26)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















