《免疫》:反复横跳!科学家发现,衰老癌细胞释放的线粒体DNA,会通过激活cGAS |
 |
《免疫》:反复横跳!科学家发现,衰老癌细胞释放的线粒体DNA,会通过激活cGAS-STING通路,发挥免疫抑制作用
来源:奇点糕 2025-04-20 09:51
针对性阻断mtDNA释放的关键通道,才有望逆转免疫抑制。近日,瑞士肿瘤研究所(IOR)团队在Immunity期刊发表的研究成果[1]就显示,被抗癌治疗诱导衰老的,可将自身的线粒体DNA(mtDNA)装进囊泡释放到细胞外,随后这些囊泡会被肿瘤微环境中的多形核髓系来源抑制细胞(PMN-MDSCs)摄取,使mtDNA激活cGAS-STING-NF- B信号,增强PMN-MDSCs的免疫抑制性。只能说,老而不死的癌细胞也太阴险了,针对性阻断mtDNA释放的关键通道,才有望逆转免疫抑制。

一图总结论文主要发现
其实从分类来说,mtDNA此前更多是被划分到细胞释放的损伤相关分子模式(DAMPs)之中,全身各处的免疫细胞可通过cGAS等感受器感知到游离mtDNA,进而激活与、炎症性疾病乃至癌症对应的免疫应答[2];2023年登上《自然》的一项研究[3]还显示,凋亡应激可促使衰老细胞将mtDNA释放到细胞外驱动SASP进程,算是 机制共享 了。
而化疗、等常用抗癌治疗手段,也经常会诱导癌细胞进入衰老状态,这些衰老癌细胞会不会也通过释放mtDNA造成负面影响呢?本次瑞士研究者们的探索就基于上述猜想展开,研究者们首先在多个不同细胞衰老模型中证实,衰老细胞释放mtDNA是普遍现象,且被多西他赛化疗或CDK4/6抑制剂治疗诱导衰老的癌细胞(细胞)也是如此。
在相应的前列腺癌肿瘤模型中,示踪实验也表明主要负责摄取mtDNA的正是PMN-MDSCs,且mtDNA是被装在胞外囊泡(EVs)内被衰老癌细胞释放出去,再被PMN-MDSCs吞噬进胞内的;随后,PMN-MDSCs的多个免疫抑制功能相关基因(如编码PD-L1的Cd274)表达就开始显著上调,NF- B、IL-6-STAT3等促癌信号通路也被激活,直接用mtDNA处理PMN-MDSCs也有相同效果,实锤了mtDNA可诱导免疫抑制。
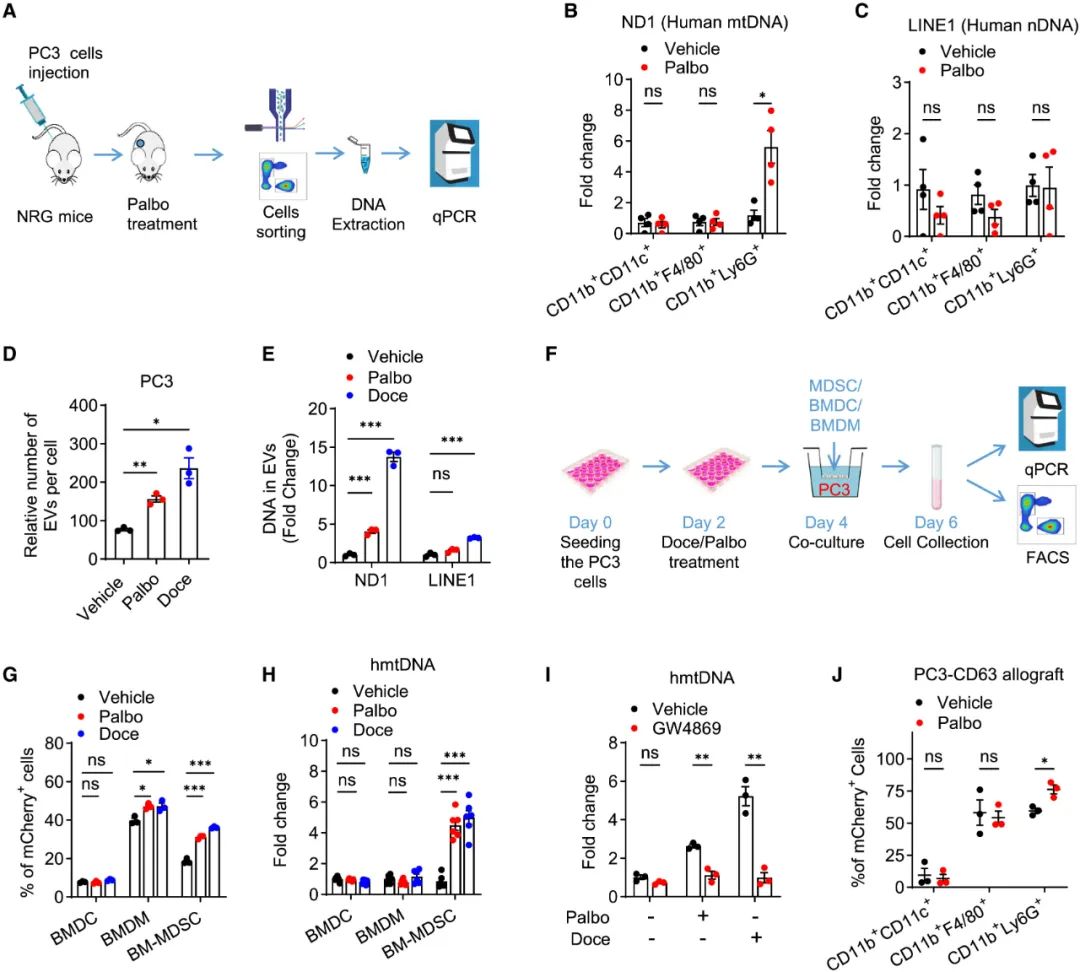
衰老癌细胞可将mtDNA包在EVs内释放,诱导PMN-MDSCs增强免疫抑制作用
而细胞内能够感知mtDNA等核酸的,就是cGAS及Toll样受体9(TLR9)等经典感受器,实验显示敲除PMN-MDSCs的cGAS,才能使mtDNA无法诱导免疫抑制增强;而cGAS感受到mtDNA后,主要会激活STING而非I型干扰素信号(IRF3-IFN轴),再由STING介导PKR样内质网激酶(PERK)来放大NF- B通路信号(PERK-eIF2 通路可抑制NF- B p65抑制蛋白I B 的翻译),完成对免疫抑制性增强的调控。
回过头来说上游mtDNA的来路,导致它们被释放出来的直接原因,是癌细胞进入衰老状态时线粒体功能异常,生成了更多线粒体活性氧(mtROS),它们一方面会使mtDNA被释放到胞浆,再经由电压依赖性阴离子通道(VDACs)排到细胞以外,另一方面还会使核酸内切酶G(EndoG)发生核转位,避免它们去降解mtDNA;而要逆转mtDNA诱导的免疫抑制,最好的干预目标就是现阶段恰好有药物可用的VDAC(在研抑制剂VBIT-4),实验也证实抑制VDAC可通过增强抗应答,改善CDK4/6抑制剂的疗效。
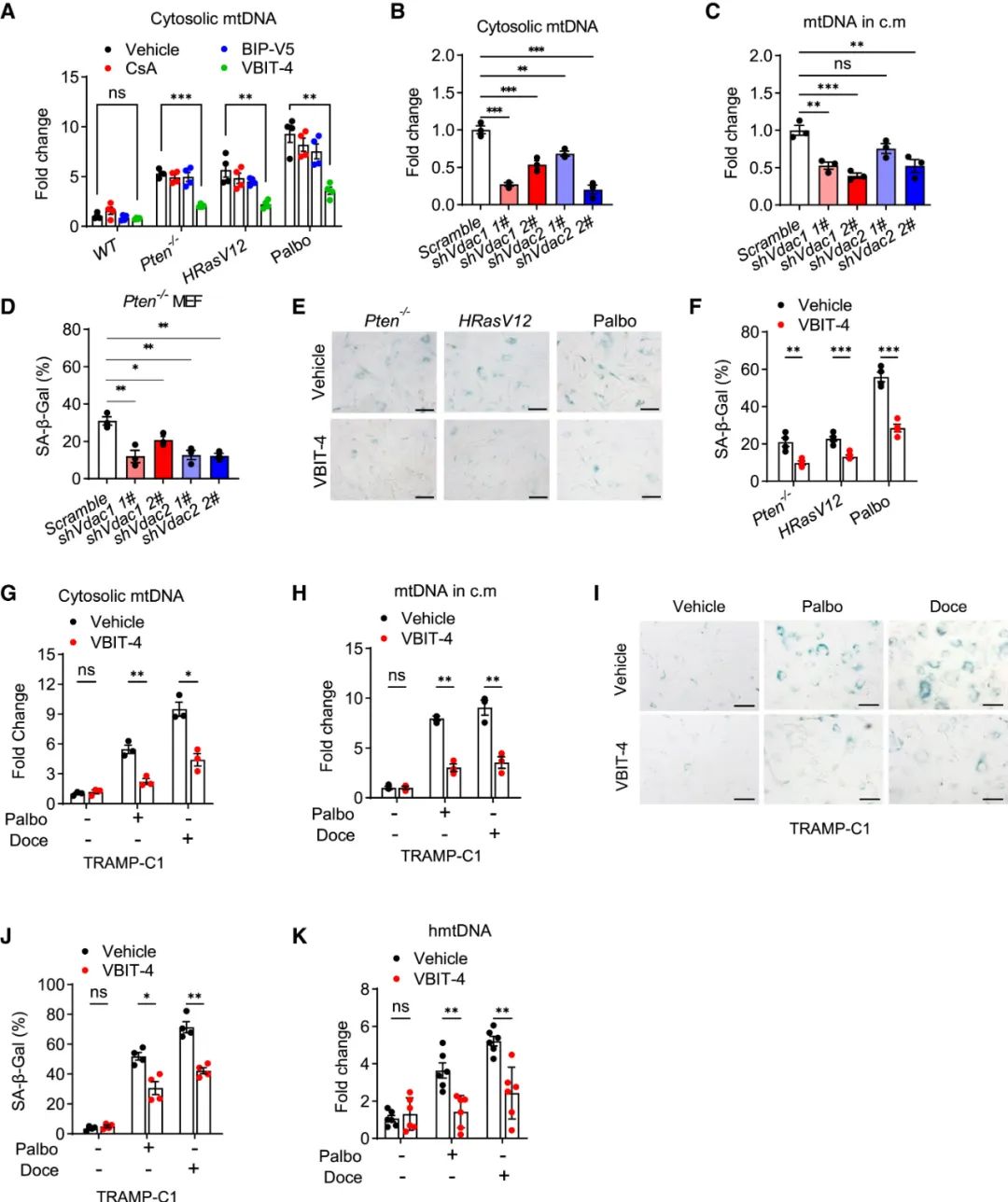
衰老癌细胞经由VDAC将线粒体释放到细胞外
参考文献:
[1]Lai P, Liu L, Bancaro N, et al. Mitochondrial DNA released by senescent tumor cells enhances PMN-MDSC-driven immunosuppression through the cGAS-STING pathway[J]. Immunity, 2025, 58(4): 811-25.e7.
[2]Lin M, Liu N, Qin Z, et al. Mitochondrial-derived damage-associated molecular patterns amplify neuroinflammation in neurodegenerative diseases[J]. Acta Pharmacologica Sinica, 2022, 43(10): 2439-2447.
[3]Victorelli S, Salmonowicz H, Chapman J, et al. Apoptotic stress causes mtDNA release during senescence and drives the SASP[J]. Nature, 2023, 622(7983): 627-636.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Science:一种经过改造的肠道细菌有望对抗肾结石 (2025-07-26)
- Science:人类首次实现 用“专属食物”精准遥控肠道内的活体药物 (2025-07-26)
- Science子刊:一种新发现的lncRNA可能解释了2型糖尿病患者肌肉量减少的原因 (2025-07-26)
- 中国药企如何“智闯”沙特? (2025-07-26)
- 马来西亚医疗旅游理事会推出MYMT 2026,打造马来西亚首个医疗旅游年 (2025-07-25)
- Int J Radiat Oncol Biol Phys:MRI导航精准放疗——让高剂量直击肿瘤顽固区,疗效提升还不伤正常组织 (2025-07-25)
- 研究发现乳酸穿梭调控巨噬细胞极化并参与2型糖尿病进程 (2025-07-25)
- 癫痫手术步入毫米时代,仁济多学科联手“机器人+激光”精准消除脑内病灶 (2025-07-25)
- Science:从源头看懂食物过敏——生命早期的一波Thetis细胞浪潮,决定你一生的饮食自由 (2025-07-25)
- Mol Neurodegener:血管“信使”藏玄机,内皮糖蛋白借囊泡激活星形胶质细胞,为阿尔茨海默病治疗指新向 (2025-07-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















