CRISPR改写免疫疗法!Cancer Cell:科学家激活NK细胞抗癌潜能,直击肿瘤转移关键靶点 |
 |
来源:100医药网 2025-06-17 14:18
来自澳大利亚生物技术公司oNKo-innate的科学家们通过研究发现,通过调节一种名为IL-15的生长因子就能增强自然杀手(NK)细胞的抗癌能力。世界卫生组织数据显示,全球每年约 1930 万癌症新发病例中,1000 万人因癌离世。尽管免疫检查点抑制剂(如 PD-1 抗体)已革新癌症治疗,但仍有大量患者面临「无响应」或「耐药」难题。其中,自然杀伤细胞(NK 细胞)作为抗癌第一道防线,其活性常被肿瘤微环境抑制 而 IL-15 作为调控 NK 细胞功能的核心细胞因子,虽能增强 NK 细胞杀伤能力,却因全身给药的毒性问题(如细胞因子风暴)限制了临床应用。
澳大利亚 oNKo-innate 公司与莫纳什大学团队在《Cancer Cell》的研究揭示:肿瘤细胞可通过 UBE2F 和 ARIH2 基因介导的 IL-15 受体(IL-15R)降解,削弱 NK 细胞对 IL-15 的敏感性。而靶向这一机制,既能规避全身毒性,又能特异性激活肿瘤局部的 NK 细胞抗癌能力。

在本研究中,研究团队利用 CRISPR-Cas9 技术,在人类 NK 细胞中进行全基因组筛选:以模拟肿瘤微环境中生理浓度的低剂量 IL-15 作为筛选压力,发现 UBE2F(NEDD8 E2 连接酶)和 ARIH2(泛素 E3 连接酶)是抑制 IL-15R 信号的关键因子。并且,敲除这两个基因后,NK 细胞表面 IL-15R(CD122)的表达量提升 2 倍,对 IL-15 的敏感性显著增强!
通过进一步探究其分子机制,研究者发现:UBE2F 通过催化 CUL5 蛋白的 Neddylation(尼德化)修饰,激活 CRL5 泛素连接酶复合体;而 ARIH2 作为 CRL5 复合体的关键组分,直接介导 IL-15R 的泛素化降解。当 UBE2F 或 ARIH2 缺失时,IL-15R 免于降解,持续激活 JAK-STAT5 信号通路,进而促进 NK 细胞增殖、分泌 IFN- 和 TNF- 等细胞因子,并上调 NKp30、NKG2D 等杀伤受体的表达。
基因编辑 NK 细胞的「抗癌超能力」验证
(1)体外实验:对抗肿瘤「疲劳」与免疫抑制
抗疲劳能力:敲除 UBE2F/ARIH2 的 NK 细胞在连续 4 轮肿瘤细胞杀伤实验中,杀伤效率较对照组提升 50%,且对腺苷、TGF- 等免疫抑制因子的抵抗能力显著增强。
CAR-NK 细胞升级:在靶向 BCMA 的 CAR-NK 细胞中敲除 UBE2F,其对耐药白血病细胞的杀伤效率在第 3 轮挑战中仍维持初始水平,IFN- 分泌量增加 3 倍。
(2)动物模型:直击原发性与转移性肿瘤
肺转移模型:敲除 Arih2/Ube2f 的小鼠体内,B16F10 黑色素瘤肺转移灶数量减少 60%,NK 细胞活性显著提升。
结直肠癌模型:MC38 肿瘤在 Ube2f 敲除小鼠中生长速度减缓 70%,肿瘤微环境中 CD122+NK 细胞比例增加,Granzyme B + 杀伤性细胞占比提升 2 倍。
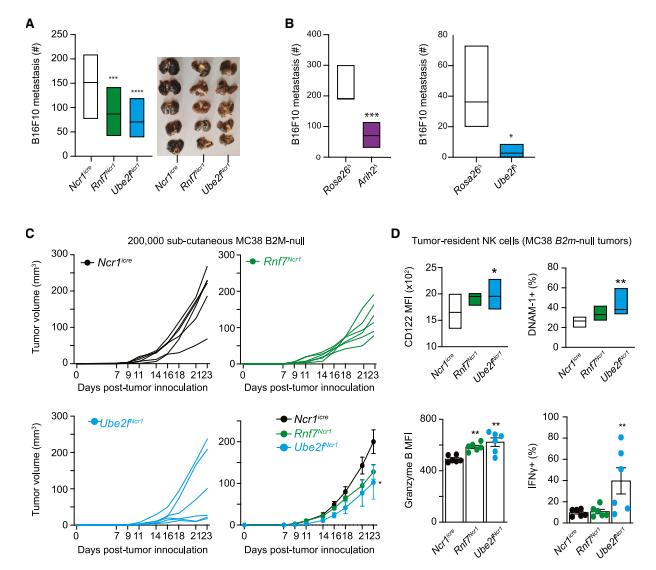
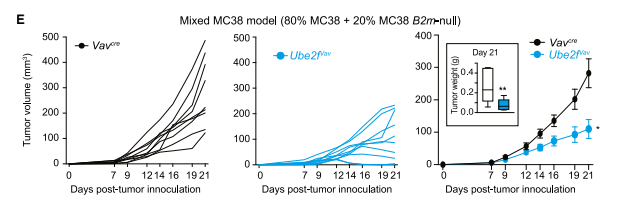
图:敲除 Ube2f、Arih2 或 Rnf7 基因的小鼠,体内原发和转移性肿瘤生长明显受抑制,肺转移模型中转移灶减少约 60%,结直肠癌模型中肿瘤体积缩小 70%
从实验室到临床
传统 IL-15 激动剂因激活外周免疫细胞易引发毒性,而靶向 UBE2F/ARIH2 仅选择性增强肿瘤局部 NK 细胞对 IL-15 的响应。实验显示,Ube2f 敲除小鼠未出现 IL-15 过表达导致的炎症反应,安全性显著优于传统疗法。
在药物开发层面,UBE2F 抑制剂可通过阻断 CUL5 激活来维持 IL-15R 表面表达,ARIH2 抑制剂则能直接阻断 IL-15R 的泛素化降解。研究已证实,NEDDylation 抑制剂 Pevonedistat 可模拟 UBE2F 缺失的效果,虽需优化剂量以降低细胞毒性,但为小分子药物开发提供了明确方向
综上,针对当前 CAR-NK 疗法面临的 持久性差 难题,该研究证实敲除 UBE2F/ARIH2 可增强 CAR-NK 细胞的抗疲劳能力,其机制可能与 mTOR 通路持续激活、糖代谢增强相关。这一发现为 基因编辑 + CAR-NK 联合疗法提供了理论基础,有望突破血液瘤与实体瘤治疗的瓶颈。
参考文献:
Iva Nikolic,Joseph Cursons,Benjamin Shields, et al. Enhancing Anti-Tumor Immunity of Natural Killer Cells through Targeting IL-15R Signaling, Cancer Cell (2025). DOI: 10.1016/j.ccell.2025.05.011.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Science:一种经过改造的肠道细菌有望对抗肾结石 (2025-07-26)
- Science:人类首次实现 用“专属食物”精准遥控肠道内的活体药物 (2025-07-26)
- Science子刊:一种新发现的lncRNA可能解释了2型糖尿病患者肌肉量减少的原因 (2025-07-26)
- 中国药企如何“智闯”沙特? (2025-07-26)
- 马来西亚医疗旅游理事会推出MYMT 2026,打造马来西亚首个医疗旅游年 (2025-07-25)
- Int J Radiat Oncol Biol Phys:MRI导航精准放疗——让高剂量直击肿瘤顽固区,疗效提升还不伤正常组织 (2025-07-25)
- 研究发现乳酸穿梭调控巨噬细胞极化并参与2型糖尿病进程 (2025-07-25)
- 癫痫手术步入毫米时代,仁济多学科联手“机器人+激光”精准消除脑内病灶 (2025-07-25)
- Science:从源头看懂食物过敏——生命早期的一波Thetis细胞浪潮,决定你一生的饮食自由 (2025-07-25)
- Mol Neurodegener:血管“信使”藏玄机,内皮糖蛋白借囊泡激活星形胶质细胞,为阿尔茨海默病治疗指新向 (2025-07-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















