利什曼原虫胞外囊泡介导感染与免疫调控!mBio揭示寄生虫-宿主互作及诊疗新靶点机制 |
 |
来源:100医药网 2025-10-10 12:28
利什曼原虫及其感染细胞释放的胞外囊泡可携带毒力因子、调节宿主免疫反应,为利什曼病的诊断与治疗提供新方向。在全球寄生虫病谱里,利什曼病虽不如疟疾 声名远扬 ,却悄无声息地威胁着数百万患者的健康 皮肤溃疡、内脏器官受损是它的典型 印记 。近日,mBio发表的一篇文章mGem: Extracellular vesicles inLeishmania-secret messengers driving infection and disease,聚焦利什曼原虫分泌的胞外囊泡(EVs),为我们解开这种寄生虫 操控 感染与疾病进程的机制,也点亮了的新希望。

利什曼原虫的生命周期复杂,在昆虫宿主中以 前鞭毛体 形式存在,进入人类等脊椎动物宿主后,会转化为 无鞭毛体 并寄生在吞噬细胞内。和其他真核生物一样,利什曼原虫及受其感染的细胞会释放EVs 这类由脂质双分子层包裹、不含复制元件的颗粒,能携带蛋白质、核酸、代谢物等活性分子,在细胞间 传递信号 ,尤其在宿主与病原体的相互作用中左右疾病走向。EVs依据生成途径可分为外泌体、微囊泡(ectosomes)和凋亡小体三类,早有研究证实,利什曼原虫及其感染细胞分泌的EVs会参与宿主-病原体互作,推动疾病发生发展。
EVs是利什曼原虫 投放 毒力因子的核心载体。为了躲避攻击、实现自身存活增殖,利什曼原虫进化出多种策略,释放EVs就是关键一招。质谱研究显示,利什曼原虫可通过EVs分泌蛋白质,外泌体更是它向宿主细胞递送蛋白的 通用通道 ,且在受感染巨噬细胞的胞质中,能检测到利什曼原虫来源的EVs。尽管EVs的生物发生机制尚未完全阐明,但蛋白质组分析发现,其包含内体机制相关蛋白及内体分选复合物(ESCRT)通路成分 要知道,ESCRT通路正是外泌体生成和释放的 幕后推手 。
利什曼原虫来源的EVs中,藏着不少关键分子:毒力因子、细胞代谢蛋白、免疫介质等都在其中。比如虫体表面最丰富的蛋白gp63,它能帮原虫逃避补体溶解、降解胞外基质,还能抑制宿主细胞的p38-MAP激酶通路。含gp63的EVs在昆虫载体中也能被检测到,当原虫传播给脊椎动物宿主时,EVs会和原虫一同分泌;更关键的是,把利什曼原虫与虫源EVs一起接种,会让疾病变得更重 这说明感染初期的相互作用,EVs也 功不可没 。不过,目前多数研究聚焦体外培养的前鞭毛体EVs,沙蝇体内EVs的研究还很少,比如 体外EVs的携带物是否和自然感染沙蝇中的一致 EVs是否参与沙蝇体内原虫的循环分化 等问题,还需要进一步探索。
除了蛋白质,利什曼原虫RNA病毒1(LRV1)也会 搭便车 EVs:EVs能作为病毒的 包膜 ,帮助LRV1在不同原虫群体间传播,还能向脊椎动物宿主递送病毒。要知道,LRV1的存在会让利什曼病更严重,感染携带LRV1的利什曼原虫的患者,治疗失败的风险也更高。此外,利什曼原虫还能通过EVs交换耐药基因;至于其携带的非编码RNA(如rRNA、tRNA)是否能调节细胞信号或基因表达,也值得深入挖掘。
利什曼原虫来源的EVs,对宿主免疫细胞功能的影响同样显著。无鞭毛体是致病阶段,会寄生并增殖于巨噬细胞内,因此巨噬细胞对EVs的反应备受关注。当巨噬细胞暴露于利什曼原虫EVs时,会 上调 促炎介质的生成,推动疾病进展;同时,EVs还会通过激活toll样受体(TLRs)来调节免疫,比如诱导巨噬细胞向 M2型 极化 这种极化状态对利什曼原虫的存活十分有利。从机制上看,利什曼原虫EVs富含多胺,巨噬细胞高效摄取多胺后,感染率会升高,且M2型标志物 精氨酸酶1 的表达也会增加。另外,含gp63的EVs除了加重疾病,也参与免疫调节。不仅如此,利什曼原虫EVs还能刺激白细胞介素-8(IL-8)、粒细胞集落刺激因子(G-CSF)及内皮生长因子-A(VEGF-A),促进血管生成 这在皮肤利什曼病特征性皮肤溃疡的形成中,可能发挥着重要作用。
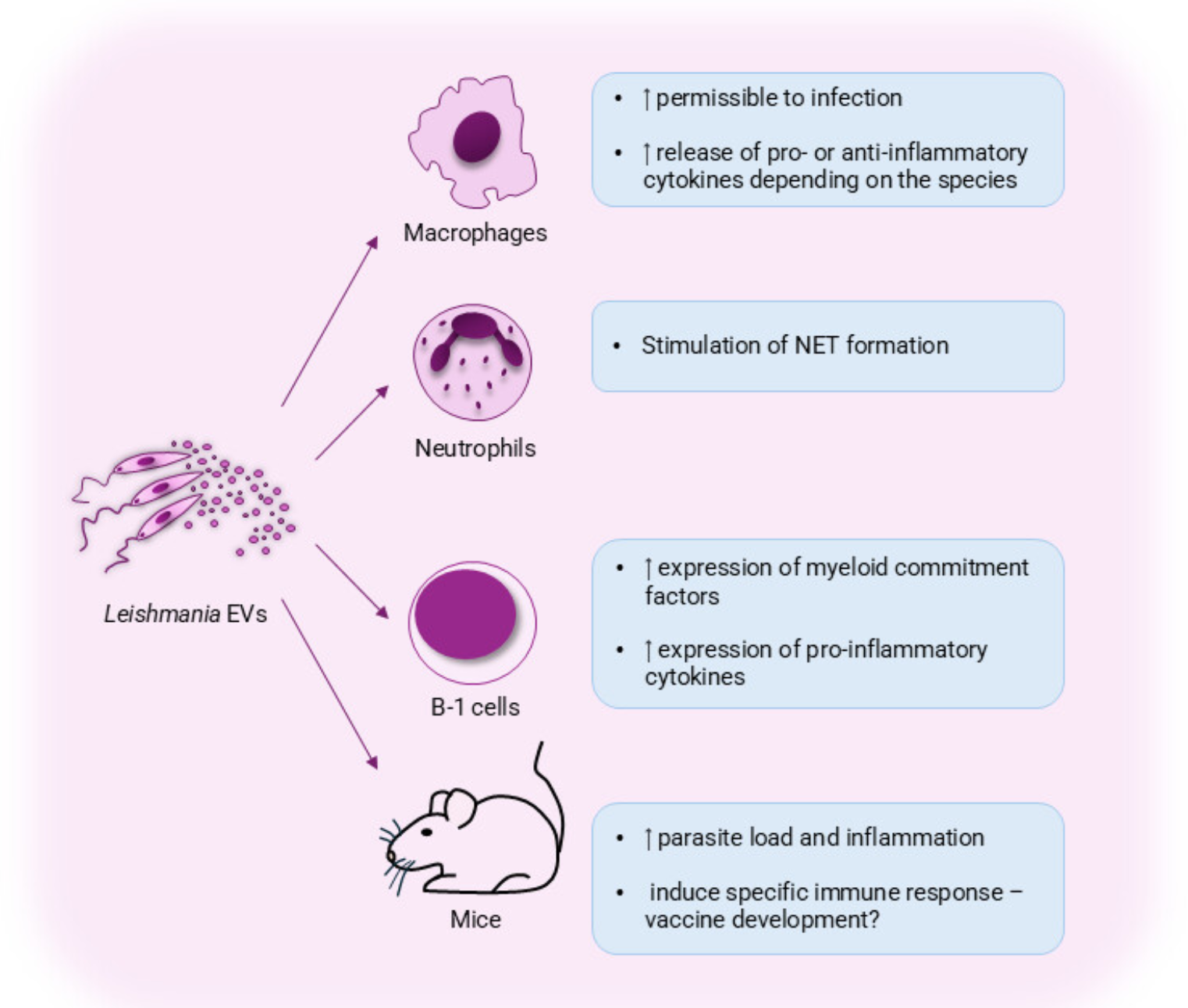
图1 利什曼病中的胞外囊泡:利什曼原虫来源的胞外囊泡对免疫细胞活化及疾病发展的影响
在人源细胞中,也能观察到类似效应:用利什曼原虫EVs预处理人巨噬细胞,会诱导炎性细胞因子生成及炎性小体活化;不过,经EVs刺激的巨噬细胞感染利什曼原虫后,虫荷并没有显著变化,这说明EVs主要调节先天免疫反应,而非直接促进原虫复制。当人中性粒细胞暴露于利什曼原虫EVs后,会通过TLR激活释放中性粒细胞胞外陷阱(NETs),而NETs对前鞭毛体有杀伤作用。这些结果表明,利什曼原虫EVs能激活人类先天免疫,进而可能影响适应性免疫应答。未来,还需研究EVs对其他细胞的作用,比如 原虫在巨噬细胞内稳定定植后,旁体细胞是否更易感染 是否助力原虫持续存在 是否进一步加剧皮肤利什曼病的炎症反应 等。
除了巨噬细胞和中性粒细胞,利什曼原虫EVs还能调节B细胞,尤其是具有免疫调节功能的B-1细胞亚型。用亚马逊利什曼原虫EVs刺激B-1细胞,会使其髓系定向因子及肿瘤因子- (TNF- )表达增加,提示B-1细胞可能向吞噬细胞样表型转化,增强杀菌能力;而预先接触B-1细胞释放的EVs的小鼠,在实验性感染中预后更好。这揭示了EVs在免疫调节中的 双重性 :虫源EVs可能通过调节宿主免疫促进感染,而宿主来源的EVs或可介导保护性免疫。理解这种平衡,对发现新的免疫调节机制及抗利什曼原虫感染治疗策略至关重要。
在与治疗领域,利什曼原虫EVs也展现出潜力。诊断上,利用利什曼原虫EVs开发的血清学检测方法,对感染者血清的识别灵敏度达95%、特异性达100%;对感染利什曼病的犬血清分析发现,其EVs携带微小RNA(miRNA),提示EVs有望作为疾病生物标志物。治疗上,间充质(MSCs)来源的EVs可部分控制实验性感染的病灶发展,且不影响虫荷;而MSCs来源的EVs与化疗联合使用时,能产生协同效应。因此,MSCs或B-1细胞来源的EVs,因具有免疫调节特性,有望用于 宿主导向治疗 ,尤其适用于炎症反应强烈的利什曼病临床类型。
从感染机制到诊疗潜力,利什曼原虫胞外囊泡就像一串 关键密码 ,串联起寄生虫与宿主的相互作用,也为疾病的诊断和治疗开辟了新路径。随着研究的不断深入,这些 微观信使 有望成为利什曼病防控的 突破口 ,为全球数百万患者带来康复的希望。(100yiyao.com)
参考文献:
Xander P, de Oliveira CI. mGem: Extracellular vesicles inLeishmania-secret messengers driving infection and disease.mBio. Published online September 22, 2025. doi:10.1128/mbio.03239-24
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 对于展开西医劣势病种按病种付费试点任务的关照 (2025-10-10)
- 利什曼原虫胞外囊泡介导感染与免疫调控!mBio揭示寄生虫-宿主互作及诊疗新靶点机制 (2025-10-10)
- Cell:同样的致病突变,为何表型天差地别?研究揭示:遗传背景才是真正的“幕后导演” (2025-10-10)
- 体检后的“黄金干预期”找到了!哈佛追踪 30 年证实:肠镜后改习惯,癌症、慢病双防 (2025-10-10)
- 天津:推进优质医疗资本下沉 完成精力科门诊全笼罩 (2025-10-10)
- 国度医保局颁布团体骗取医保基金典型案例(第二期) (2025-10-10)
- Cell子刊:复旦大学章真/华国强利用类器官预测直肠癌患者对放化疗的响应 (2025-10-09)
- 中国博后一作Nature论文:开发AI模型,高精度预测酶的特异性,已回国加入南京师范大学 (2025-10-09)
- 突破脊髓调控性行为传统认知!Nat Commun:腰脊髓甘丙肽阳性神经元调控雄性小鼠交配与射精的核心机制 (2025-10-09)
- 内蒙古大学×同济大学合作发表Nature Biotechnology论文:突破牛羊基因编辑育种瓶颈 (2025-10-09)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















