非典型抗精神病药物!住友制药Latuda(盐酸鲁拉西酮)在日本获批,已在中国上市! |
 |

2020年03月27日/BIOON/--住友制药(Sumitomo Dainippon Pharma)近日宣布,非典型抗精神病药物Latuda (中文商品名:罗舒达 ,通用名:lurasidone HCl,盐酸鲁拉西酮片)在日本获得批准,用于治疗精神分裂症和双相。
Latuda的活性药物成分为lurasidone(鲁拉西酮),这是一种非典型抗精神病药物,由住友制药发现和开发。与其他现有的抗精神分裂症药物相比,鲁拉西酮具有独特的化学结构,据信对多巴胺D2、5-羟色胺(5-HT2A)、5-羟色胺(5-HT7)受体均具有亲和力,在这些受体中具有拮抗作用。此外,鲁拉西酮对5-羟色胺(5-HT1A)受体具有部分激动作用,对组胺H1或毒蕈碱M1受体无明显的亲和力。
在美国,Latuda分别于2010年和2013年获得批准治疗精神分裂症的和双相I型;在2012-2017年期间,Latuda陆续获得全球多个国家批准这2个适应症,其中2016年在中国台湾和中国香港获批精神分裂症、2017年获中国台湾批准双相I型。2019年1月底,Latuda(罗舒达 )获得中国国家药品监督管理局(NMPA)批准,用于精神分裂症成人患者治疗。2019年9月,住友制药中国子公司将Latuda(罗舒达 )推向国内市场。
在国外的指南中,Latuda被认为是一种低体重增加风险的抗精神病药物,并被推荐为治疗双相的首选药物之一。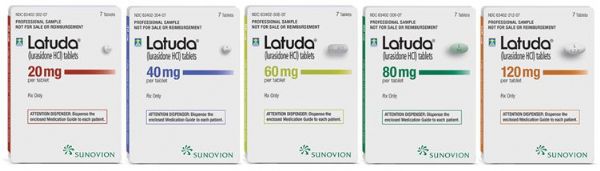
Latuda在日本的批准,涉及治疗精神分裂症患者的III期研究JEWEL以及治疗双相I型抑郁症患者的另一项III期研究ELEVATE的数据。这2项研究的数据已分别在2019年1月10日和2017年6月9日发布。
——JEWEL:是一项多中心、安慰剂对照、随机、双盲研究,在多个国家开展(包括日本),评估了lurasidone治疗精神分裂症患者的疗效和安全性。结果显示,采用预先规定的主要终点分析,在意向性治疗群体(ITT,n=478)中,治疗6周后,与安慰剂组(n=233)相比,lurasidone 40mg/天治疗组(n=245)在阳性和阴性症状量表(PANSS)总评分方面相对基线表现出统计学意义的显著改善(-19.3分 vs -12.7分,p<0.001)。此外,治疗6周后,与安慰剂组相比,lurasidone治疗组在临床总体印象严重程度量表(CGI-S)总评分方面相对基线也表现出统计学意义的显著改善,达到了研究的次要疗效终点。
——ELEVATE:是一项多中心、安慰剂对照、随机、双盲研究,在亚洲和部分欧洲国家开展(包括日本),评估了lurasidone治疗双相I型抑郁症患者的疗效和安全性。结果显示,采用预先规定的主要终点分析,在意向性治疗群体(ITT,n=522)中,治疗6周后,与安慰剂组(n=171)相比,lurasidone 20-60mg/天治疗组(n=182)在蒙哥马利抑郁评定量表(MADRS)总评分方面相对基线表现出统计学意义的显著改善(-13.6分 vs 10.6,调整后的p=0.007)。lurasidone 80-120mg/天治疗组(n=169)与安慰剂组相比MADRS总评分也显示出改善,但差异无统计学显著性(-12.6分 vs -10.6分,调整后的p=0.057)。(100医药网100yiyao.com)
原文出处:Sumitomo Dainippon Pharma Announces roval of Atypical Antychotic Agent, LATUDA Tablets in Japan
医药网新闻
- 相关报道
-
- Nature Methods:蛋白质“变形金刚”设计指南——AI“脑补”自然进化,一键生成智能分子开关 (2025-08-10)
- N Engl J Med:改写移植规则!从“免疫耐受”迈向“免疫规避”的新纪元 (2025-08-10)
- Science重磅:破解阿尔茨海默病抗体药的脑出血副作用——突破血脑屏障,靶向递送抗Aβ抗体 (2025-08-10)
- Nat Rev Neurosci重要综述:自主神经系统的分子和功能多样性——系统回顾了该领域近十年来的关键进展 (2025-08-09)
- Cancer Cell:于君团队证实,补充这种益生菌,可增强结直肠癌免疫治疗效果 (2025-08-09)
- Cancer Cell:魏嘉/李颜团队揭示未成熟中性粒细胞在癌症骨转移中的关键作用,并提出治疗新策略 (2025-08-09)
- 为何CAR-T 疗法易复发?Mol Cancer:细胞衰老成“隐形杀手”,共刺激域差异决定疗效命运 (2025-08-08)
- Nature:多发性硬化症的“元凶”现身?科学家揭示EB病毒惊人发现! (2025-08-08)
- Nature:锂缺乏或会诱发阿尔兹海默病,但锂化合物却能逆转小鼠疾病 (2025-08-08)
- 不止供能,还能抗癌?!Cell Metabol:葡萄糖能帮抗癌 T 细胞“充电”!糖鞘脂合成是关键 (2025-08-08)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















